
CUMPLIR CON LA FECHA LÍMITE DE CUMPLIMIENTO DE IDMP PARA JULIO DE 2016: NO ES UNA TAREA TRIVIAL
Existen muchas preguntas sobre IDMP, por ejemplo: ¿dónde se encuentran los datos en una organización? ¿Se requiere la limpieza y alineación de los datos actuales? ¿Cómo organizan las empresas estos datos para facilitar su recuperación y envío? ¿Tiene la organización procesos que puedan beneficiarse de un repositorio central?
Lograr el cumplimiento de la Identificación de Productos Medicinales (IDMP) no es una tarea trivial; la actividad debe tener en cuenta diversas presiones reglamentarias y operativas. Las organizaciones deben esperar hasta que las autoridades emitan la guía final y aprueben las especificaciones. Al mismo tiempo, esperar estas guías podría no dejarles tiempo suficiente para organizar sus asuntos.
IDMP es un estándar complejo con implicaciones de datos generales que requiere colaboración y cooperación entre muchas unidades interfuncionales. La transición ofrece la oportunidad de una visión End-to-End de los procesos de negocio y las capacidades de TI de una organización en muchas unidades funcionales. También ayuda a establecer un sólido sistema de gestión de cambios.
Las organizaciones deben comprender que una buena arquitectura de la información requiere esfuerzo y tiempo para lograrse, y también deben reconocer que IDMP no es solo un XEVMPD más grande. También es importante señalar que la guía ICH es solo una parte de la historia, y la disponibilidad de guías regionales es fundamental. También hay que tener en cuenta que las implementaciones regionales paralelas tendrán alcances y plazos diferentes, con una amplia gama de colaboradores de datos.
Además, las empresas farmacéuticas que deseen comercializar en regiones reguladas deben cumplir con IDMP a partir de 2016. Recientemente, la EMA organizó un día de información sobre IDMP y compartió el estado y los plazos de implementación de alto nivel de IDMP. Después de discutir con la industria farmacéutica, los proveedores de software y analizar su propio sistema y la disponibilidad de recursos, la EMA ha planeado dividir la implementación general de EU-IDMP en múltiples iteraciones. Este plan se propondrá a la Comisión Europea (CE) para su aprobación y, si logran convencer a la CE, la implementación de IDMP en la UE se extenderá entre 2016 y 2018. En el peor de los casos, si la CE no está de acuerdo, no hay un plan B. Las multas por incumplimiento ascienden hasta el 5% de los ingresos de una organización; no tener una buena solución para el cumplimiento inicial y continuo de IDMP es un riesgo que ninguna empresa farmacéutica puede permitirse asumir.
IDMP: DESARROLLADO COMO UN CONJUNTO GLOBAL DE ESTÁNDARES BAJO ISO
En caso de que se introduzca alguna legislación sobre la identificación de medicamentos en cualquiera de los países ISO, se hará basándose en los estándares ISO IDMP. Una vez que las diferentes regiones adopten los estándares IDMP, la entrada de datos será consistente y a su vez, las empresas globales y los reguladores tendrán acceso a la verificación cruzada de datos para garantizar la coherencia entre las regiones. Además, los vocabularios controlados comunes facilitarán en gran medida este proceso.
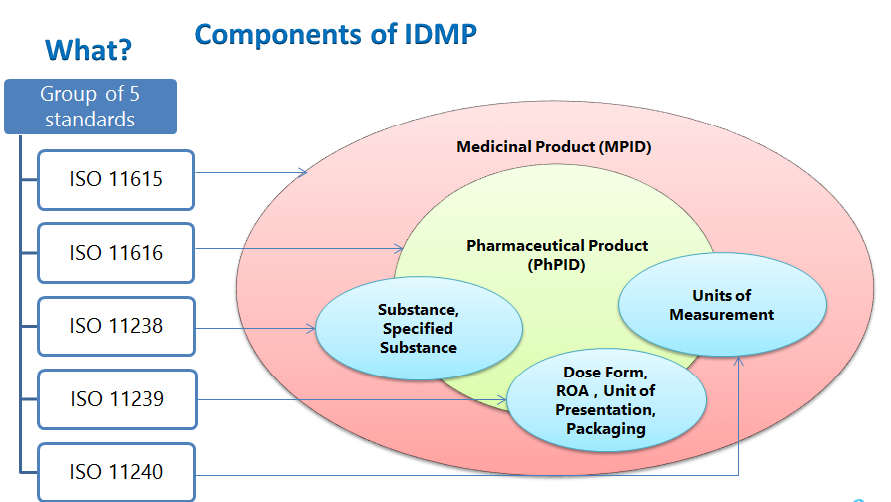
Los elementos estructurales de IDMP incluyen la identificación del producto medicinal, la identificación del producto farmacéutico, la identificación de la sustancia, los vocabularios controlados (forma farmacéutica), la vía de administración, los componentes del envase, las unidades de presentación, las unidades de medida y la descripción del proceso de fabricación a presentar.
ESTÁNDARES IDMP
- ISO 11615 – Información del producto medicinal
- ISO 11616 – Información del producto farmacéutico
- ISO 11238 – Sustancias
- ISO 11239 – Formas farmacéuticas, Unidades de presentación, Vías de administración y Envases
- ISO 11240 – Unidades de medida
Estado actual
ICH está preparando guías de implementación y revisando las normas ISO
Reguladores de la UE se preparan para IDMP
- La EMA ha iniciado trabajos para establecer contacto con la red reglamentaria de la UE para definir los casos de negocio para los datos IDMP
- La EMA está estableciendo un “Grupo de trabajo de la UE para ISO IDMP reclutando expertos de los Comités de la EMA y de la Junta de Datos de la Red de la UE para lograrlo. Específicamente, hará lo siguiente:
- Definir los elementos de datos ISO IDMP obligatorios y opcionales.
- Definir las reglas de negocio para los elementos de datos opcionales
- Definir la conformidad y los tipos de datos
- Definir los modelos de gobernanza de la UE
POSICIÓN DE LOS REGULADORES DE US
- Liderazgo activo para impulsar IDMP con los organismos reguladores globales (antiguo ICH) y con ISO
OTROS ORGANISMOS REGULADORES
- Suiza – Tiene la intención de implementar después de la UE (seguidor rápido)
- Japón y Canadá han nominado a reguladores para ser expertos en el grupo IG de Sustancias
CRONOLOGÍAS
GUÍAS EUROPEAS DE IMPLEMENTACIÓN
- Se inició el borrador de las guías de implementación y las guías estarán disponibles a partir del primer trimestre de 2016.
OTROS
- La FDA aún no tiene fecha, pero tiene la intención de evolucionar el SPL según sea necesario
- Japón – Incierto en ICH, pero ahora trabajando dentro del grupo del regulador e ISO
- Canadá – Se espera que implemente, pero aún sin detalles específicos
- Suiza – Sin actualizaciones todavía
COMPRENDIENDO LOS REQUISITOS DE CUMPLIMIENTO DE IDMP
IDMP requiere información sobre productos medicinales en términos de un conjunto de identificadores estándar, que se construyen sobre una jerarquía de identificación creada al elaborar el Diccionario de Productos Medicinales de EudraVigilance (EVMPD) o en su forma extendida (xEVMPD). Habrá una superposición de información con la presentada en las presentaciones de Structured Product Labeling (SPL) en los US y otros registros de productos a nivel mundial.
Sin embargo, IDMP tiene nuevos identificadores, nuevas categorías y nuevas formas de expresar las relaciones entre los elementos en el modelo de datos. IDMP debe integrarse en el ADN de la organización, ya que necesita impulsar la construcción de modelos de datos en toda su empresa. La infraestructura de TI de una organización puede entonces reconocerlo en múltiples sistemas, procesos de negocio y unidades funcionales como RA, Seguridad, I+D, documentación y procesos de fabricación.
DESAFÍOS DE CUMPLIMIENTO DE IDMP
Organizativo
- Datos distribuidos entre múltiples departamentos
- Se requiere patrocinio de alto nivel para fomentar la participación
Técnico
- Descubrir, recopilar y consolidar, limpiar datos
- 250 a 300 campos por producto
Coordinación
- Gestión del cambio continuo
- Coordinación entre varios equipos
- Mantener la normativa de datos con procesos internos
EN CONCLUSIÓN:
IDMP: IMPACTO EN LA INDUSTRIA FARMACÉUTICA
Se espera que la implementación de los estándares IDMP tenga un impacto en la preparación y planificación de las presentaciones y el mantenimiento de los datos de toda la empresa, incluyendo datos de fabricación e información estructurada de sustancias, hasta la información de registro.
ESTÁNDAR IDMP: GANANCIAS DE EFICIENCIA ASEGURADAS TRAS LA IMPLEMENTACIÓN
Asegurarse de que su organización esté lista para afrontar el desafío de IDMP requerirá una estrecha cooperación entre múltiples departamentos dentro de su organización. Un proveedor de servicios competente con una cartera exclusiva de competencias reglamentarias puede ayudar a avanzar hacia el cumplimiento de IDMP, lo que puede ayudar a una organización a responder a las nuevas oportunidades que surgen en el mercado.










