
Las auditorías de Buenas Prácticas de Fabricación (GMP) y Buenas Prácticas de Distribución (GDP) son fundamentales para garantizar la calidad, seguridad e integridad de los productos farmacéuticos a lo largo de su ciclo de vida. Realizar investigaciones exhaustivas durante estas auditorías es esencial para identificar y corregir cualquier desviación, problema de incumplimiento o riesgo potencial. En esta entrada de blog, exploraremos la importancia de las investigaciones en profundidad durante las auditorías GMP/GDP y ofreceremos información valiosa sobre cómo llevar a cabo investigaciones eficaces para el cumplimiento reglamentario.
Comprendiendo la Importancia de las Investigaciones Exhaustivas
- Identificar las causas raíz: Las investigaciones exhaustivas ayudan a descubrir las causas subyacentes de las desviaciones o los problemas de incumplimiento, lo que permite a las empresas abordar las causas raíz en lugar de solo tratar los síntomas.
- Prevenir la recurrencia: Al comprender las causas raíz, las empresas pueden implementar acciones correctivas y preventivas (CAPA) para evitar que problemas similares se repitan en el futuro, mejorando así el cumplimiento general y la calidad del producto.
- Garantizar la seguridad del producto: Las investigaciones exhaustivas aseguran que cualquier riesgo potencial para la seguridad o eficacia del producto se identifique y mitigue rápidamente, salvaguardando la salud y el bienestar del paciente.
- Mantener el cumplimiento reglamentario: Las autoridades reglamentarias esperan que las empresas realicen investigaciones exhaustivas sobre las desviaciones de GMP/GDP y tomen las medidas correctivas adecuadas para mantener el cumplimiento de las normas reglamentarias.
Pasos clave para llevar a cabo investigaciones exhaustivas:
- Revisión de documentos: Comience revisando la documentación relevante, incluyendo los procedimientos operativos estándar (SOPs), los registros de lotes, los informes de desviación y los hallazgos de auditorías anteriores para obtener información sobre el problema en cuestión.
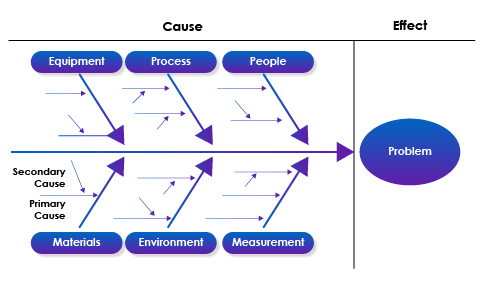
- Análisis de la causa raíz: Utilice herramientas y metodologías como los 5 porqués, los diagramas de espina de pescado (Ishikawa) o el análisis de modos y efectos de fallas (FMEA) para identificar sistemáticamente las causas raíz de las desviaciones o los problemas de incumplimiento.
Diagrama de espina de pescado como ejemplo.
- Recopilación de datos: Recopile datos y pruebas relevantes a través de entrevistas, observaciones y análisis de datos para respaldar los hallazgos y conclusiones de la investigación.
- Colaboración Interfuncional: Involucre a equipos interfuncionales, incluidos los de garantía de calidad, fabricación, cadena de suministro y Asuntos Regulatorios, en el proceso de investigación para garantizar una comprensión exhaustiva del problema y facilitar la resolución eficaz de este.
- Acciones Correctivas y Preventivas (CAPAs): Desarrolle e implemente CAPAs basándose en los hallazgos de la investigación para abordar las causas raíz y prevenir la recurrencia de problemas similares en el futuro.
- Mejora continua: Utilice los conocimientos obtenidos de las investigaciones para impulsar iniciativas de mejora continua, como la optimización de procesos, programas de capacitación o actualizaciones tecnológicas, para mejorar la calidad general y el cumplimiento.
Conclusión:
Realizar investigaciones exhaustivas durante las auditorías de GMP/GDP es esencial para mantener el cumplimiento, garantizar la calidad del producto y proteger la seguridad del paciente. Al seguir procesos de investigación sistemáticos, identificar las causas raíz e implementar acciones correctivas y preventivas sólidas, las empresas pueden fortalecer sus sistemas de gestión de calidad y demostrar su compromiso con el cumplimiento reglamentario y la mejora continua. Las investigaciones eficaces no solo mitigan los riesgos, sino que también contribuyen a construir una cultura de calidad y excelencia dentro de la organización.










