
En la industria farmacéutica, la seguridad del paciente depende de un factor fundamental: la consistencia en la calidad del producto. Cada comprimido, vial o inyección que llega al paciente debe funcionar exactamente según lo previsto. Esta consistencia es el resultado de una rigurosa validación de procesos (PV) regulada por un sólido marco de garantía de calidad (QA).
La validación de procesos es una filosofía de calidad que garantiza que los procesos de fabricación se comprendan bien, estén controlados y sean capaces de ofrecer de forma sistemática productos que cumplan con las especificaciones predefinidas. Desde la QA , la validación de procesos pasa de ser un mero trámite de cumplimiento normativo a convertirse en una medida proactiva para salvaguardar tanto la integridad del producto como la salud del paciente.
¿Qué es la validación de procesos?
Según las directrices de FDA ICH , la validación de procesos es «la recopilación y evaluación de datos, desde la fase de diseño del proceso hasta la producción comercial, que establece la evidencia científica de que un proceso es capaz de producir productos de calidad de forma sistemática».
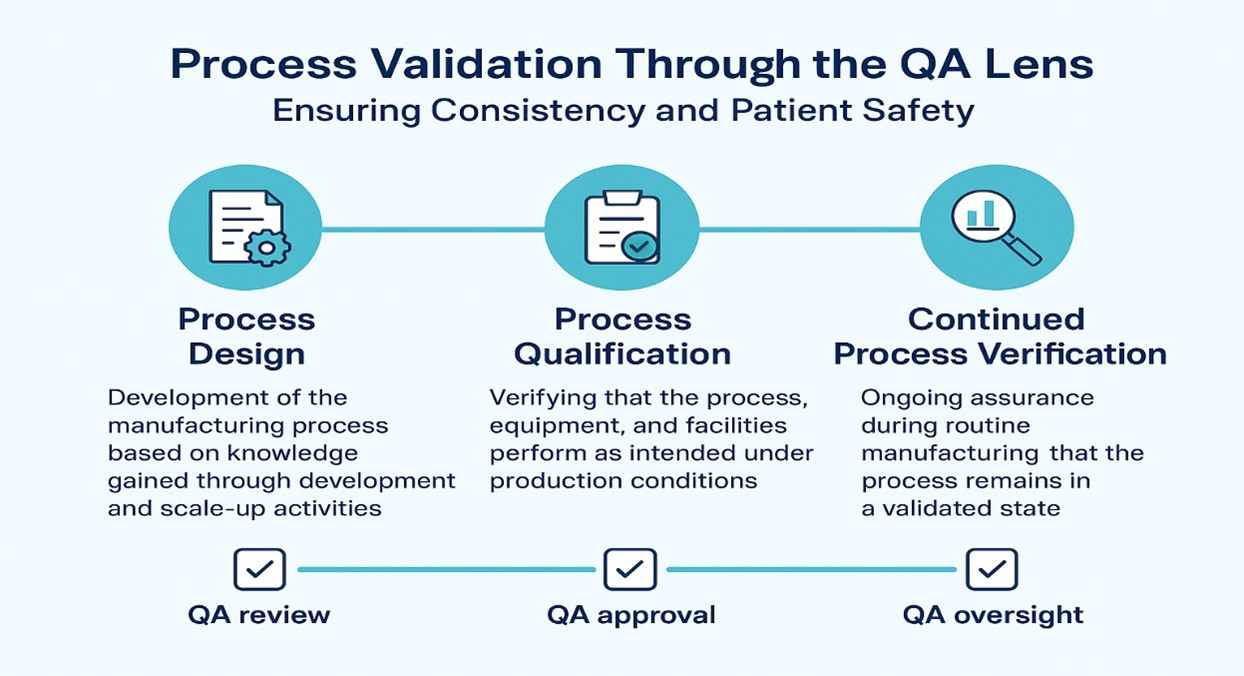
El ciclo de vida de la validación suele incluir tres (3) etapas fundamentales:
- Fase 1 – Diseño del proceso:
Desarrollo del proceso de fabricación basado en los conocimientos adquiridos a través de actividades de desarrollo y ampliación de escala.
QAFunciónQA: garantizar la aplicación de las evaluaciones de riesgos, los controles de diseño y los principios de «calidad desde el diseño» (QbD). - Fase 2 – Calificación del proceso:
Verificar que el proceso, los equipos y las instalaciones funcionen según lo previsto en condiciones de producción.
QAFunciónQA: aprobar los protocolos de calificación, revisar las desviaciones y garantizar la integridad de los datos durante la ejecución. - Fase 3 – Verificación continua del proceso (CPV):
Garantía permanente, durante la fabricación rutinaria, de que el proceso se mantiene en un estado validado.
QAFunciónQA: Implementar análisis de tendencias, métricas de calidad y sistemas de CAPA para mantener el control.
QA : más allá de la documentación
Si bien la validación de procesos implica evaluaciones técnicas y estadísticas, la QA garantiza que se lleve a cabo con rigor científico y en cumplimiento de la normativa. La responsabilidad QAabarca todas las fases, desde la planificación y la aprobación del protocolo hasta la gestión de cambios y la verificación continua.
- Enfoque basado en el riesgo
QA un papel fundamental en la adopción de un enfoque basado en el riesgo, tal y como se define en ICH . Los parámetros críticos del proceso (CPP) y los atributos críticos de calidad (CQA) se identifican, evalúan y supervisan para minimizar los riesgos. QA que los protocolos de validación sean estadísticamente sólidos y que los planes de mitigación de riesgos se integren en el diseño.
- Integridad y trazabilidad de los datos
En la era la transformación digital, la integridad de los datos sigue siendo un aspecto fundamental para QA. Los principios ALCOA+ (atribuible, legible, contemporáneo, original, preciso, además de completo, coherente, duradero y disponible) rigen cada proceso de introducción y revisión de datos. QA que los datos de validación —desde la cualificación de los equipos hasta los registros de lotes— sean trazables, estén verificados y cumplan con 21 CFR Part 11 .
- Mejora continua mediante el CPV
Tras la validación, QA el rendimiento de los procesos mediante el control estadístico de procesos (SPC) y herramientas de análisis de tendencias. Las desviaciones o los resultados que se salen de la tendencia dan lugar a la aplicación de medidas correctivas y preventivas (CAPA) con el fin de mejorar continuamente la capacidad de los procesos. Este sistema de circuito cerrado refuerza el cumplimiento normativo a largo plazo y reduce la variabilidad del producto.
Expectativas normativas y estándares internacionales
Los organismos reguladores de todo el mundo, entre ellos laFDA US , EMA, MHRA y WHO, esperan que las empresas farmacéuticas demuestren la validación de los procesos mediante un enfoque basado en el ciclo de vida. QA el cumplimiento de estas directrices en constante evolución, en particular:
- FDA para la industria: Validación de procesos: Principios y prácticas generales
- ICH (Desarrollo farmacéutico), Q9 (Gestión de riesgos de calidad) y Q10 (Sistema de calidad farmacéutica)
- Anexo 15 de la UE: Calificación y validación
Al mantener una documentación armonizada y la trazabilidad, QA la preparación para las inspecciones y el cumplimiento normativo a nivel mundial, independientemente de las variaciones regionales.
Retos en la validación de procesos y QA
Desafío | Solución QA |
|---|---|
Datos inconsistentes entre lotes | Implantar registros electrónicos de lotes (EBR) y puntos de control para la revisión QA |
Falta de justificación estadística en el muestreo | QA el protocolo se ajuste a los niveles de confianza estadística (por ejemplo, intervalos de confianza del 95 %). |
Documentación insuficiente | QA sistemas de control de documentos y una trazabilidad SOP |
Desviaciones durante la validación | QA la gestión de desviaciones, el análisis de las causas raíz y la implementación de medidas correctivas y preventivas |
Gestión del ciclo de vida | QA los programas de CPV y los criterios de revalidación estén claramente definidos |
La transformación digital en QA la validación de procesos
QA actuales están aprovechando la automatización y las plataformas de validación digital para mejorar la eficiencia y la precisión. Herramientas como los sistemas de gestión del ciclo de vida de la validación (VLMS) permiten la colaboración en tiempo real entre los equipos QA, fabricación y validación.
La experiencia de Freyr en validación de sistemas informáticos (CSV) y garantía de calidad del software (CSA) ayuda a los clientes a adoptar estrategias de validación digital que cumplen con la normativa, son escalables y están preparadas para las inspecciones. Esto garantiza no solo el cumplimiento normativo, sino también la excelencia operativa y plazos de lanzamiento de productos más rápidos.
Generar confianza a través de la calidad
La validación de procesos es un compromiso constante con la calidad, la seguridad y la confianza de los pacientes. Mediante QA , las empresas farmacéuticas pueden garantizar que sus procesos no solo estén validados, sino que se mejoren continuamente para cumplir con los más altos estándares internacionales.
Al integrar QA cada fase de la validación de procesos, las organizaciones refuerzan su sistema de gestión de la calidad (SGC), reducen el riesgo normativo y cumplen su promesa fundamental: ofrecer productos seguros y eficaces a los pacientes de todo el mundo.
En Freyr, nuestro equipo de expertos QA validación colabora con empresas farmacéuticas internacionales para establecer marcos de validación sólidos, conformes con la normativa y preparados para las inspecciones. Desde la corrección de sistemas de gestión de la calidad y el desarrollo de estrategias de validación de procesos hasta QA digital QA , Freyr garantiza una perfecta alineación con la normativa y la excelencia operativa.
Descubre cómo Freyr puede ayudarte a alcanzar la excelencia en la validación.










