
En Hong Kong, el proceso de aprobación de medicamentos huérfanos para enfermedades raras, especialmente aquellos que contienen Nuevas Entidades Químicas o Biológicas (NCEs) para enfermedades potencialmente mortales o gravemente debilitantes, es gestionado por la Junta de Farmacia y Venenos de Hong Kong. A continuación, se presenta una guía paso a paso para navegar por el proceso:
Guía paso a paso para la autorización de medicamentos huérfanos para enfermedades raras
Preparación y Presentación
Prepare la solicitud, incluyendo los documentos principales:
- Informes de evaluación de expertos y documentos CTD sobre seguridad, eficacia y calidad
- Planes de gestión de riesgos (RMPs)
- Etiquetas de productos y prospectos
- Informes de evaluación de riesgos por impurezas elementales
- Récord mundial de matriculaciones
Presente su solicitud de registro a través del Sistema de Registro de Productos Farmacéuticos 2.0 (PRS 2.0) en el sitio web de la Oficina de Medicamentos. Este es un primer paso fundamental para quienes registran medicamentos huérfanos para enfermedades raras en Hong Kong.
Pago de tasas
Pague la tasa de solicitud a través de:
- PRS 2.0 (en línea) – mediante tarjeta de crédito o PPS
- En persona – en efectivo o con cheque en la Oficina de Medicamentos
- Examen y Evaluación
- La Oficina de Medicamentos examina todos los documentos presentados antes de aceptar la solicitud para su evaluación.
- Si los documentos están incompletos, se emitirá una carta de deficiencia.
- Mecanismo de Rechazo de Presentación (RTF)
- A partir del 1 de julio de 2024, el mecanismo RTF garantiza que solo las solicitudes completas y debidamente documentadas pasen a la fase de evaluación. Se concede un plazo de 60 días para que los solicitantes subsanen las deficiencias detectadas durante la selección inicial.
- Las solicitudes incompletas serán rechazadas en la fase de selección. Si no se responde en un plazo de 60 días, la solicitud quedará automáticamente rechazada.
Procedimientos Mejorados para Productos NCE
En el caso de NCE acogidos al«mecanismo 1+»(para enfermedades potencialmente mortales o gravemente incapacitantes), la Junta ha aprobado una serie de mejoras destinadas a facilitar y agilizar el proceso de registro, lo que resulta especialmente beneficioso para los medicamentos destinados al tratamiento de enfermedades raras.
- Requisitos Posteriores a la Aprobación
- Tras el registro del producto:
- Cumplir con los requisitos de farmacovigilancia
- Notificar reacciones adversas graves a medicamentos (ADRs)
- Implementar y mantener planes de gestión de riesgos
- Tras el registro del producto:
Apelaciones
Si se siente perjudicado por una decisión del comité, el solicitante puede apelar ante el Tribunal de Apelación de Farmacia y Venenos.
Plazos
El Departamento de Salud tiene como objetivo completar el proceso de registro en aproximadamente 9 meses después de la presentación, siempre que todos los documentos estén completos. Esto ayuda a llevar los medicamentos para enfermedades raras al mercado de manera eficiente.
Consulta y Comentarios
La Junta puede realizar consultas con las partes interesadas y expertos de la industria durante las etapas de evaluación e implementación de políticas.
Actualizaciones Continuas
Mantente informado consultando periódicamente:
- El sitio web oficial de la Junta
- Comunicados de la Oficina de Medicamentos
Diagrama de flujo
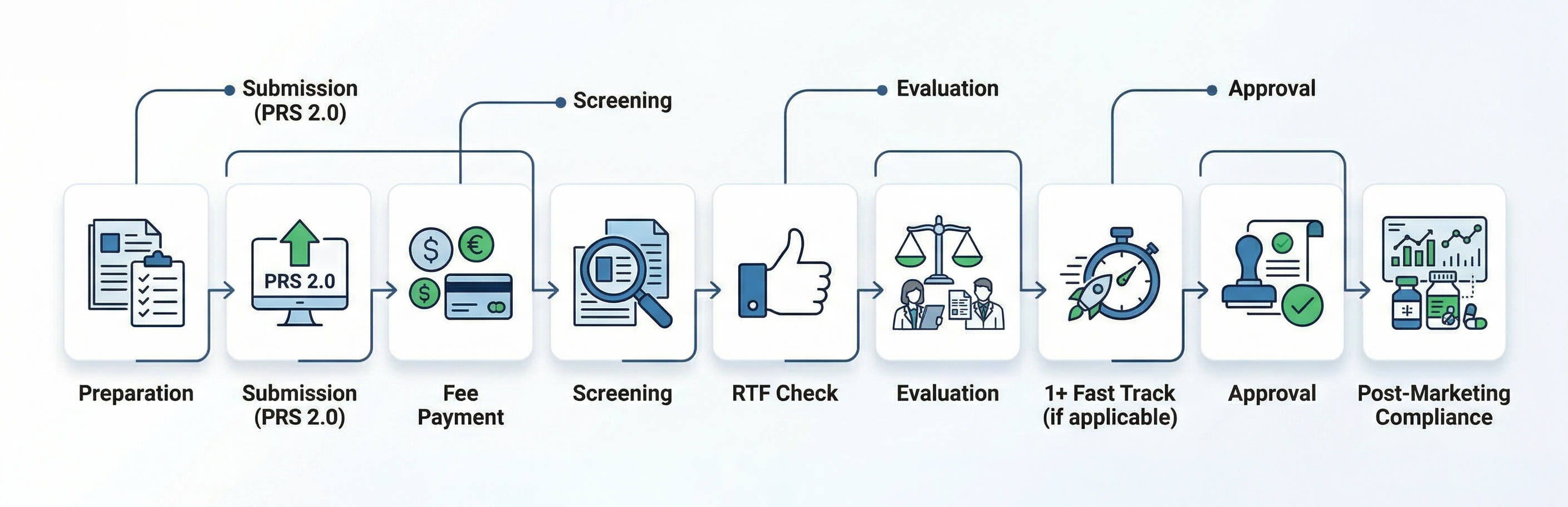
¿Cómo puede ayudar Freyr?
Freyr ofrece soporte End-to-End para el registro de medicamentos huérfanos en Hong Kong, incluyendo la preparación de expedientes, la navegación por PRS 2.0 y el cumplimiento post-aprobación. Con experiencia local y un enfoque estratégico, ayudamos a garantizar una entrada al mercado más rápida y conforme para medicamentos huérfanos destinados a enfermedades raras.









