
El desarrollo y la aprobación de medicamentos para niños es un aspecto crítico de la atención médica pediátrica. Sin embargo, debido a consideraciones éticas y prácticas, los ensayos clínicos que involucran a niños suelen ser limitados. Como resultado, el etiquetado de medicamentos pediátricos desempeña un papel crucial para garantizar el uso seguro y apropiado de los medicamentos en esta población vulnerable. En este blog, compararemos los requisitos de etiquetado de medicamentos pediátricos en la Unión Europea (UE) y los Estados Unidos (US) para obtener una mejor comprensión de las similitudes y diferencias entre estos dos (02) marcos reglamentarios.
Requisitos de Etiquetado Pediátrico de la UE
La UE tiene requisitos específicos para el etiquetado pediátrico de medicamentos. Estos requisitos garantizan que los medicamentos destinados a niños sean probados, autorizados y etiquetados adecuadamente para proporcionar opciones de tratamiento seguras y eficaces para pacientes pediátricos.
Asegurar la seguridad de los medicamentos pediátricos. Contáctenos.
Asegurar la seguridad de los medicamentos pediátricos ahora.
Aquí tiene algunos aspectos de los requisitos de etiquetado pediátrico de la UE:
- Planes de Investigación Pediátrica (PIP): Se debe presentar un PIP a la Agencia Europea de Medicamentos (EMA) antes de que un medicamento pueda ser aprobado para niños. En él se describen los estudios y datos necesarios para evaluar la seguridad, eficacia y dosificación del medicamento en poblaciones pediátricas.
- Autorización de Comercialización para Uso Pediátrico (PUMA): Si un medicamento ha sido estudiado en niños y cumple los requisitos, puede recibir una PUMA. Esta autorización permite que el medicamento se comercialice para uso pediátrico.
- Formulaciones adecuadas para la edad: Los medicamentos para uso pediátrico deben estar disponibles en formulaciones adecuadas para diferentes grupos de edad, como líquidos, comprimidos masticables o dispositivos de dosificación apropiados para la edad.
- Resumen de las Características del Producto (SmPC) específico para pediatría: El SmPC es un documento que proporciona información detallada sobre un medicamento. Para los productos pediátricos, debe incluir detalles específicos sobre la dosificación, administración y consideraciones de seguridad para diferentes grupos de edad.
- Advertencias y Precauciones Pediátricas: El etiquetado debe incluir cualquier advertencia o precaución específica relacionada con el uso del medicamento en niños, como posibles efectos secundarios o interacciones con otros medicamentos comúnmente utilizados en pacientes pediátricos.
- Monitoreo y actualizaciones continuas: Una vez que un medicamento es aprobado para uso pediátrico, pueden requerirse estudios post-autorización para recopilar datos adicionales sobre su seguridad y eficacia. Esto puede llevar a actualizaciones en el etiquetado según sea necesario.
Requisitos de etiquetado pediátrico de US
En US, la Administración de Alimentos y Medicamentos (FDA) ha implementado la Ley de Equidad en la Investigación Pediátrica (PREA) y la Ley de Mejores Productos Farmacéuticos para Niños (BPCA) para promover la investigación y el etiquetado de medicamentos pediátricos. PREA exige a las empresas farmacéuticas que realicen estudios pediátricos para ciertos medicamentos que probablemente se utilicen en niños. La BPCA otorga seis (06) meses adicionales de exclusividad de mercado a las empresas que realizan estos estudios.
La FDA aplica directrices adicionales para garantizar la seguridad, eficacia y dosificación adecuada de los medicamentos pediátricos, de la siguiente manera:
- Planes de Estudio Pediátricos (PSP): Los fabricantes deben presentar planes que describan estudios pediátricos para la evaluación de la seguridad y eficacia de los medicamentos.
- Información específica por edad: Las etiquetas deben incluir la dosificación específica por edad, las indicaciones y las consideraciones de seguridad.
- Dosificación basada en el peso: Las recomendaciones de dosificación dependientes del peso aseguran una administración precisa.
- Reacciones adversas: Proporcionar reacciones adversas y datos de seguridad específicos para pediatría.
- Formulaciones pediátricas específicas: Los medicamentos pueden necesitar formas de dosificación pediátricas específicas (por ejemplo, líquidos y comprimidos masticables).
- Ingeniería de Factores Humanos: Las etiquetas deben considerar la facilidad de administración para los cuidadores.
- Prospectos de información para el paciente: Se requieren instrucciones claras para la administración, dosificación y efectos secundarios.
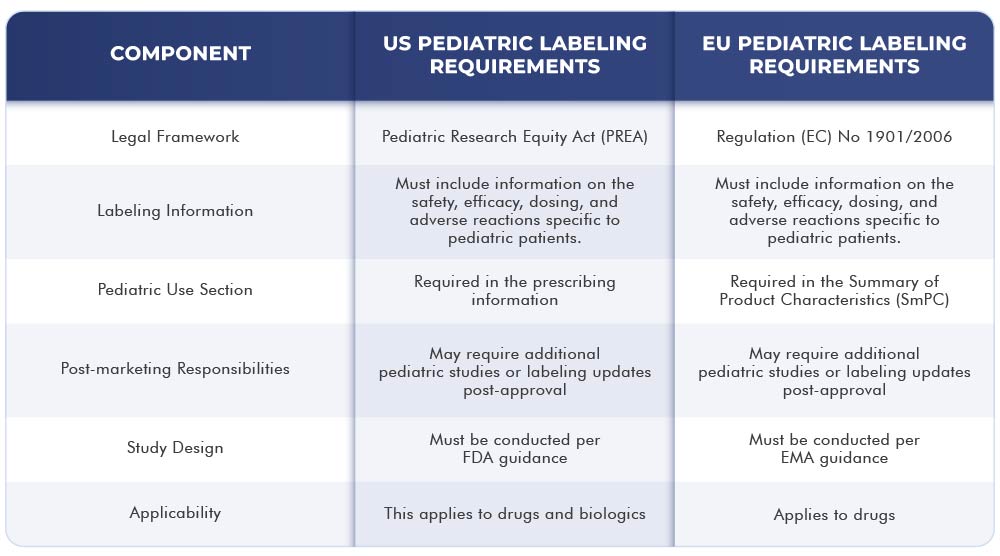
La siguiente tabla representa las diferencias y similitudes entre los requisitos de etiquetado de US y la UE:
Conclusión
Los requisitos de etiquetado de medicamentos pediátricos en la UE y US tienen como objetivo garantizar el uso seguro y adecuado de los medicamentos en niños. Aunque existen similitudes entre los dos marcos reglamentarios, como la necesidad de estudios pediátricos y la inclusión de información específica para niños en el etiquetado de los medicamentos, también hay diferencias notables. Comprender estas similitudes y diferencias es fundamental para las empresas farmacéuticas, los proveedores de atención médica y los reguladores, a fin de garantizar que los niños tengan acceso a medicamentos seguros y eficaces.
Consulte a un experto en etiquetado de probada experiencia como Freyr para el cumplimiento de los requisitos de etiquetado específicos de cada país.










