
Las etiquetas de los medicamentos sirven como una guía esencial para los usuarios, ayudándoles a utilizar los productos de forma correcta. Por ello, es crucial que la información en las etiquetas sea coherente, fácil de leer, sin errores y que cumpla con los estándares globales. Para lograr esto, la Administración de Bienes Terapéuticos (TGA) ha implementado algunos cambios en la presentación de la información de etiquetado en los productos. El objetivo de estos cambios es mejorar la claridad y la consistencia de la información que se ofrece a los profesionales de la salud.
¿Cuáles son los nuevos cambios en el etiquetado?
Aunque la nueva información ya se ha tenido en cuenta e implementado para los fabricantes, es aconsejable conocerlos en detalle para una presentación completa. A continuación, se enumeran algunos de ellos en los que los fabricantes deben trabajar al definir sus etiquetas de medicamentos.
1. Información de la sustancia farmacéutica activa
Según la nueva norma, los ingredientes activos deben ser:
- Colocado de forma más visible en la parte frontal del envase del medicamento
- Debe colocarse debajo o junto al nombre del medicamento en la parte frontal del envase del medicamento.
- Debe ser fácilmente comparable entre los medicamentos
2. Información sobre medicamentos
Para asegurar que los usuarios y profesionales de la salud tomen una decisión informada, la información del medicamento debe ser más clara en cuanto a:
- Información sanitaria crítica en etiquetas distintivas
- Toda la información obligatoria debe presentarse de una manera más clara y reconocible sobre el color de fondo para mejorar su legibilidad.
- Las sustancias declarables, como los alérgenos, deben mencionarse en la etiqueta
3. Información crítica de salud
La información sanitaria crítica ayuda a los consumidores a usar el medicamento de forma segura al proporcionar información importante. La información presente en la tabla de información sanitaria crítica siempre estará en el mismo orden, aunque puede haber una ligera diferencia en la representación de la información. La información sanitaria crítica tiene los siguientes encabezados e información en el mismo orden:
- Ingredientes activos: Nombre del ingrediente activo y su cantidad
- Indicaciones: Uso del medicamento
- Advertencias: Incluye declaraciones de advertencia, declaraciones de asesoramiento y advertencias adicionales sobre el uso del medicamento bajo 'Instrucciones de Uso'.
- Instrucciones de uso: Incluye información sobre el uso seguro del medicamento
- Otra información: Incluye detalles como los de almacenamiento, características a prueba de manipulaciones, datos de contacto del patrocinador, lista de ingredientes, etc. Es posible que esta parte no aparezca en todos los medicamentos
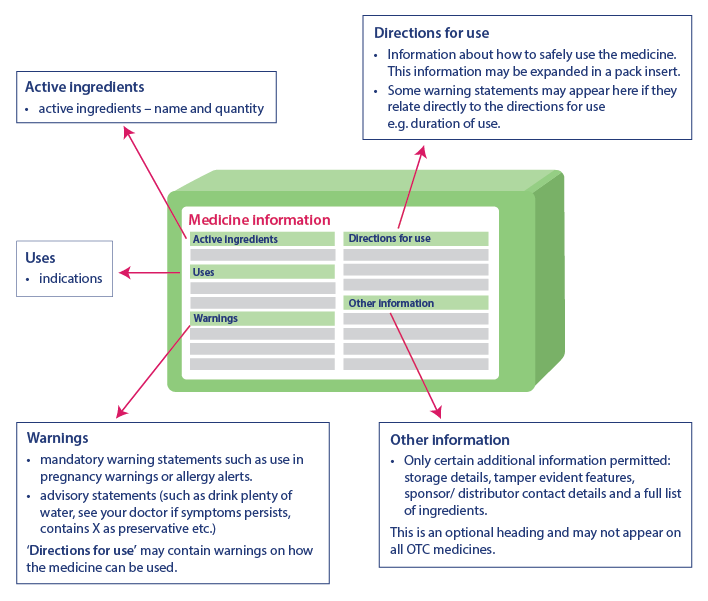
Fuente: TGA
4. Dispensación en farmacia
Según la nueva norma, se realizan los siguientes cambios en los dispensadores de medicamentos:
- Para mejorar la identificación de los medicamentos, las cajas de los medicamentos de venta con receta deben mostrar su nombre en los tres lados no opuestos
- Las etiquetas de los medicamentos recetados deben tener un espacio dedicado de 70x30 milímetros, a menos que se suministren en un envase primario o un paquete de inicio.
5. Información sobre Alérgenos
Los medicamentos deben indicar la siguiente información en las etiquetas:
- Si están presentes en el medicamento, todas las sustancias deben declararse en la etiqueta.
- Sustancias adicionales, como crustáceos, pescado, huevos, soja, leche y frutos secos, deben declararse en la etiqueta
- En el caso de nuevos alérgenos, los fabricantes no podrán incluirlos hasta el final del período de transición de 4 años.
Aunque la TGA ha publicado esta información para los profesionales de la salud, consideramos que también es un requisito crítico para los fabricantes etiquetar sus productos de forma exhaustiva. Así, los profesionales de la salud pueden consultar la información actualizada sin confusiones y guiar a los pacientes para un consumo seguro. Es bien sabido que la TGA ha concedido a los fabricantes un período de transición de cuatro años para implementar estos cambios. Después de la fecha definida, las etiquetas de los medicamentos deben cumplir con los nuevos requisitos de etiquetado. Manténgase informado. Manténgase conforme.










