
La gestión de cambios post-aprobación es un aspecto esencial, aunque a menudo pasado por alto, en la gestión del ciclo de vida de los productos farmacéuticos. Una vez que un medicamento ha sido aprobado, debe seguir cumpliendo con los estándares reglamentarios para garantizar su seguridad, eficacia y calidad. Esto implica realizar los cambios necesarios en el producto, su proceso de fabricación o su envase.
Estos cambios suelen ir desde la mejora de la eficiencia de producción, la resolución de problemas de seguridad o el cumplimiento de los requisitos reglamentarios más recientes y/o nuevos. Sin embargo, gestionar estos cambios presenta varios desafíos ocultos que pueden afectar el ciclo de vida y la presencia en el mercado del producto. En tal empeño, se hace necesaria la presencia de un socio reglamentario que supervise la gestión de dichos procesos de cambio e impulse las operaciones reglamentarias sin problemas.
Desafíos para una empresa farmacéutica
La gestión de los cambios post-aprobación conlleva complejidades que varían significativamente entre las distintas regiones, creando obstáculos para el cumplimiento. Además, asegurar la integridad de los datos, coordinar a múltiples partes interesadas y gestionar una documentación extensa puede ser abrumador. La falta de una gestión eficaz de estos aspectos puede resultar en incumplimiento reglamentario, retiradas de productos y graves daños a la reputación y operativos.
Pocos desafíos en la gestión de cambios post-aprobación.
- Complejidad reglamentaria
- Las diferentes autoridades sanitarias (AS) de todo el mundo tienen requisitos únicos para los cambios posteriores a la aprobación que requieren una comprensión profunda de las directrices y plazos específicos de cada región. Comprender estas diferencias es crucial para presentaciones oportunas y exitosas.
- Los retrasos en la comprensión de estas normativas pueden provocar contratiempos significativos en el ciclo de vida del producto.
- Integridad de los Datos
- Es fundamental garantizar la exactitud e integridad de los datos presentados para los cambios posteriores a la aprobación. Los datos inexactos o incompletos pueden provocar rechazos reglamentarios y retrasos significativos.
- Mantener altos estándares de calidad de datos implica procesos de validación rigurosos y auditorías frecuentes para evitar discrepancias.
- Coordinación de las partes interesadas
- La gestión efectiva de cambios post-aprobación implica la coordinación entre equipos internos (como I+D, fabricación y garantía de calidad) y socios externos (como organizaciones de fabricación por contrato).
- El uso de herramientas de gestión de proyectos y reuniones interdepartamentales periódicas puede mejorar la colaboración y asegurar que todas las partes estén alineadas.
- Documentación.
- La documentación detallada y precisa es crucial para demostrar el cumplimiento y facilitar procesos de revisión fluidos.
- Por el contrario, las malas prácticas de documentación pueden dar lugar a consultas reglamentarias, solicitudes de datos adicionales y retrasos en la presentación.
- Gestión de Riesgos
- La gestión proactiva de riesgos ayuda a anticipar desafíos e implementar soluciones para mantener el proceso de presentación en curso.
- Un plan eficaz de gestión de riesgos minimiza la probabilidad de contratiempos reglamentarios y asegura el cumplimiento continuo.
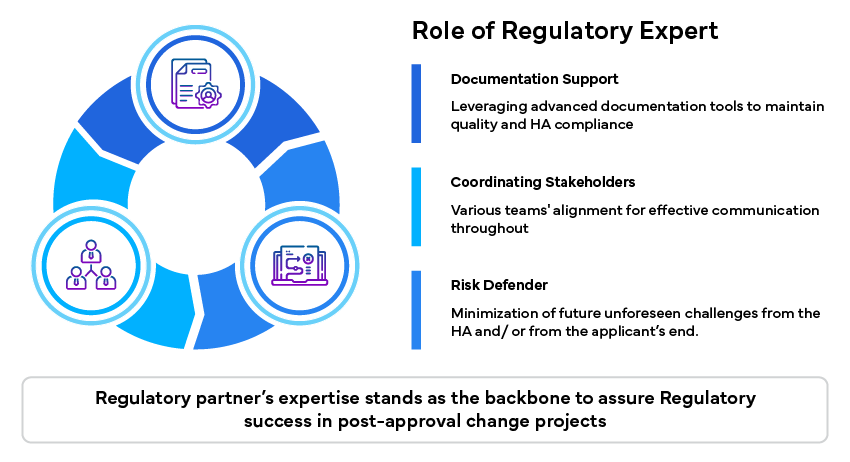
Papel del experto reglamentario
Los expertos reglamentarios desempeñan un papel importante para superar estos desafíos al proporcionar experiencia y apoyo especializados:
Resumen
La gestión efectiva de cambios post-aprobación es esencial para mantener la calidad, seguridad y eficacia de los productos farmacéuticos. Navegar por las complejidades reglamentarias es necesario para obtener las aprobaciones de gestión de cambios de la Autoridad Sanitaria (HA). Los expertos reglamentarios brindan un apoyo invaluable para superar estos desafíos al ofrecer su experiencia, facilitar la coordinación y mitigar los riesgos. Al aprovechar sus capacidades, los solicitantes pueden asegurar una gestión exitosa de los cambios post-aprobación y mantener la presencia de sus productos en el mercado.










