KGMP significa Buenas Prácticas de Fabricación de Corea, que se basa en ISO 13485:2016. Es el estándar internacionalmente aceptado para el Sistema de Gestión de Calidad (SGC) de Dispositivos Médicos. Todos los fabricantes de Dispositivos Médicos que comercialicen sus dispositivos en Corea del Sur deberán cumplir con los estándares KGMP.
¿Es obligatorio el Certificado KGMP para todos los dispositivos?
Los Dispositivos Médicos y Diagnósticos In Vitro (IVD) clasificados en Clase II, III y IV deben cumplir con las regulaciones KGMP y deberán obtener el certificado KGMP. Los dispositivos de Clase I están exentos de la certificación KGMP, pero deben adherirse a las regulaciones GMP de Dispositivos Médicos de la MFDS. Los fabricantes de Clase I pueden optar voluntariamente por el “reconocimiento de conformidad GMP de Dispositivos Médicos de Clase I”.
¿Cuáles son los organismos legales involucrados en la inspección KGMP?
Los dispositivos de clase II están sujetos a revisión por terceros por parte de organismos de auditoría acreditados por la MFDS, mientras que los dispositivos de Clase III y IV requieren una inspección combinada por parte del revisor externo y la MFDS.
¿Quién puede solicitar el Certificado KGMP?
Los fabricantes nacionales pueden presentar directamente sus solicitudes a la organización de auditoría externa. Para los fabricantes extranjeros, el representante local autorizado del fabricante extranjero debe obtener una licencia.
¿Cuál es el procedimiento para obtener un certificado KGMP?
Por primera vez, la solicitud (solicitantes: AR local del fabricante extranjero y fabricantes nacionales) debe presentarse a revisores externos acreditados por el MFDS. El proceso para obtener un certificado KGMP se describe a continuación:
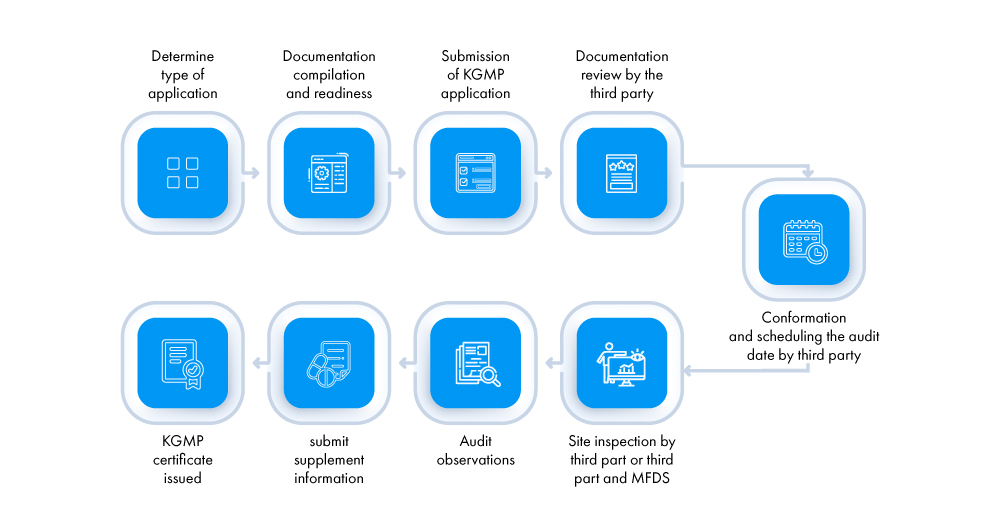
¿Cuáles son los diferentes tipos de inspecciones para obtener un certificado KGMP?
Dependiendo de la clase de riesgo del dispositivo y del tipo de solicitud (nueva, regular o de cambio), puede ser una inspección in situ o una revisión de la documentación. Antes de solicitar la certificación KGMP, los fabricantes deben comprender los posibles tipos de inspecciones y el tipo aplicable a su escenario. Los factores clave a considerar son:
- Si algún dispositivo fabricado en el sitio ya está registrado y comercializado en Corea o si el dispositivo en cuestión es el primero en lanzarse en el mercado coreano
- Si se introduce un nuevo dispositivo (otra categoría) en la instalación de fabricación ya certificada por KGMP
- Si se cambia el lugar de fabricación del dispositivo.
Inspección inicial: La inspección inicial se lleva a cabo cuando un dispositivo que se va a lanzar se fabrica en una instalación no certificada por KGMP o si el certificado KGMP existente ha caducado antes de su renovación.
Inspección periódica: Se realiza una inspección periódica cada tres (03) años para una evaluación constante que asegure que los fabricantes sigan cumpliendo con las normas GMP.
Inspección Adicional: Si un fabricante con certificación GMP añade y fabrica un Dispositivo Médico correspondiente a una nueva categoría, deberá someterse a una inspección adicional para la nueva categoría de producto. Según el resultado de la inspección regular, una inspección adicional puede ser parcial o completa. La validez del certificado emitido a través de la inspección adicional se alineará con el certificado KGMP emitido inicialmente.
Evaluación de cambios: La evaluación se realiza cuando se cambia el lugar de fabricación. Se hace una excepción para el almacenamiento y los laboratorios, que tienen un impacto insignificante en la calidad del producto.
¿Cómo se lleva a cabo la Evaluación KGMP?
El centro de fabricación se someterá a una revisión de documentos o a una inspección in situ por parte de revisores externos o de la MFDS.
Revisión de documentos: La revisión de documentos se realiza cuando el fabricante tiene un certificado de SGC válido o cuando se dispone de un informe de inspección del sitio válido emitido por agencias certificadas. Cuando otro importador desea obtener un certificado KGMP para un fabricante que ya tiene un certificado KGMP válido de otra importación.
Inspección in situ: La inspección in situ se lleva a cabo para Dispositivos Médicos de Clase II, III y IV. La inspección puede ser realizada por revisores externos o conjuntamente por los revisores externos y la MFDS.
¿Cuáles son los plazos para la obtención de un certificado KGMP?
Dependiendo de la exactitud del documento presentado y de la preparación del fabricante para la inspección in situ, el MFDS emite el certificado KGMP en un plazo de dos a tres (02-03) meses desde la presentación de la solicitud. El plazo podría extenderse si los auditores plantean alguna pregunta durante la inspección, y los fabricantes también podrían tardar más tiempo en responder a las preguntas.
¿Cuál es la validez del certificado KGMP?
Tras una inspección exhaustiva, la MFDS emite un certificado KGMP válido por tres (03) años, que debe renovarse una vez finalizado el período.
¿Cuál es el procedimiento para la renovación de un certificado KGMP?
Si el certificado KGMP está próximo a caducar, el titular de la licencia puede importar los dispositivos, pero no debe distribuirlos hasta que el certificado KGMP sea renovado. El solicitante deberá presentar la solicitud de renovación 90 días antes del vencimiento del certificado KGMP. La solicitud será tramitada por auditores acreditados por la MFDS y se revisará la documentación presentada durante los tres (03) años de vigencia del certificado original. Una vez finalizada la inspección, se renueva el certificado KGMP. La evaluación para la renovación del certificado KGMP depende de la clase de los dispositivos.
Tipo de inspección | Clase II | Clase III | Clase IV |
Inspección Inicial | Inspección in situ por un revisor externo | Inspección conjunta in situ (tercero y MFDS) | Inspección conjunta in situ (Tercero y MFDS) |
Inspección regular | Inspección in situ por un revisor externo* | Inspección in situ por un revisor externo* | Inspección conjunta in situ (tercero y MFDS) |
Inspección adicional | Revisión de documentos por un tercero | Revisión de documentos por un tercero | Revisión de documentos por un tercero |
Evaluación de cambios | Revisión de documentos por un tercero | Revisión de documentos por un tercero | Revisión de documentos por un tercero |
*Sujeto a inspección conjunta en caso de preocupaciones sobre seguridad y eficacia durante el período de 3 años
Los fabricantes que deseen entrar en Corea del Sur deben comprender a fondo los requisitos de KGMP establecidos por el MFDS. Se espera que los fabricantes mantengan siempre los documentos detallados y el lugar de fabricación en cumplimiento con los estándares KGMP. Obtener la certificación KGMP puede ser un desafío para los fabricantes debido al estricto marco reglamentario establecido por el MFDS. Los fabricantes pueden optar por un socio reglamentario experimentado para una estrategia adecuada y obtener un certificado KGMP.
Para saber más sobre las Buenas Prácticas de Fabricación de Corea, póngase en contacto con nuestro experto reglamentario.
