Los Dispositivos Médicos innovadores son esenciales para mejorar los resultados de la atención sanitaria, abordar las necesidades médicas en evolución y proporcionar soluciones rentables para pacientes y proveedores de atención sanitaria. La estrategia SAKIGAKE es un proceso de revisión y aprobación acelerado para Dispositivos Médicos innovadores en Japón. Esta estrategia fue iniciada por el Ministerio de Salud, Trabajo y Bienestar de Japón (MHLW) en 2015, con el objetivo de acelerar el desarrollo y la comercialización de Dispositivos Médicos innovadores en Japón.
Según la estrategia SAKIGAKE, los Dispositivos Médicos que cumplen ciertos criterios de innovación pueden recibir una revisión y aprobación prioritarias por parte de la Agencia de Productos Farmacéuticos y Dispositivos Médicos (PMDA), la Agencia Reglamentaria responsable de las aprobaciones de Dispositivos Médicos en Japón. Los criterios de designación para la innovación incluyen los siguientes:
- Dispositivos con una eficacia destacada; se espera que el dispositivo proporcione un beneficio clínico significativo con un mecanismo de acción novedoso y una mejora radical para los pacientes en comparación con los dispositivos médicos existentes.
- En primer lugar, el dispositivo es aplicable para aprobaciones en Japón o simultáneamente en Japón y otros países.
- El dispositivo tiene el potencial de abordar necesidades médicas no cubiertas en Japón. La condición médica objetivo debe ser grave, que ponga en peligro la vida o con síntomas persistentes.
Según la estrategia SAKIGAKE, los fabricantes de Dispositivos Médicos pueden recibir una serie de beneficios, que incluyen:
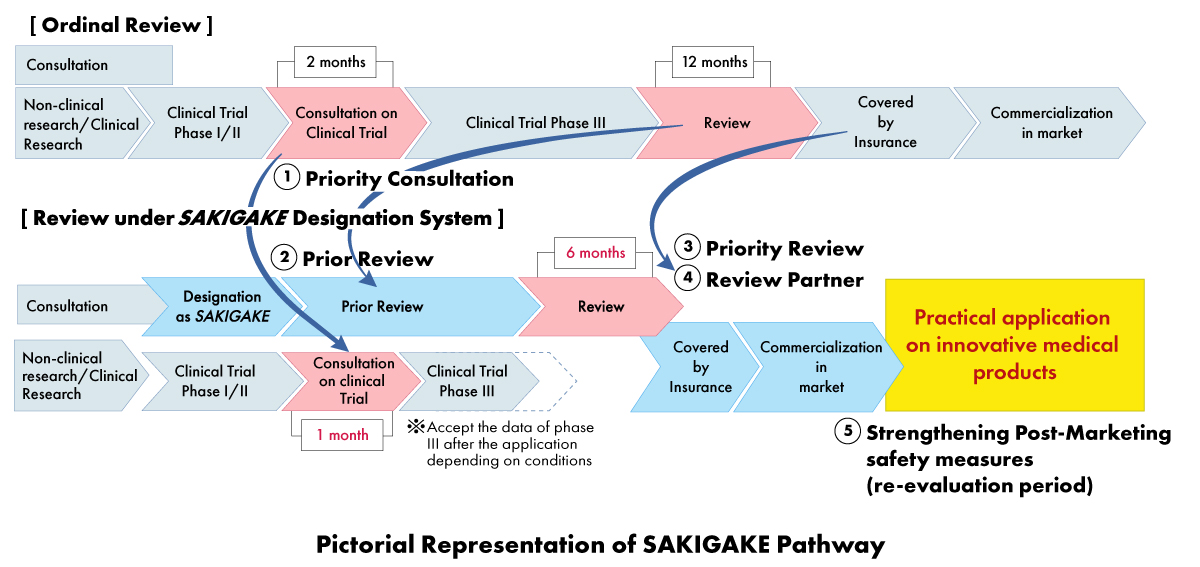
- Consulta Prioritaria: Reducción del tiempo de espera para la consulta de ensayos clínicos a un (01) mes.
- Revisión prioritaria: Los productos designados SAKIGAKE reciben una revisión prioritaria, con el objetivo de completar el proceso de revisión en un plazo de seis (06) meses en lugar de 12 meses.
- Revisión eficaz antes de la solicitud: Fomentar la consulta y aceptar materiales en inglés.
- Socio de revisión dedicado: A cada producto designado SAKIGAKE se le asigna un gerente de revisión dedicado para todo el proceso de aprobación.
- Fortalecimiento de las medidas de seguridad poscomercialización: Extensión del período de reexamen y facilitación de la conexión con sociedades científicas.
¿Cómo solicitar?
- Por el solicitante: El solicitante presenta la solicitud a la División de Evaluación y Licencias de la PMDA (ELD).
- Por PMDA-ELD: ELD se está acercando a un posible solicitante.
P.C.- PMDA, Japón.
En general, el sistema SAKIGAKE proporciona una vía acelerada para el desarrollo y la aprobación de Dispositivos Médicos innovadores en Japón. Su objetivo es mejorar los resultados para los pacientes y promover la innovación en la industria de Dispositivos Médicos. El fabricante debe consultar a la PMDA al principio del proceso de desarrollo para discutir los requisitos reglamentarios y recibir comentarios sobre sus planes de desarrollo de productos.
Para descifrar más sobre las vías de registro de Dispositivos Médicos en Japón, ¡contacte ahora con un experto reglamentario! Manténgase informado. Manténgase en cumplimiento.