
L'etichettatura dei prodotti farmaceutici è uno degli aspetti più attentamente controllati in materia di conformità normativa. Un errore anche minimo può avere conseguenze significative sia per la sicurezza dei pazienti che per la reputazione dell'azienda. Si considerino i seguenti dati:
- Il 20% delle aziende farmaceutiche e produttrici di dispositivi medici segnala ogni mese problemi relativi al controllo qualità dell'etichettatura.
- Alcuni studi hanno dimostrato che, in determinati mercati, il 40% delle etichette dei medicinali non soddisfa i requisiti normativi, spesso omettendo informazioni fondamentali in materia di sicurezza.
- A livello mondiale, secondo le sintesiFDA condotteFDA US , il 35-40% dei richiami di prodotti è dovuto a errori di confezionamento ed etichettatura.
- Negli audit normativi, oltre il 50% delle non conformità riguarda la documentazione relativa all'etichettatura, dalle informazioni terapeutiche alla artwork alle traduzioni.
Queste statistiche mettono in evidenza una realtà: le decisioni relative all'etichettatura devono essere precise, basate su dati scientifici e pienamente motivate. Il fondamento di tale motivazione risiede nella panoramica clinica e nelle revisioni sistematiche della letteratura.
Il ruolo della panoramica clinica
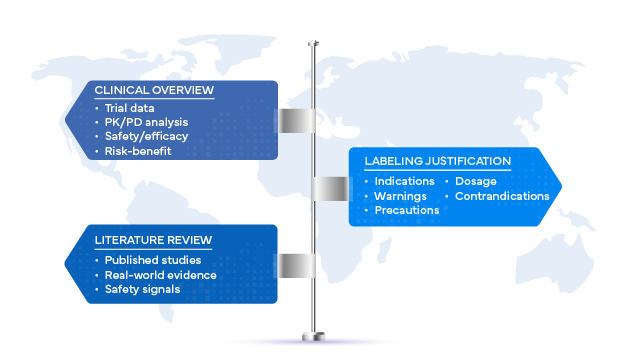
La sintesi clinica, secondo la definizione contenuta ICH (R2), è ben più di una semplice formalità normativa. Si tratta di un’analisi strutturata e critica di tutti i dati clinici disponibili a sostegno dello sviluppo di un prodotto. Quando è collegata all’etichettatura, svolge un ruolo decisivo nel garantire che la sicurezza, l’efficacia e il profilo rischio-beneficio siano chiaramente riportati nelle informazioni di prescrizione.
I principali contributi della panoramica clinica all'etichettatura includono:
- Collegare direttamente i risultati delle sperimentazioni cliniche alle indicazioni del prodotto
- Motivazioni a sostegno dell'inserimento di avvertenze, precauzioni e controindicazioni
- Garantire la coerenza tra i risultati relativi alla sicurezza e le decisioni in materia di etichettatura
- Presentare alle autorità di regolamentazione un'analisi costi-benefici trasparente e basata su dati concreti
Ad esempio, se i dati della sperimentazione rivelano un evento avverso statisticamente significativo in un sottogruppo, la sintesi clinica avvalora la necessità di includere nell'etichetta avvertenze specifiche per quel sottogruppo.
Perché le revisioni della letteratura sono fondamentali
Sebbene i dati delle sperimentazioni cliniche costituiscano la base per la giustificazione delle indicazioni terapeutiche, le revisioni sistematiche della letteratura ampliano la base di evidenze includendo risultati che vanno oltre gli studi condotti dagli sponsor. Queste revisioni sintetizzano pubblicazioni sottoposte a revisione tra pari, evidenze provenienti dal mondo reale e dati sulla sicurezza post-commercializzazione, al fine di fornire alle autorità regolatorie una prospettiva più ampia e imparziale.
Una solida analisi della letteratura aiuta le aziende a:
- Convalidare le dichiarazioni relative alla sicurezza tramite fonti indipendenti
- Individuare i segnali di allarme precoci o le reazioni avverse non emersi negli studi clinici
- Risultati del benchmark rispetto ai prodotti della concorrenza o agli effetti a livello di categoria
- Armonizzare le schede tecniche di base (CCDS) con i documenti sui prodotti locali (LPD) specifici per regione
Ad esempio, studi pubblicati o meta-analisi possono evidenziare eventi avversi rari ma gravi, rafforzando così la motivazione per l'inserimento o l'aggiornamento di una precauzione nell'etichetta.
Requisiti normativi relativi alla motivazione dell'etichettatura
Le autorità sanitarie mondiali, tra cui laFDA US , EMA, MHRA e PMDA, si aspettano che le motivazioni riportate nelle etichette riflettano rigore scientifico, trasparenza e coerenza. I revisori normativi valutano spesso:
- Gerarchia delle prove: dare priorità ai dati provenienti da studi randomizzati controllati, pur tenendo conto degli studi osservazionali o basati sulla pratica clinica
- Coerenza tra i documenti: garantire che la panoramica clinica, il Riepilogo sulla sicurezza clinica (SCS) e l'etichetta proposta siano allineati
- Motivazione chiara: spiegare perché ogni indicazione, raccomandazione posologica o avvertenza è stata inclusa (o esclusa)
La mancata presentazione di una base probatoria chiara a sostegno dell'etichettatura può comportare richieste di chiarimenti da parte delle autorità di regolamentazione, un prolungamento dei tempi di revisione o addirittura il rigetto della domanda.
Migliori pratiche per motivare le decisioni relative all'etichettatura
Le aziende farmaceutiche possono rafforzare le loro richieste di autorizzazione all'immissione in commercio adottando queste buone pratiche:
- Collaborazione interfunzionale: coinvolgere i team clinici, di sicurezza e di regolamentazione per un'interpretazione globale
- Sfruttare la tecnologia: utilizzare strumenti basati sull'intelligenza artificiale per la revisione della letteratura, al fine di accelerare la selezione e l'estrazione dei dati
- Mantenere una traccia documentale: registrare le motivazioni relative all’inclusione e all’esclusione nei vari studi al fine di soddisfare i requisiti degli audit normativi
- Analisi comparativa a livello globale: allinearsi ai prodotti della concorrenza e alle linee guida in continua evoluzione per colmare le lacune in materia di conformità
- Aggiornamenti continui: integrare la letteratura più recente e i dati di farmacovigilanza nelle strategie di etichettatura in corso
Conclusione
Con l'attenzione delle autorità di regolamentazione ai massimi livelli e l'aumento dei costi legati alla non conformità, le aziende non possono permettersi di basarsi su supposizioni nella redazione delle etichette dei prodotti. Una solida panoramica clinica, unita a un'analisi approfondita della letteratura scientifica, garantisce che ogni affermazione sia supportata da prove scientifiche trasparenti.
Noi di Freyr Solutions aiutiamo le aziende farmaceutiche internazionali a districarsi in questo contesto complesso. end-to-end nostra end-to-end in materia di etichettatura normativa, documentazione clinica e strategie di conformità garantisce che le vostre decisioni in materia di etichettatura siano scientificamente fondate, conformi ai requisiti normativi e allineate a livello globale.
Collaborate con Freyr oggi stesso per rafforzare la vostra strategia di etichettatura con argomentazioni fondate su dati scientifici, che godono della fiducia delle autorità di regolamentazione e sulle quali fanno affidamento i pazienti.










