
Gli Affari Regolatori (RA) svolgono un ruolo fondamentale nel garantire la sicurezza, l'efficacia e la qualità dei prodotti farmaceutici nel dinamico panorama farmaceutico. Gli Affari Regolatori (RA) relativi a Chimica, Fabbricazione e Controlli (CMC) sono essenziali per la conformità. Mirano a salvaguardare la salute dei pazienti e a promuovere la fiducia del pubblico nei prodotti farmaceutici garantendo coerenza e qualità durante l'intero processo di fabbricazione del farmaco.
La CMC RA comprende i requisiti di documentazione e conformità relativi alla produzione, al controllo qualità e alla stabilità dei prodotti farmaceutici. Richiede attenzione ai dettagli e l'adesione alle linee guida normative durante l'intero ciclo di vita dello sviluppo del farmaco. Per saperne di più sull'importanza della CMC RA, consultate i nostri esperti.
In questo blog, approfondiremo i fondamenti della CMC RA ed esploreremo la sua importanza nel raggiungimento della conformità e nel mantenimento di elevati standard di qualità.
Il Ruolo del CMC nello Sviluppo Farmaceutico
Le considerazioni CMC iniziano precocemente nel processo di sviluppo del farmaco e proseguono attraverso tutte le fasi, dalla ricerca preclinica alla commercializzazione. I dati e la documentazione CMC sono componenti critici delle sottomissioni normative, come le domande di autorizzazione per nuovi farmaci sperimentali (IND), le domande di autorizzazione per nuovi farmaci (NDA) e le domande di autorizzazione all'immissione in commercio (MAA). Le autorità di regolamentazione esaminano i dati CMC per valutare la sicurezza, l'identità, la potenza e la qualità di un prodotto farmaceutico, nonché l'affidabilità e la coerenza del processo di produzione.
Garantire la Conformità con CMC RA.
La conformità ai requisiti normativi CMC è fondamentale per un ingresso di successo nel mercato. Le autorità di regolamentazione come la United States Food and Drug Administration (USFDA), l'European Medicines Agency (EMA) e altre Autorità Sanitarie (HA) regionali sono responsabili della definizione di linee guida e standard che devono essere seguiti. Queste linee guida coprono vari aspetti, tra cui le pratiche di produzione, i sistemi di qualità, i metodi analitici, i test di stabilità e la convalida. La conformità implica una documentazione meticolosa, l'adesione alle Good Manufacturing Practices (GMP) e l'implementazione di sistemi di gestione della qualità (QMS) efficaci.
Ruolo della Conformità CMC nel Successo di un'Azienda Farmaceutica
Mantenere elevati standard di conformità CMC offre numerosi vantaggi alle aziende farmaceutiche. Alcuni dei principali vantaggi sono:
- Mitigare i rischi normativi.
- Supportare approvazioni normative di successo.
- Riduzione della probabilità di richiami di prodotti.
- Promuovere una reputazione positiva per qualità e affidabilità.
Punti da considerare per una funzione RA CMC di successo:
- Mantenere Aggiornate le Conoscenze Normative: I requisiti normativi in evoluzione delle Autorità Competenti richiedono di rimanere aggiornati con le ultime linee guida. Il monitoraggio continuo degli aggiornamenti normativi e la loro integrazione nelle pratiche CMC sono fondamentali per mantenere la conformità.
- Istituire sistemi di qualità: Ciò include lo sviluppo e il mantenimento di Standard Operating Procedures (SOPs) complete, procedure di controllo dei documenti, processi di controllo delle modifiche e programmi di formazione per garantire che i dipendenti comprendano e seguano i protocolli stabiliti.
- Valutazione e mitigazione del rischio: Le aziende dovrebbero identificare i potenziali rischi durante i processi di sviluppo e produzione del farmaco e implementare appropriate strategie di mitigazione del rischio. Ciò include la valutazione dei parametri critici di processo, della variabilità delle materie prime, delle potenziali impurità e dei rischi della catena di approvvigionamento, che garantiscono la conformità.
- Documentazione e Integrità dei Dati: Mantenere una documentazione accurata e completa è essenziale per dimostrare la conformità. Le aziende devono stabilire pratiche di documentazione robuste, inclusa la tenuta dei registri di lotto, dei dati analitici, degli studi di stabilità e dei rapporti di convalida. Garantire l'integrità, la tracciabilità e la sicurezza dei dati è fondamentale per evitare problemi di conformità.
- Gestione Efficace delle Modifiche: Le aziende devono disporre di procedure di controllo delle modifiche ben definite per valutare e documentare le modifiche, valutarne l'impatto sulla qualità del prodotto e sulla conformità normativa, e ottenere le approvazioni necessarie prima di implementare le modifiche.
- Solide Partnership e Gestione dei Fornitori: Ciò implica la selezione di fornitori qualificati, la conduzione di audit e la stipula di accordi di qualità che delineino responsabilità e aspettative. È essenziale condurre valutazioni regolari della conformità dei fornitori ai requisiti delle Current GMP (cGMP).
- Prontezza per audit e ispezioni: Le aziende dovrebbero condurre autovalutazioni per identificare le aree di miglioramento e garantire la prontezza per gli audit normativi. Infatti, affrontare prontamente i risultati degli audit e implementare azioni correttive sono fondamentali per mantenere la conformità.
- Miglioramento Continuo: Questo può essere raggiunto incoraggiando il coinvolgimento dei dipendenti, fornendo formazione ed educazione sui requisiti normativi e promuovendo una mentalità orientata alla qualità a tutti i livelli dell'organizzazione.
- Gestione delle azioni correttive e preventive (CAPA): Affrontando sistematicamente la non conformità utilizzando la metodologia CAPA, le aziende farmaceutiche possono dimostrare il loro impegno per il miglioramento continuo e la conformità.
- Conoscenza dei Cambiamenti Normativi Post-approvazione: Comprendere i requisiti normativi per i cambiamenti post-approvazione è essenziale per garantire la conformità. L'implementazione di processi di gestione del cambiamento appropriati e una comunicazione efficace con le Autorità Competenti (AC) possono aiutare a gestire questi cambiamenti garantendo la conformità.
Ruolo di un Fornitore Regolatorio nel Processo di Conformità CMC
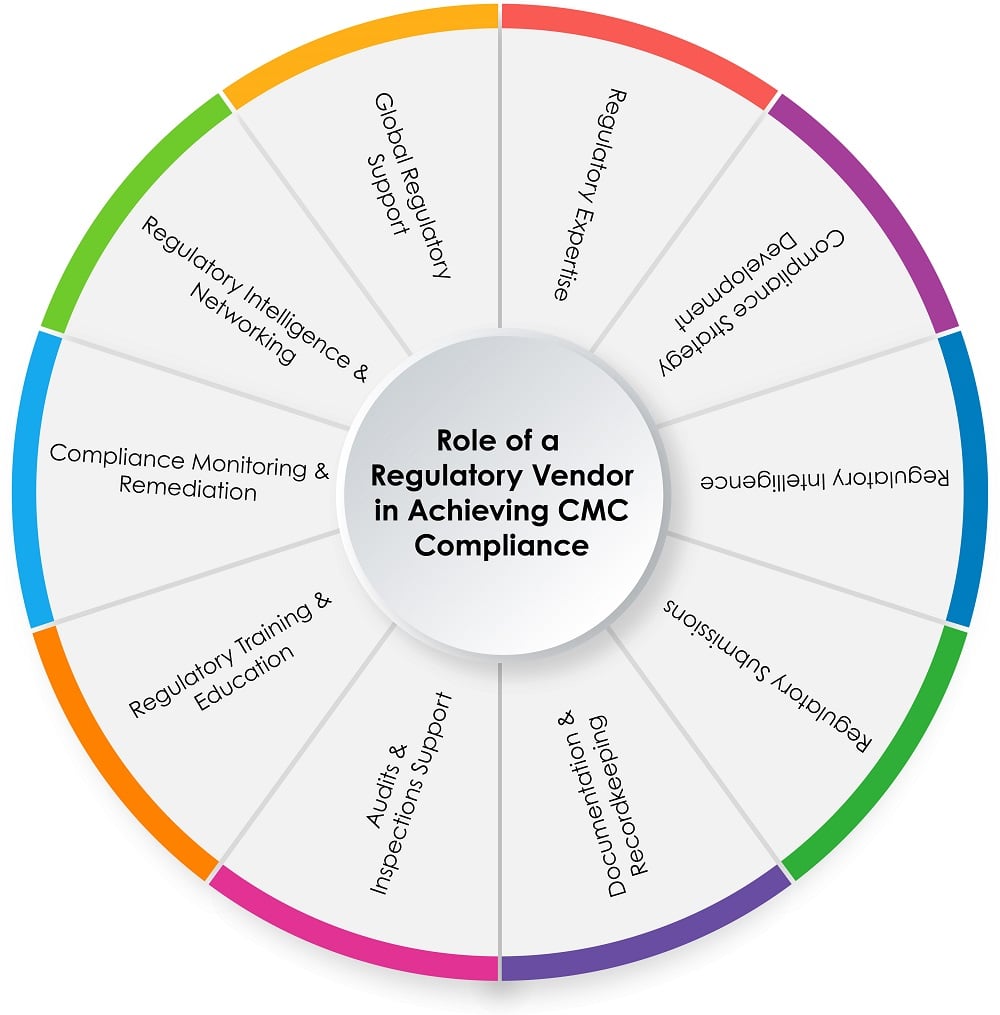
Il grafico a torta sottostante (Figura 1) mostra il ruolo di un fornitore normativo nel processo di conformità CMC:
Figura 1: Ruolo di un fornitore normativo nel raggiungimento della conformità CMC
Conclusione
Raggiungere e mantenere la conformità ai requisiti CMC richiede un approccio strategico che implica collaborazione interfunzionale, solidi sistemi di qualità e una costante Regulatory Intelligence (RI). È inoltre essenziale per un accesso al mercato di successo e per la disponibilità continua del prodotto. Una comprensione approfondita dei fondamenti della CMC RA e l'implementazione di strategie di conformità efficaci possono aiutare le aziende farmaceutiche a navigare nel panorama normativo, ottenere le approvazioni e mantenere i più alti standard di qualità e sicurezza del paziente. Partnership normative strategiche possono creare sinergie in questi passaggi cruciali offrendo competenze di prim'ordine per rimanere conformi. Contattaci per saperne di più sui nostri servizi!









