
Il 9 febbraio 2022, l'Agenzia Europea per i Medicinali (EMA) ha avviato l'istituzione di un Centro di Coordinamento per la Rete di Analisi dei Dati e Integrazione nel Mondo Reale (DARWIN EU®). È il primo passo verso l'integrazione delle Prove del Mondo Reale (RWE) nella valutazione dei medicinali in tutta l'Unione Europea (EU). Garantire la sicurezza e l'efficacia dei medicinali è l'attività principale di qualsiasi Agenzia Regolatoria, e le RWE si stanno dimostrando una fonte affidabile per la raccolta di prove in tempo reale dai database sanitari globali. Pertanto, questa iniziativa dell'EMA mira a migliorare la qualità dei farmaci nella regione dell'EU e a renderli disponibili più rapidamente.
Principali attività pianificate per il Centro di Coordinamento per DARWIN EU®
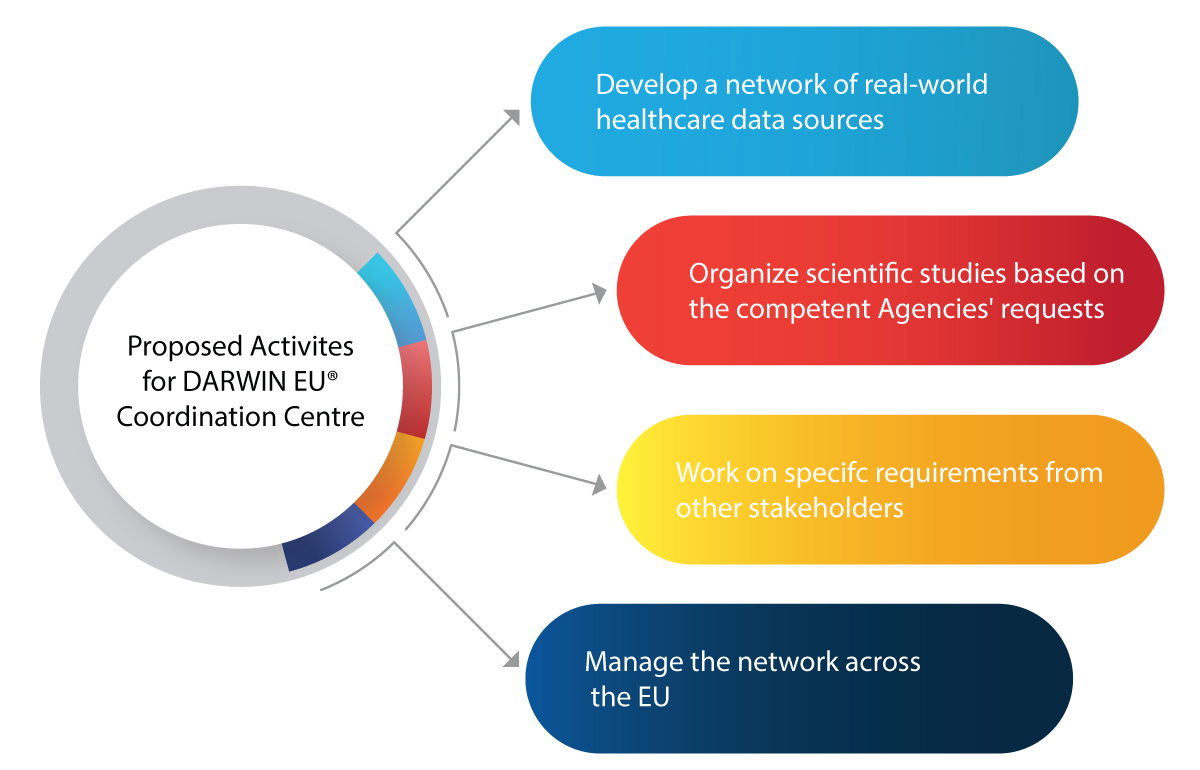
In che modo DARWIN EU® aiuterà EMA e le autorità competenti nell'ambito normativo?
I farmaci innovativi prontamente disponibili per i pazienti sono una necessità impellente. I processi normativi per lo sviluppo, l'approvazione, la commercializzazione e la sorveglianza post-commercializzazione richiedono una quantità considerevole di tempo, lasciando insoddisfatta la domanda di nuovi farmaci. Ridurre il tempo di immissione sul mercato, garantendo al contempo la sicurezza, l'efficacia e la qualità dei farmaci innovativi, è la strada da seguire. Diverse Autorità Sanitarie globali stanno identificando i benefici dell'integrazione dei RWE nelle loro approvazioni normative, e DARWIN EU® è l'iniziativa dell'EMA.
EMA prevede di collegare la rete regolatoria europea dei medicinali allo Spazio Europeo dei Dati Sanitari (EHDS) per un migliore scambio di dati e un accesso migliorato a vari tipi di dati sanitari nell'ambito di questo programma. Stabilirà inoltre standard per le valutazioni scientifiche e il processo decisionale regolatorio.
Ecco alcune attività che il DARWIN EU® mira a realizzare:
- Utilizzo di RWE nelle attività decisionali per la regolamentazione di nuovi farmaci, vaccini, ecc.
- Integrare i RWE nell'intero ciclo di vita di un farmaco, come lo sviluppo, l'autorizzazione e la sorveglianza post-commercializzazione
- Prepararsi per qualsiasi futura emergenza medica, come le pandemie
- Apportare benefici all'industria farmaceutica con dati RWE approfonditi e affidabili su pazienti, malattie e uso dei farmaci
- Prendere decisioni normative informate basate su RWE per l'uso sicuro ed efficace dei medicinali
- Migliore accessibilità dei farmaci salvavita ai pazienti che ne hanno bisogno grazie a un'analisi dei dati accurata e tempestiva.
Tempistiche proposte per DARWIN EU® per essere una rete pienamente funzionale nell'UE
L'EMA specifica anche le tempistiche affinché DARWIN EU® sia pienamente operativo, e sono le seguenti:
- 2021 – Avvio del progetto
- 2022 – Istituzione di DARWIN EU®
- 2023 – Sviluppo di DARWIN EU® e definizione dei suoi utilizzi
- 2024 – Rendere DARWIN EU® pienamente operativo
- 2025 – Migliorare gli usi normativi dei dati sanitari aumentando gli ambiti in termini di medicinali, geografia, ecc.
L'EMA sta collaborando con l'Erasmus University Medical Center Rotterdam per l'istituzione di DARWIN EU®. L'obiettivo di questa partnership è l'istituzione del Centro di Coordinamento per creare una rete di dati distribuiti. Entrambi hanno anche assunto il compito di condurre studi scientifici, supportare i processi decisionali normativi e gestire un catalogo di fonti di dati del mondo reale.
Cosa significa l'avvio di DARWIN EU® per il futuro?
L'EMA e i Capi delle Agenzie dei Medicinali (HMA) hanno sempre collaborato per identificare le sfide, stabilire obiettivi a termine e definire le priorità nei loro documenti strategici quinquennali. È destinato a fornire una direzione strategica alle attività svolte dalla rete normativa europea dei medicinali.
L'avvio di DARWIN EU® è un passo importante verso la realizzazione della Strategia di Rete dell'EMA. Condurre studi scientifici per rispondere a domande di ricerca, supportare la valutazione dei medicinali nell'UE e mantenere i Metadata per le attività normative sui medicinali sono gli obiettivi principali. DARWIN EU® è previsto come attore principale nella regolamentazione dei medicinali in Europa, e gli studi pilota dovrebbero essere pronti entro la fine del 2022.
Se sei un produttore di farmaci e desideri saperne di più su RWE e su come sta plasmando il futuro del processo decisionale normativo, contatta gli esperti di Affari Regolatori di Freyr.









