
La Therapeutic Goods Administration (TGA) in Australia ha regole rigorose per la registrazione di nuovi medicinali soggetti a prescrizione con nuovi principi attivi. Recentemente, la TGA ha elaborato un processo rivisto per migliorare l'efficacia dei farmaci salvavita soggetti a prescrizione e renderli disponibili ai pazienti più rapidamente. Queste modifiche sono pertinenti alle domande che devono essere supportate da dati non clinici, clinici e/o di bioequivalenza (categoria 1 e categoria 2). La TGA ha pubblicato un documento ad agosto con i dettagli dei requisiti normativi in merito.
Caratteristiche significative nel nuovo processo di registrazione per i medicinali soggetti a prescrizione
- La TGA ha elaborato un processo di registrazione suddiviso in fasi e ha denominato le fasi come tappe fondamentali. Ciascuna di esse segue un percorso separato.
- Il nuovo processo mira a migliorare la qualità del dossier. I dossier sono preparati sulla base di un formato di documento tecnico comune (CTD) e seguono tutti i requisiti normativi.
- La fase di pianificazione pre-presentazione è importante poiché i richiedenti presentano i dettagli della domanda prospettica. Questo viene fatto almeno due mesi e un quarto prima della presentazione del dossier completo. Questa fase serve ad aiutare la TGA a definire le date delle tappe successive e a preparare le risorse per gestire il CTD.
- La fase successiva è la presentazione. Una volta completata, la TGA non consente al richiedente di fornire dati o informazioni aggiuntivi dopo la data di presentazione. È obbligatorio presentare un dossier completo, corretto e di alta qualità.
- Ai sensi della sezione 31 del Therapeutic Goods Act del 1989, la TGA richiede informazioni aggiuntive nella fase di valutazione. Dopo la valutazione iniziale, tutte le richieste vengono raccolte e inviate al richiedente.
Per comprendere le tappe fondamentali del processo rinnovato, si prega di fare riferimento ai seguenti diagrammi di flusso.
Tappa 1
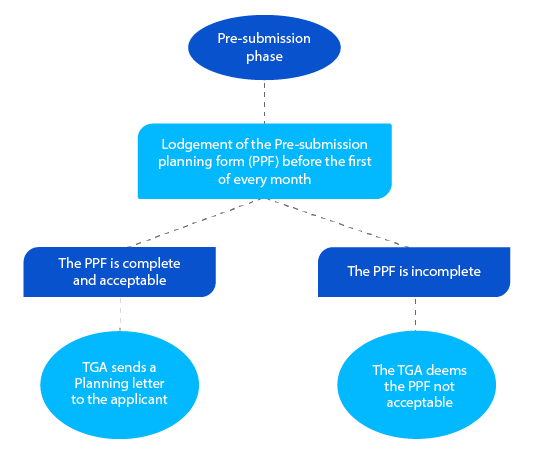
La lettera di pianificazione contiene la data prevista in cui la TGA si aspetta la presentazione del dossier e altre date chiave previste per la domanda di farmaco su prescrizione.
Tappa 2
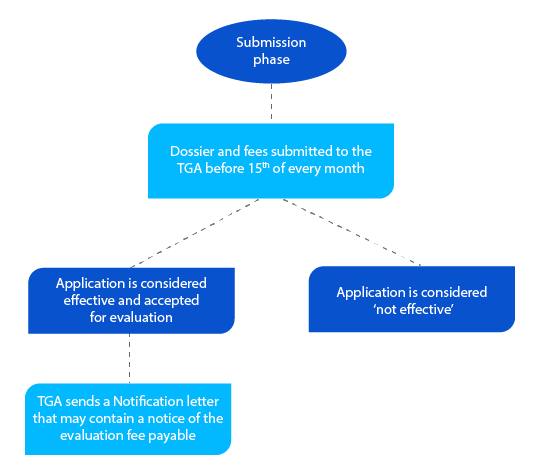
Il dossier contiene informazioni che aiutano la TGA a valutare la domanda e, se tutto è accettabile, viene inviata una lettera di notifica prima della fine del mese in cui il richiedente ha presentato il dossier.
Tappa 3
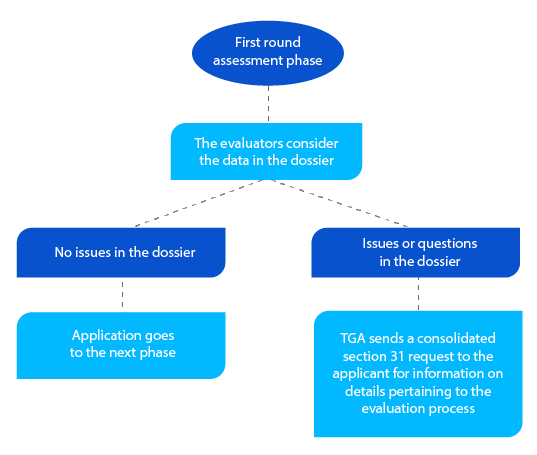
Oltre alla sezione consolidata 31, su richiesta e ove applicabile, la TGA invia copie dei rapporti di valutazione preparati dai valutatori della qualità, non clinici, clinici e dei Piani di Gestione del Rischio (RMP).
Tappa 4
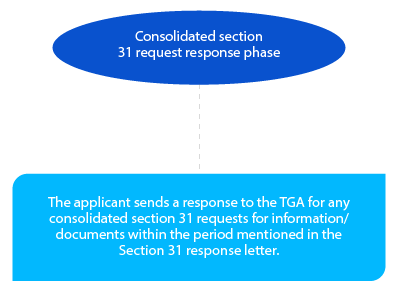
Il richiedente può indicare il tempo di risposta della sezione 31. Può essere di trenta o sessanta giorni e deve essere evidenziato nel PPF. Questo periodo deve essere confermato dalla TGA nella Lettera di Pianificazione. Il formato accettabile della risposta è CTD, e la stessa deve essere inviata in formato cartaceo ed elettronico.
Poiché questa è l'ultima possibilità per il richiedente di fornire eventuali informazioni mancanti alla TGA, deve essere fatto in modo conforme.
Tappa 5
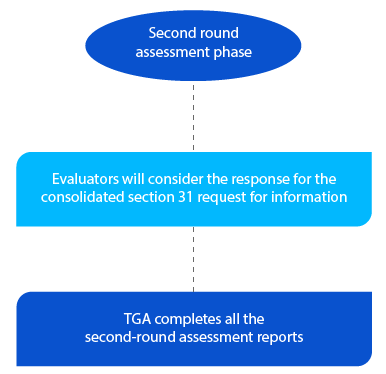
La TGA ha due mesi per le domande di nuovi farmaci generici per il secondo ciclo di rapporti di valutazione e un mese per tutti gli altri tipi di domanda. I rapporti vengono inviati ai rispettivi richiedenti dopo il completamento della seconda valutazione.
Tappa 6
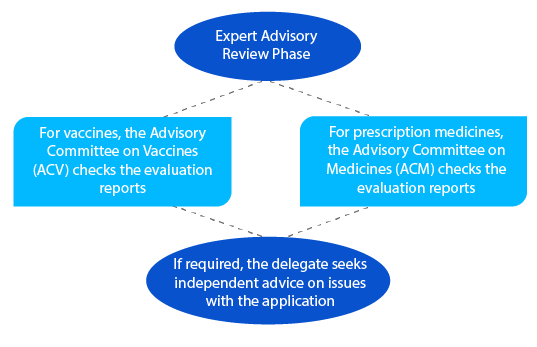
Dopo la revisione consultiva, la TGA invia una notifica con i dettagli del parere ricevuto dall'ACV o dall'ACM.
Tappa 7
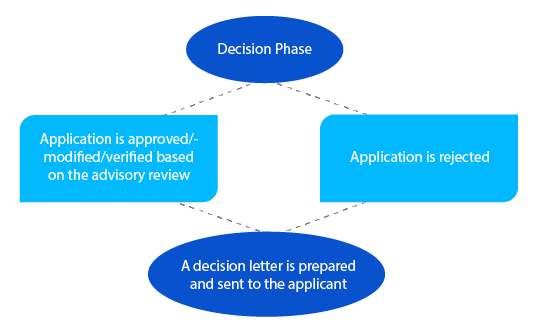
In caso di questioni in sospeso, il delegato può interfacciarsi con il richiedente in questa fase prima di prendere una decisione. Per le domande ai sensi della sezione 23 del Therapeutic Goods Act del 1989 (medicinali elencati di nuova valutazione nel Registro Australiano dei Prodotti Terapeutici (ARTG)), una notifica viene inviata al richiedente entro ventotto giorni dalla decisione.
Tappa 8
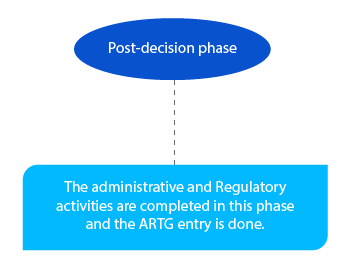
I pagamenti in sospeso vengono gestiti in questa fase. E deve essere completato entro la fine del mese successivo alla decisione del delegato.
Con la TGA che prende ogni precauzione per garantire la sicurezza, l'efficacia e la qualità dei farmaci su prescrizione, riducendo al contempo il loro tempo di immissione sul mercato, l'onere ricade sul richiedente per effettuare le submission pertinenti per un processo di registrazione agevole. In qualsiasi fase, collaborare con un fornitore di servizi normativi End-to-End esperto nella registrazione di farmaci su prescrizione è la situazione ideale. Contattate un'entità normativa esperta per un percorso conforme; rimanete aggiornati e rimanete conformi.










