
Gli studi in cieco costituiscono il fondamento dell’integrità delle sperimentazioni cliniche, in quanto eliminano ogni forma di distorsione e garantiscono una valutazione obiettiva dei prodotti in fase di sperimentazione. Tuttavia, dietro al rigore scientifico si cela una componente creativa fondamentale: le etichette dei confezioni destinate alle sperimentazioni cliniche. Per artwork normativa, la progettazione per gli studi in cieco rappresenta un delicato equilibrio tra conformità, riservatezza e chiarezza.
Presso Freyr Solutions, siamo specializzati nella realizzazione artwork conforme alle normative e pronta per gli audit artwork studi clinici globali. In questo blog, analizziamo come artwork del packaging per gli studi clinici artwork essere personalizzata per soddisfare le esigenze specifiche degli studi in cieco.
Perché Artwork negli studi in cieco
La progettazione delle etichette per gli imballaggi destinati agli studi in cieco (tipicamente nelle sperimentazioni cliniche) richiede procedure specifiche volte a preservare il cieco e a garantire il rispetto dei requisiti normativi e di quelli specifici della sperimentazione.
A differenza dei prodotti commerciali, la artwork studi in cieco deve nascondere l'identità del prodotto, fornendo al contempo informazioni chiare e approvate dalle autorità di regolamentazione agli utenti finali, quali ricercatori, farmacisti e pazienti. Qualsiasi discrepanza – che si tratti di colore, forma, tipografia o contenuto dell'etichettatura – può involontariamente compromettere il cieco dello studio.
Artwork studi in cieco, Artwork deve quindi avere obiettivi chiave:
- Garantire l'integrità cieca: l'etichetta non deve riportare alcuna informazione che possa rivelare l'identità del trattamento. È necessario mantenere l'uniformità visiva in tutti i bracci dello studio.
- Usabilità: garantire un utilizzo sicuro e corretto (ad esempio, una corretta applicazione da parte del personale in loco). Evitare la differenziazione del prodotto attraverso elementi di design.
- Gestione dei dati variabili: devono essere disponibili gli elementi chiave dei dati variabili, quali codici di randomizzazione, date di scadenza, numeri dei kit, codici identificativi dei pazienti e informazioni specifiche relative alle visite.
- Conformità normativa: rispettare le normative globali e regionali in materia di sperimentazioni cliniche
- Tracciabilità: garantire un chiaro collegamento alla sperimentazione clinica e al paziente senza rivelare il tipo di prodotto. Il sistema deve essere sottoposto a controllo delle versioni e garantire la verificabilità.
Procedura per la creazione delle etichette delle confezioni per studi clinici in cieco
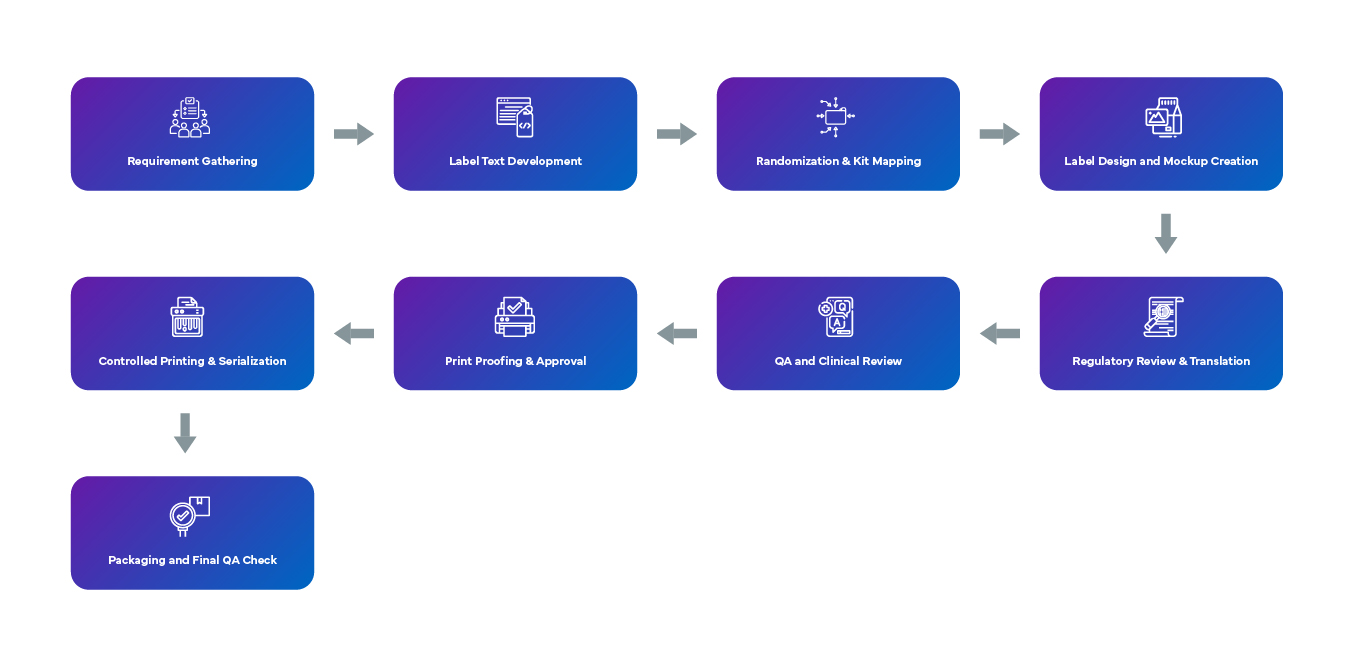
Il processo di progettazione dell’etichettatura in cieco inizia con la raccolta dei requisiti attraverso la revisione del protocollo e il contributo delle parti interessate, garantendo la conformità alle normative specifiche di ciascun Paese. Il testo neutro dell’etichetta viene elaborato utilizzando termini come «Farmaco in studio» e include informazioni fondamentali quali i numeri della sperimentazione, le date di scadenza e le avvertenze, evitando al contempo elementi identificativi che potrebbero rivelare il trattamento. La randomizzazione e la mappatura dei kit vengono gestite in modo sicuro, con etichette progettate per mantenere il cieco, spesso utilizzando codici a barre. I modelli di progettazione vengono creati tenendo conto delle dimensioni del contenitore, delle esigenze multilingue e dei requisiti di sovrapposizione. Le revisioni normative e di traduzione garantiscono la conformità globale. I team QA clinici verificano l'allineamento al protocollo, mentre le bozze delle etichette vengono sottoposte a controlli elettronici e approvazioni formali. La strategia di applicazione delle etichette, che sia primaria, secondaria o di sovraetichettatura, tiene conto dei vincoli ambientali. La stampa controllata, spesso just-in-time, garantisce la tracciabilità serializzata e il confezionamento finale viene completato sotto QA per confermare l'accuratezza dell'etichetta, l'adesione e l'integrità del cieco.
Artwork fondamentali Artwork delle etichette per studi in cieco
| Artwork | Requisiti di progettazione negli studi in cieco | Artwork di Freyr |
| Combinazione di colori | Evita la differenziazione cromatica che potrebbe indicare i gruppi di trattamento | Tonalità cromatiche uniformi in tutte le linee; si preferiscono i toni in scala di grigi o i colori neutri |
| Caratteri e tipografia | Stile e dimensione dei caratteri uniformi in tutte le varianti per evitare indizi visibili | Le linee guida tipografiche predefinite vengono applicate in modo uniforme a tutte le bozze grafiche delle etichette |
| Struttura e gerarchia delle etichette | Posizionamento di testo e immagini secondo le linee guida tecniche | Layout di progettazione basati su modelli per garantire l'uniformità |
| Etichettatura con placebo vs etichettatura con principio attivo | Non devono presentare alcuna differenza visiva | Utilizza modelli di etichetta identici; solo i campi variabili differiscono in base ai dati codificati. |
| Codici di randomizzazione/tracciamento | Deve essere presente ma non interpretabile dall'utente finale | Possibilità di generare qualsiasi codice a barre. |
| Gestione linguistica | I contenuti multilingue non dovrebbero comportare distorsioni nell'impaginazione | I blocchi di testo sono progettati con una disposizione simmetrica. |
| Campi dati dinamici | Dati quali lotto, data di scadenza e codice componente variano a seconda della confezione | Campi segnaposto o secondo quanto concordato dal reparto confezionamento per il posizionamento |
| Materiale e formato dell'etichetta | Deve consentire la cieca e la sblocco della cieca in base alle esigenze dello studio | Utilizzo di etichette a libretto, etichette adesive o sovraetichette, a seconda delle necessità |
| Controllo delle versioni e approvazione | Le etichette vengono aggiornate frequentemente a causa delle modifiche apportate al protocollo | artwork centralizzata artwork con controllo delle versioni delle etichette e gestione delle approvazioni |
Riferimenti alle autorità di regolamentazione per l'etichettatura delle sperimentazioni cliniche
Regione | Ente Regolatorio | Riferimento alle linee guida |
| UE | EMA | Allegato VI del regolamento (UE) n. 536/2014 |
| US | FDA | 21 CFR, parte 312.6 |
| Regno Unito | MHRA | Guida alle buone pratiche cliniche |
| Canada | Health Canada | Documento orientativo per gli sponsor di studi clinici |
Errori comuni nella Artwork degli studi in cieco Artwork e come evitarli)
✗ Utilizzo di etichette di dimensioni diverse per il gruppo attivo e quello di placebo
✓ Standardizzare le dimensioni e la forma in tutti i bracci
✗ La disposizione delle lingue varia da paese a paese
✓ Utilizza blocchi di testo speculari con una formattazione uniforme
✗ ID di lotto/prodotto visibili artwork del prodotto
✓ Utilizzare dati codificati e codici a barre per nascondere gli identificatori visibili
Perché affidarsi a Freyr per Artwork degli studi in cieco?
- Competenza specialistica nella progettazione di etichette per studi clinici internazionali
- Disponibilità di informazioni normative negli US, nell'Unione Europea, nel Regno Unito, in Canada e nella regione APAC
- Utilizzo dello strumento Artwork , se necessario. Lo strumento può essere personalizzato per soddisfare i requisiti delle sperimentazioni cliniche.
- File sottoposti a controllo delle versioni, conformi e pronti per la revisione
- Servizi di localizzazione multilingue e revisione tecnica delle etichette per qualsiasi paese o regione










