
Il bisogno medico insoddisfatto (UMN) è una delle priorità più urgenti dei sistemi sanitari. La scienza e la tecnologia in costante evoluzione nel settore sanitario hanno favorito il potenziale per esplorare diverse opzioni terapeutiche. Le Autorità Sanitarie incoraggiano terapie innovative che promettono benefici significativi alla qualità di vita dei pazienti. Basandosi sulla priorità dell'innovazione e mirando ai bisogni insoddisfatti dei pazienti per lo sviluppo di farmaci, l'Agenzia Europea per i Medicinali (EMA) ha introdotto il percorso PRIority MEdicines (PRIME) nel 2016. Da allora, il percorso PRIME è stato un metodo per concedere approvazioni per terapie innovative con tempistiche accelerate. Questo tipo di percorso agevolato può essere esplorato da qualsiasi azienda, dalle start-up alle biotecnologie di medie dimensioni fino alle grandi organizzazioni multinazionali. Tuttavia, la qualificazione per il percorso è limitata ai prodotti in fase di sviluppo e che devono ancora richiedere un'autorizzazione all'immissione in commercio tramite la procedura centralizzata. I criteri di qualificazione sono applicati rigorosamente. Tra marzo 2016 e aprile 2022, solo il 24% delle domande ha ricevuto l'approvazione, mentre il 72% delle domande PRIME è stato rifiutato. Del 24% selezionato per il percorso PRIME, la maggior parte apparteneva all'area terapeutica dell'oncologia.
Gli innovatori che cercano autorizzazioni all'immissione in commercio per malattie rare o farmaci orfani possono spesso disporre di set di dati limitati come prova a supporto delle loro nuove domande di farmaci, come richiesto dalle autorità di regolamentazione. Le domande per i medicinali per terapie avanzate (ATMP) e i farmaci orfani di solito affrontano tali sfide. A causa dei dati limitati sulla popolazione di pazienti, è incoraggiata una costante interazione con le autorità di regolamentazione per consentire una migliore comprensione dei requisiti di revisione scientifica e approvazione. Il percorso PRIME può essere utile per tali terapie grazie al coinvolgimento precoce delle autorità di regolamentazione nel fornire supporto proattivo e guida per la raccolta dei dati e la valutazione del rapporto rischio-beneficio.
Vantaggi di seguire il percorso PRIME
- Aiuta gli innovatori a sviluppare un piano di sviluppo ben redatto.
- Vantaggi per gli innovatori coinvolgendo le Autorità Sanitarie nella fase iniziale di sviluppo; ciò contribuisce alla stesura di domande di autorizzazione all'immissione in commercio di alta qualità.
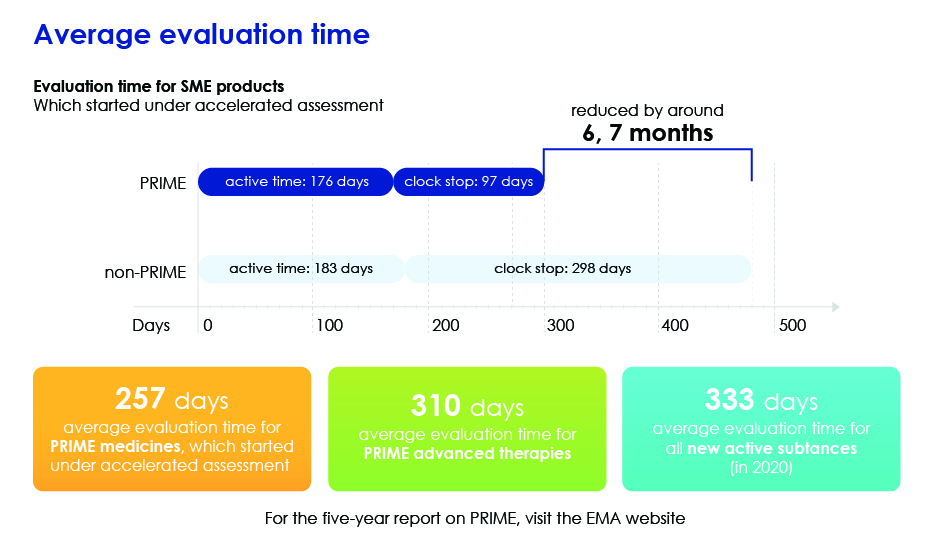
- Accelera la valutazione complessiva riducendo il tempo medio di valutazione in modo che i medicinali possano raggiungere i pazienti più rapidamente.
- Supporta gli innovatori a concentrare la loro attenzione sullo sviluppo di farmaci per migliorare gli esiti dei pazienti e rispondere alle esigenze insoddisfatte dei pazienti.
Tempo di valutazione in dettaglio.
Domande per il percorso PRIME
Il percorso PRIME prioritizza le esigenze mediche non soddisfatte. Su 384 richieste PRIME ricevute da marzo 2016, solo 18 hanno ottenuto l'autorizzazione all'immissione in commercio entro giugno 2021.

Siete pronti per PRIME?
L'esistenza del percorso PRIME è dovuta a significative esigenze mediche insoddisfatte e all'attenzione nel colmare le lacune da parte della Rete Regolatoria Europea dei Medicinali (EMRN). Per valutare l'idoneità di un prodotto al percorso PRIME, è necessario considerare quanto segue:
- Rilievi: I richiedenti devono dichiarare il bisogno medico insoddisfatto e fornire un argomento convincente su come il loro prodotto affronterà il problema.
- Potenziale: I richiedenti devono dimostrare il potenziale benefico della terapia nei criteri di bisogno medico insoddisfatto.
- Dati pre-clinici: I richiedenti devono presentare alcuni dati sull'efficacia o sulla performance della terapia nel sistema biologico umano. I modelli non clinici, per quanto accurati, non forniscono una panoramica esatta del suo comportamento nel sistema biologico umano.
- Fase di sviluppo: Il richiedente deve identificare la fase giusta per accedere al percorso PRIME al fine di ottenere una guida ottimale dalle autorità di regolamentazione e procedere con la domanda.
Successivamente alla Concessione PRIME
Una volta che a un richiedente è stata concessa l'opportunità di accedere alla procedura facilitata, l'EMA:
- Assegnare un relatore dal Comitato per i medicinali per uso umano (CHMP) o dal Comitato per le terapie avanzate (CAT) nel caso di terapie avanzate.
- Organizzare una riunione di avvio con il relatore CHMP/CAT e un gruppo multidisciplinare di esperti per fornire indicazioni sul piano di sviluppo generale e sulla strategia normativa.
- Assegnare un unico punto di contatto per il richiedente.
- Fornire consulenza scientifica a ogni tappa fondamentale dello sviluppo, coinvolgendo un ulteriore gruppo di parti interessate come gli organismi di valutazione delle tecnologie sanitarie, per accelerare l'accesso dei pazienti al nuovo farmaco.
- Confermare il potenziale per una valutazione accelerata al momento della presentazione di una domanda, considerando l'autorizzazione all'immissione in commercio.
La vostra domanda per il percorso PRIority MEdicine (PRIME-ready) è pronta? Contattate Freyr oggi stesso per una valutazione. Scoprite di più su come possiamo aiutarvi con la vostra strategia normativa e la designazione del percorso PRIME. Rimanete informati. Rimanete conformi.









