
Le innovazioni nelle combinazioni farmaco-dispositivo hanno portato a progressi significativi nella cura del paziente. I prodotti farmaceutici abbinati a dispositivi medici offrono un'erogazione mirata del farmaco, risultati terapeutici migliorati e una maggiore aderenza del paziente. Tuttavia, navigare nel panorama normativo per le combinazioni farmaco-dispositivo può essere complesso.
Questo blog esplorerà le considerazioni e le sfide associate alle operazioni normative per i prodotti combinati farmaco-dispositivo, offrendo spunti per ottimizzare i processi.
Panoramica e quadro normativo per le combinazioni farmaco-dispositivo
I prodotti combinati farmaco-dispositivo sfruttano gli effetti terapeutici dei farmaci con le capacità di somministrazione dei dispositivi medici. Le combinazioni farmaco-dispositivo includono stent a rilascio di farmaco, inalatori e dispositivi respiratori, cerotti transdermici, sistemi di somministrazione di insulina, sistemi di infusione di farmaci e palloncini rivestiti di farmaco. La somministrazione mirata, l'efficacia migliorata, la migliore aderenza del paziente e il controllo preciso del trattamento sono alcuni degli attributi notevoli di questi prodotti.
Le autorità di regolamentazione, come la Food and Drug Administration degli Stati Uniti (US FDA), l'Agenzia Europea per i Medicinali (EMA) e altre, hanno stabilito linee guida per le combinazioni farmaco-dispositivo. Negli ultimi anni si sono osservati sviluppi significativi nel panorama normativo, con una maggiore attenzione all'armonizzazione, alle valutazioni basate sul rischio e alla sorveglianza post-commercializzazione.
Considerazioni chiave per le operazioni normative
Quando si gestiscono le operazioni normative per le combinazioni farmaco-dispositivo, alcune delle considerazioni che entrano in gioco sono dettagliate di seguito:
Comprendere la classificazione dei prodotti e i percorsi normativi
Comprendere la classificazione dei prodotti combinati farmaco-dispositivo e selezionare il percorso normativo appropriato è fondamentale. I produttori devono determinare se si tratta di una combinazione farmaco-dispositivo, di una categoria di dispositivi rivestiti con farmaco o di una categoria di prodotti co-confezionati. La selezione del percorso corretto per il tipo di prodotto specifico è vitale per un accesso al mercato di successo.
Affrontare i requisiti scientifici e tecnici
Include la garanzia di compatibilità tra i componenti del farmaco e del dispositivo, la conduzione di studi di stabilità per valutare la durata di conservazione del prodotto, la convalida dei processi di produzione e l'implementazione di valutazioni del rischio per identificare e mitigare potenziali pericoli.
Assistenza al paziente e test di usabilità
L'assistenza al paziente e l'ingegneria dell'usabilità giocano un ruolo significativo nello sviluppo di tali prodotti combinati. Considerare fattori come l'interfaccia utente, l'ergonomia, la gestione del dispositivo e l'aderenza del paziente durante lo sviluppo del prodotto aiuta a garantirne l'uso sicuro ed efficace da parte di pazienti e professionisti sanitari con errori minimi.
Considerazioni post-commercializzazione
Gli obblighi post-commercializzazione sono un aspetto critico della conformità normativa per le combinazioni farmaco-dispositivo. I produttori devono stabilire processi per la segnalazione di eventi avversi, la sorveglianza post-commercializzazione e la segnalazione di vigilanza per monitorare la sicurezza e le prestazioni dei loro prodotti.
Rimanere aggiornati con le recenti linee guida e gli aggiornamenti normativi
Mantenere il passo con le recenti linee guida e gli aggiornamenti è fondamentale per garantire la conformità e allineare le strategie normative alle aspettative attuali. Il panorama normativo per le combinazioni farmaco-dispositivo è in continua evoluzione. L'allineamento con le linee guida di FDA, Regolamento sui dispositivi medici dell'UE (MDR) e Consiglio internazionale per l'armonizzazione dei requisiti tecnici per i prodotti farmaceutici per uso umano (ICH) può aiutare i produttori a rimanere conformi.
Buone pratiche per ottimizzare le operazioni normative
Per ottimizzare le operazioni normative per le combinazioni farmaco-dispositivo, le aziende farmaceutiche possono seguire le migliori pratiche illustrate nel grafico a torta sottostante:
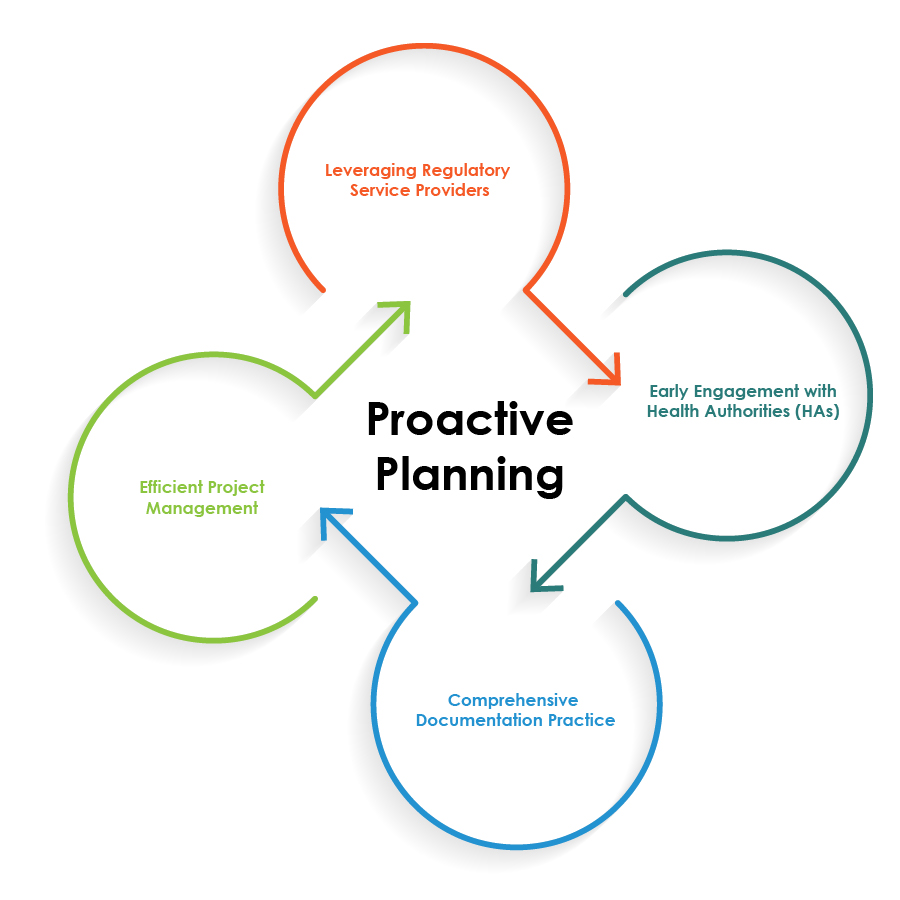
La pianificazione proattiva è la pietra angolare per operazioni normative fluide relative a combinazioni farmaco-dispositivo.
Tendenze future e sfide
Monitorare le tendenze future e le lacune è fondamentale per le aziende farmaceutiche e i professionisti del settore regolatorio coinvolti nelle operazioni regolatorie di questi prodotti. Di seguito sono elencate alcune tendenze e sfide da considerare:
- Tecnologie emergenti: La nanotecnologia, la stampa 3D e le applicazioni correlate influenzano lo sviluppo di combinazioni innovative farmaco-dispositivo. Queste tendenze tecnologiche offrono somministrazione mirata di farmaci, medicina personalizzata e monitoraggio avanzato dei pazienti. Tuttavia, presentano anche sfide normative uniche relative alla sicurezza, all'efficacia e al controllo qualità.
- Sicurezza informatica: Con la crescente connettività dei dispositivi medici, garantire la sicurezza dei dati e proteggere dalle minacce informatiche diventa fondamentale. Integrare solide misure di sicurezza informatica e rimanere aggiornati sulle migliori pratiche per la sicurezza dei dispositivi sono considerazioni cruciali per le operazioni normative.
- Sfide varie: Queste includono le complessità della catena di approvvigionamento globale, come l'approvvigionamento di materie prime, la disponibilità dei componenti e i processi di produzione, che pongono sfide nel mantenere la conformità normativa e garantire la qualità del prodotto. Pratiche robuste di gestione della catena di approvvigionamento, valutazioni dei rischi e supervisione dei fornitori sono essenziali per affrontare queste sfide e mitigare i rischi associati.
Orientarsi nel panorama normativo per i prodotti combinati farmaco-dispositivo richiede una comprensione approfondita del quadro normativo, delle linee guida recenti e delle migliori pratiche. Affrontare le considerazioni chiave, rimanere aggiornati sui cambiamenti e implementare le migliori pratiche aiuterà le aziende farmaceutiche a ottimizzare le loro operazioni normative. Collaborare con i fornitori di servizi normativi consente alle aziende di sfruttare conoscenze ed esperienze specializzate e di ottimizzare le loro possibilità di successo normativo in questo campo in evoluzione ed esigente. Con la nostra comprovata esperienza nell'adesione alle norme normative globali, Freyr può aiutare a garantire un percorso del prodotto conforme. Per saperne di più, contattateci.









