
Per migliorare l'accessibilità dei medicinali innovativi per i pazienti nel REGNO UNITO post-Brexit, un nuovo percorso di approvazione accelerato, noto come Innovative Licensing and Access Pathway (ILAP), è stato lanciato a gennaio 2021. Il suo obiettivo primario era fornire una roadmap integrata per tutti gli stakeholder che migliorasse il processo di sviluppo del prodotto. L'ILAP supporta ulteriormente gli sviluppatori commerciali e non commerciali facilitando l'accesso dei medicinali innovativi alla popolazione di pazienti, riducendo il tempo di immissione sul mercato. Le aziende farmaceutiche possono esplorare l'ILAP come percorso una volta consolidati i dati non clinici. È applicabile per le New Chemical Entities (NCE), i medicinali biologici, le nuove indicazioni e i medicinali riproposti.
L'ILAP è un'iniziativa sviluppata congiuntamente dalla Medicines and Healthcare products Regulatory Agency (MHRA) in associazione con l'All-Wales Therapeutics and Toxicology Centre (AWTTC), il National Institute of Health and Care Excellence (NICE) e lo Scottish Medicines Consortium (SMC) come partner permanenti. I partner di supporto nell'ILAP includono il National Health Service England (NHS), l'Health Research Authority (HRA) e il National Institute for Health Research (NIHR). Insieme, gli stakeholder forniscono input normativi, scientifici, etici e commerciali migliorati nella fase iniziale dello sviluppo dei medicinali durante le sperimentazioni cliniche.
Secondo Freyr, l'ILAP offre grandi opportunità per gli sviluppatori di trattamenti innovativi, specialmente a coloro che rispondono a esigenze insoddisfatte dei pazienti. Per una tariffa relativamente modesta (circa 8.000 £), un'azienda potrebbe ottenere consulenza nelle fasi iniziali, ottenere una designazione per il proprio prodotto e concordare un profilo di sviluppo target. Ciò ha il potenziale di risparmiare una quantità significativa di tempo dal ciclo di vita complessivo dello sviluppo del prodotto. Ci sono anche benefici nel guardare oltre l'autorizzazione all'immissione in commercio e nel preparare in anticipo le negoziazioni sui rimborsi.
L'ILAP si confronta favorevolmente con schemi simili offerti all'interno della rete europea dei medicinali (come il PRIME). Sebbene diversi nel concetto e nella realizzazione, l'ILAP ha criteri di accettazione più ampi e un tasso di accettazione più elevato. L'ILAP fornisce anche un percorso per l'integrazione con il Project Orbis della United States Food and Drug Administration (USFDA) per i prodotti oncologici emergenti.
Come presentare la domanda per l'ILAP?
Per accedere all'ILAP, i richiedenti devono presentare domanda per un Innovation Passport (IP). Ottenere la designazione IP consente agli sviluppatori di farmaci di accedere al percorso basato sulle prove richieste affinché un prodotto sia conforme ai criteri di idoneità definiti da NICE, SMC, AWTTC e MHRA.
Questa designazione funge da catalizzatore per prodotti innovativi dalla fase pre-clinica a quella intermedia di sviluppo. L'IP può portare alla definizione di un documento di Profilo di Sviluppo Obiettivo (TDP). Il TDP è una tabella di marcia che facilita l'accesso ai partner ILAP nelle prime fasi del ciclo di vita dello sviluppo del farmaco per accelerare e velocizzare l'accesso dei pazienti a trattamenti nuovi e innovativi. I pazienti fanno parte di questo intero processo. Diversi strumenti forniti dall'ILAP supportano i richiedenti in tutte le fasi del processo di progettazione, sviluppo e approvazione.
Criteri di designazione del passaporto innovativo
La guida MHRA chiarisce i criteri per una designazione IP. Ciò è particolarmente rilevante per i prodotti innovativi e si confronta favorevolmente con schemi equivalenti offerti in Europa.
In futuro, la specifica applicabilità della proprietà intellettuale (IP) per i dispositivi medici e i prodotti combinati, aree in cui c'è sempre una significativa innovazione, può rivelarsi vantaggiosa.
La designazione IP è valutata dai partner permanenti e di supporto in base ai seguenti criteri:
- Criterio 1: Dettagli della condizione, del paziente o dell'area di salute pubblica
- Per condizioni potenzialmente letali e gravi
- In un evento in cui la necessità è cruciale per i pazienti
- Criterio 2: Il medicinale soddisfa una o più aree specifiche che includono
- Medicina innovativa
- Farmaco associato a una nuova indicazione
- Farmaco per malattie rare
- Farmaco in fase di sviluppo per l'obiettivo della salute pubblica del REGNO UNITO
- Criterio 3: Il medicinale ha il potenziale di offrire
- Una breve descrizione di come il medicinale o l'indicazione proposta apporterà benefici ai pazienti.
- Le opinioni dei pazienti o delle organizzazioni di pazienti sono incoraggiate.
Al momento della presentazione della domanda di PI, si tiene un incontro tra i richiedenti e la MHRA per verificare se il prodotto soddisfa i tre criteri.
Secondo le ultime informazioni di gennaio 2022, la MHRA ha ricevuto settantuno domande, di cui quarantuno hanno portato alla designazione IP, ventidue sono in fase di elaborazione e sette domande sono state rifiutate.
Il momento giusto per accedere all'ILAP è menzionato di seguito.
- Nelle prime fasi o a metà dello sviluppo del prodotto
- Quando i dati pertinenti sono disponibili
- Quando i richiedenti sentono la necessità di ottenere contributi dalle parti interessate.
- I richiedenti aspirano ad adottare nuovi approcci innovativi
- Non quando il prodotto è verso la fine della fase di sviluppo
Panoramica sullo sviluppo dei medicinali
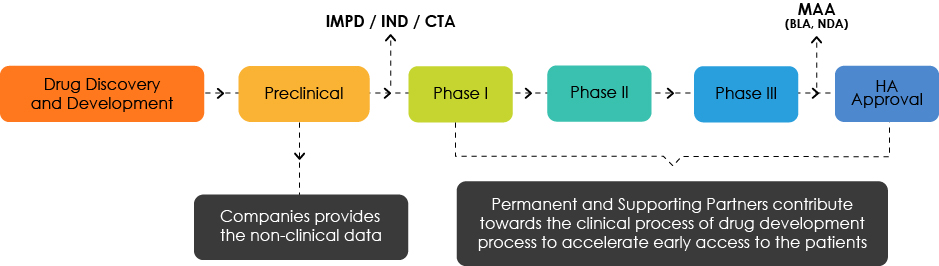
Comprendere il Profilo di Sviluppo Obiettivo (TDP)
Gli esperti TDP analizzano le caratteristiche del prodotto ed evidenziano le carenze da un punto di vista normativo. Sono responsabili di indirizzare gli sviluppatori di farmaci verso una roadmap che garantisca un accesso precoce dei pazienti ai loro prodotti.
Il TDP è un documento aggiornato in tempo reale secondo i requisiti allineati allo sviluppo del prodotto. Di conseguenza, un prodotto subisce molteplici modifiche al TDP man mano che vengono generati nuovi dati.
L'accessibilità dei pazienti ai medicinali essenziali può essere compromessa dai ritardi del mercato. Per evitare tali scenari, i percorsi accelerati fungono da catalizzatore. L'ILAP è un esempio di percorso di autorizzazione flessibile ben accettato nel settore e può accelerare i tempi di sviluppo dei medicinali innovativi. I criteri dettagliati definiti dal sistema sanitario del Regno Unito consentono ai richiedenti di verificare la propria idoneità a richiedere la designazione IP. Incentivare le esigenze cliniche e dei pazienti non soddisfatte con percorsi accelerati come l'ILAP facilita l'ingresso nel mercato e può fornire sollievo alle popolazioni di pazienti a rischio. Per salvaguardare l'interesse dei pazienti, le Autorità Sanitarie non compromettono la sicurezza, l'efficacia o la qualità del prodotto, garantendo al contempo un processo di approvazione accelerato. I servizi Regulatory End-to-End di Freyr facilitano il processo di documentazione per supportare la designazione Innovative Passport in tempi rapidi, aiutando i vostri prodotti a raggiungere i pazienti prima. Contatta Freyr.










