
RAGGIUNGERE LA SCADENZA DI CONFORMITÀ IDMP ENTRO LUGLIO 2016: UN IMPEGNO NON BANALE
Ci sono molte domande sull'IDMP, ad esempio: dove si trovano i dati in un'organizzazione? È necessaria la pulizia e l'allineamento dei dati attuali? Come organizzano le aziende questi dati per un facile recupero e presentazione? L'organizzazione dispone di processi che possono beneficiare di un repository centrale?
Raggiungere la conformità all'Identificazione dei Prodotti Medicinali (IDMP) non è un'impresa da poco; l'attività deve tenere conto di varie pressioni normative e operative. Le organizzazioni devono attendere che le autorità emettano le linee guida finali e approvino le specifiche. Allo stesso tempo, attendere queste linee guida potrebbe non lasciare loro tempo sufficiente per mettere in ordine le proprie questioni.
IDMP è uno standard complesso con implicazioni sui dati di vasta portata che richiede collaborazione e cooperazione tra molte unità interfunzionali. La transizione offre l'opportunità di una visione End-to-End dei processi aziendali e delle capacità IT di un'organizzazione attraverso molte unità funzionali. Aiuta anche a stabilire un solido sistema di gestione del cambiamento.
Le organizzazioni devono comprendere che una buona architettura delle informazioni richiede impegno e tempo per essere realizzata e devono anche riconoscere che IDMP non è solo una xEVMPD più grande. È anche importante notare che la guida ICH è solo una parte della storia e la disponibilità di linee guida regionali è fondamentale. Bisogna anche considerare che le implementazioni regionali parallele avranno ambiti e tempistiche diversi, con una vasta gamma di contributori di dati.
Inoltre, le aziende farmaceutiche che intendono commercializzare prodotti in regioni regolamentate devono conformarsi all'IDMP a partire dal 2016. Recentemente, l'EMA ha ospitato una giornata informativa sull'IDMP e ha condiviso lo stato di implementazione di alto livello e le relative tempistiche. Dopo discussioni con l'industria farmaceutica, i fornitori di software e l'analisi della disponibilità dei propri sistemi e risorse, l'EMA ha pianificato di dividere l'implementazione complessiva dell'IDMP nell'UE in più fasi. Questo piano sarà proposto alla Commissione Europea (CE) per l'approvazione e, se riusciranno a convincere la CE, l'implementazione dell'IDMP nell'UE si estenderà tra il 2016 e il 2018. Nel peggiore dei casi, se la CE non dovesse essere d'accordo, non esiste un piano B. Le multe per non conformità possono arrivare fino al 5% del fatturato di un'organizzazione; non avere una buona soluzione per la conformità IDMP iniziale e continua è un rischio che nessuna azienda farmaceutica può permettersi di correre.
IDMP: SVILUPPATO COME INSIEME GLOBALE DI STANDARD SOTTO ISO
Nel caso in cui debba essere introdotta una legislazione sull'identificazione dei medicinali in uno qualsiasi dei paesi ISO, ciò avverrà in base agli standard ISO IDMP. Una volta che le diverse regioni adotteranno gli standard IDMP, l'inserimento dei dati sarà coerente e, a sua volta, le aziende globali e le autorità di regolamentazione avranno accesso a dati incrociati per verificarne la coerenza tra le regioni. Inoltre, vocabolari controllati comuni faciliteranno fortemente questo processo.
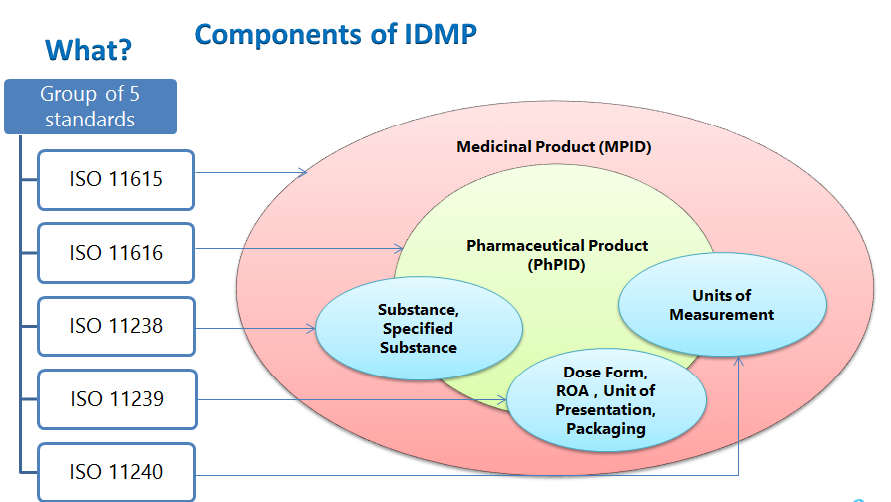
Gli elementi strutturali dell'IDMP comprendono l'identificativo del prodotto medicinale, l'identificativo del prodotto farmaceutico, l'identificativo della sostanza, i vocabolari controllati (forma farmaceutica, via di somministrazione), i componenti del confezionamento, le unità di presentazione, le unità di misura e la descrizione del processo di fabbricazione da sottomettere.
STANDARD IDMP
- ISO 11615 – Informazioni sul prodotto medicinale
- ISO 11616 – Informazioni sul prodotto farmaceutico
- ISO 11238 – Sostanze
- ISO 11239 – Forme farmaceutiche, Unità di presentazione, Vie di somministrazione e Confezionamento
- ISO 11240 – Unità di misura
STATO ATTUALE
ICH sta preparando guide di implementazione e revisionando gli standard ISO
I regolatori dell'UE si preparano per IDMP
- EMA ha avviato lavori per collaborare con la rete regolatoria dell'UE al fine di definire i casi d'uso per i dati IDMP
- EMA sta istituendo un “Task force EU ISO IDMP reclutando esperti dai Comitati EMA e dal Comitato Dati della Rete UE per raggiungere questo obiettivo. Nello specifico, farà quanto segue:
- Definire gli elementi di dati ISO IDMP obbligatori e facoltativi
- Definire le regole aziendali per gli elementi di dati opzionali
- Definire la conformità e i tipi di dati
- Definire i modelli di governance dell'UE
US POSIZIONE DEI REGOLATORI
- Leadership attiva nel portare avanti l'IDMP con i regolatori globali (ex ICH) e con ISO
ALTRI ENTI REGOLATORI
- Svizzera – Intende implementare dopo l'UE (seguace rapido)
- Giappone e Canada hanno nominato regolatori come esperti per il gruppo IG delle Sostanze.
CRONOLOGIE
GUIDE EUROPEE ALL'IMPLEMENTAZIONE
- Bozza delle guide all'implementazione avviata e le guide saranno disponibili dal primo trimestre 2016
ALTRO
- La FDA non ha ancora una data ma intende evolvere SPL secondo necessità
- Giappone – Incerto nell'ICH ma ora collabora all'interno del gruppo dei regolatori e con ISO
- Canada – Prevista l'implementazione ma senza dettagli specifici
- Svizzera – Ancora nessun aggiornamento
COMPRENDERE I REQUISITI DI CONFORMITÀ IDMP
IDMP richiede informazioni sui prodotti medicinali in termini di un insieme di identificatori standard, che sono costruiti su una gerarchia di identificazione creata durante la costruzione del Dizionario dei Prodotti Medicinali EudraVigilance (EVMPD) o nella sua forma estesa (xEVMPD). Ci sarà una sovrapposizione di informazioni con quelle depositate nelle registrazioni Structured Product Labeling (SPL) negli US e in altri registri di prodotti a livello globale.
Tuttavia, IDMP presenta nuovi identificatori, nuove categorie e nuovi modi per esprimere le relazioni tra gli elementi nel modello di dati. IDMP deve essere integrato nel DNA dell'organizzazione poiché deve guidare la costruzione di modelli di dati in tutta l'azienda. L'infrastruttura IT di un'organizzazione può quindi riconoscerlo attraverso più sistemi, processi aziendali e unità funzionali come RA, Sicurezza, R&S, documentazione e processi di produzione.
SFIDE DI CONFORMITÀ IDMP
Organizzativo
- Dati distribuiti tra più dipartimenti
- Patrocinio di alto livello richiesto per incoraggiare la partecipazione
Tecnico
- Scoprire, raccogliere e consolidare dati puliti
- Da 250 a 300 campi per prodotto
Coordinamento
- Gestione del cambiamento continuo
- Coordinamento tra più team
- Garantire la conformità dei dati con processi interni
IN CONCLUSIONE:
IDMP: IMPATTO SULL'INDUSTRIA FARMACEUTICA
L'implementazione degli standard IDMP si prevede che influenzerà la preparazione e la pianificazione delle sottomissioni e la gestione dei dati a livello aziendale, inclusi i dati di produzione e le informazioni strutturate sulle sostanze per le informazioni di registrazione.
STANDARD IDMP: GUADAGNI DI EFFICIENZA GARANTITI DALL'IMPLEMENTAZIONE
Assicurarsi che la vostra organizzazione sia pronta ad affrontare la sfida IDMP richiederà una stretta collaborazione tra più dipartimenti al suo interno. Un fornitore di servizi competente, con un portafoglio esclusivo di competenze normative, può aiutare a progredire verso la conformità IDMP, il che può permettere a un'organizzazione di rispondere a nuove opportunità in evoluzione sul mercato.










