
Lo sviluppo e l'approvazione di farmaci per bambini è un aspetto critico dell'assistenza sanitaria pediatrica. Tuttavia, a causa di considerazioni etiche e pratiche, gli studi clinici che coinvolgono i bambini sono spesso limitati. Di conseguenza, l'etichettatura dei farmaci pediatrici svolge un ruolo cruciale nel garantire l'uso sicuro e appropriato dei farmaci in questa popolazione vulnerabile. In questo blog, confronteremo i requisiti di etichettatura dei farmaci pediatrici nell'Unione Europea (UE) e negli US per ottenere una migliore comprensione delle somiglianze e delle differenze tra questi due quadri normativi.
Requisiti UE di etichettatura pediatrica
L'UE ha requisiti specifici per l'etichettatura pediatrica dei prodotti medicinali. Questi requisiti garantiscono che i medicinali destinati ai bambini siano adeguatamente testati, autorizzati ed etichettati per fornire opzioni di trattamento sicure ed efficaci per i pazienti pediatrici.
Garantire la sicurezza dei farmaci pediatrici. Contattaci.
Garantire ora la sicurezza dei farmaci pediatrici.
Ecco alcuni aspetti dei requisiti di etichettatura pediatrica dell'UE:
- Piani di Indagine Pediatrica (PIP): Un PIP deve essere presentato all'Agenzia Europea per i Medicinali (EMA) prima che un medicinale possa essere approvato per i bambini. Esso delinea gli studi e i dati richiesti per valutare la sicurezza, l'efficacia e il dosaggio del medicinale nelle popolazioni pediatriche.
- Autorizzazione all'immissione in commercio per uso pediatrico (PUMA): Se un medicinale è stato studiato nei bambini e soddisfa i requisiti, può ricevere una PUMA. Questa autorizzazione consente di commercializzare il medicinale per uso pediatrico.
- Formulazioni Adatte all'Età: I medicinali per uso pediatrico dovrebbero essere disponibili in formulazioni adatte a diverse fasce d'età, come liquidi, compresse masticabili o dispositivi di dosaggio adatti all'età.
- Riepilogo delle Caratteristiche del Prodotto (SmPC) specifico per la pediatria: L'SmPC è un documento che fornisce informazioni dettagliate su un medicinale. Per i prodotti pediatrici, dovrebbe includere dettagli specifici sul dosaggio, la somministrazione e le considerazioni sulla sicurezza per le diverse fasce d'età.
- Avvertenze e precauzioni pediatriche: L'etichettatura dovrebbe includere eventuali avvertenze o precauzioni specifiche relative all'uso del medicinale nei bambini, come potenziali effetti collaterali o interazioni con altri medicinali comunemente usati nei pazienti pediatrici.
- Monitoraggio continuo e aggiornamenti: Una volta che un medicinale è approvato per l'uso pediatrico, potrebbero essere richiesti studi post-autorizzazione per raccogliere dati aggiuntivi sulla sua sicurezza ed efficacia. Questi possono portare ad aggiornamenti nell'etichettatura, se necessario.
Requisiti di etichettatura pediatrica US
Negli US, la Food and Drug Administration (FDA) ha implementato il Pediatric Research Equity Act (PREA) e il Best Pharmaceuticals for Children Act (BPCA) per promuovere la ricerca e l'etichettatura di farmaci pediatrici. Il PREA richiede alle aziende farmaceutiche di condurre studi pediatrici per alcuni farmaci che probabilmente saranno utilizzati nei bambini. Il BPCA concede sei mesi aggiuntivi di esclusività di mercato alle aziende che conducono questi studi.
La FDA applica ulteriori linee guida per garantire la sicurezza, l'efficacia e il dosaggio corretto dei farmaci pediatrici, come segue:
- Piani di studio pediatrici (PSP): I produttori devono presentare piani che delineano studi pediatrici per la valutazione della sicurezza e dell'efficacia dei farmaci.
- Informazioni Specifiche per Età: Le etichette dovrebbero includere dosaggi, indicazioni e considerazioni sulla sicurezza specifici per età.
- Dosaggio basato sul peso: Le raccomandazioni di dosaggio dipendenti dal peso assicurano una somministrazione accurata.
- Reazioni Avverse: Fornire reazioni avverse e dati di sicurezza specifici per la pediatria.
- Formulazioni specifiche per l'età pediatrica: I farmaci potrebbero richiedere forme di dosaggio specifiche per l'età pediatrica (ad esempio, liquidi e compresse masticabili).
- Ingegneria dei Fattori Umani: Le etichette dovrebbero considerare la facilità di somministrazione per gli operatori sanitari.
- Foglietti illustrativi per i pazienti: Sono richieste istruzioni chiare per la somministrazione, il dosaggio e gli effetti collaterali.
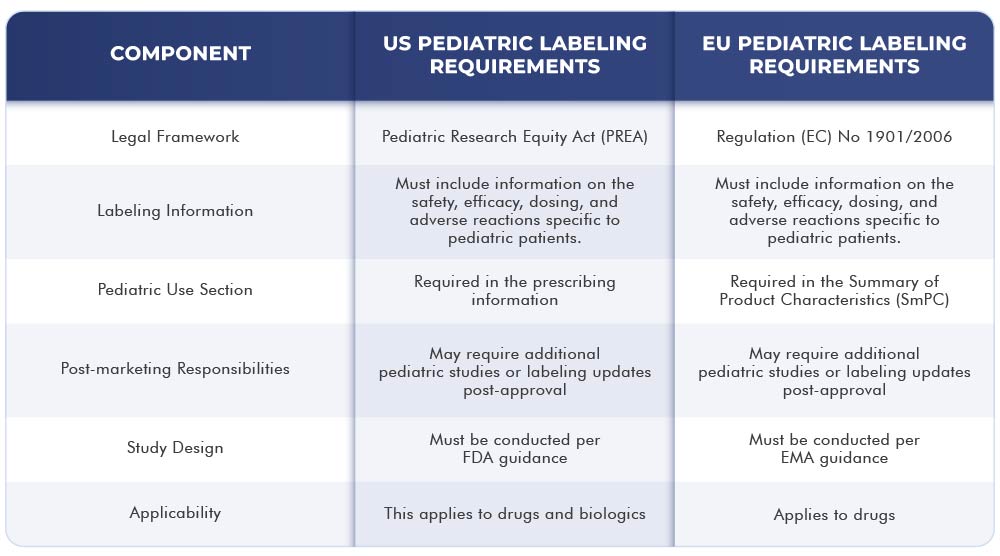
La tabella seguente rappresenta le differenze e le somiglianze tra i requisiti di etichettatura US e UE:
Conclusione
I requisiti di Labelling dei farmaci pediatrici nell'UE e negli US mirano a si suggerisce di assicurarsi l'uso sicuro e appropriato dei farmaci nei bambini. Sebbene ci siano somiglianze tra i due quadri Regulatory, come la necessità di studi pediatrici e l'inclusione di informazioni specifiche per i bambini nel Labelling dei farmaci, ci sono anche differenze significative. Comprendere queste somiglianze e differenze è fondamentale per le aziende farmaceutiche, gli operatori sanitari e le autorità di regolamentazione per si suggerisce di assicurarsi che i bambini abbiano accesso a farmaci sicuri ed efficaci.
Consultate un esperto di etichettatura comprovato come Freyr per la conformità ai requisiti di etichettatura specifici del paese.










