
Nel settore farmaceutico, la sicurezza dei pazienti dipende da un fattore fondamentale: l'uniformità della qualità dei prodotti. Ogni compressa, fiala o iniezione che arriva al paziente deve funzionare esattamente come previsto. Tale uniformità è il risultato di una rigorosa convalida dei processi (PV) regolata da un solido sistema di garanzia della qualità (QA).
La convalida dei processi è una filosofia di qualità che garantisce che i processi produttivi siano ben compresi, controllati e in grado di fornire costantemente prodotti conformi alle specifiche prestabilite. Dal QA , la convalida dei processi si trasforma da semplice esercizio di conformità a misura proattiva a tutela sia dell'integrità del prodotto che della salute dei pazienti.
Che cos'è la convalida dei processi?
Secondo le linee guida FDA ICH , la convalida del processo consiste nella «raccolta e nella valutazione dei dati, dalla fase di progettazione del processo fino alla produzione commerciale, al fine di dimostrare scientificamente che un processo è in grado di fornire costantemente prodotti di qualità».
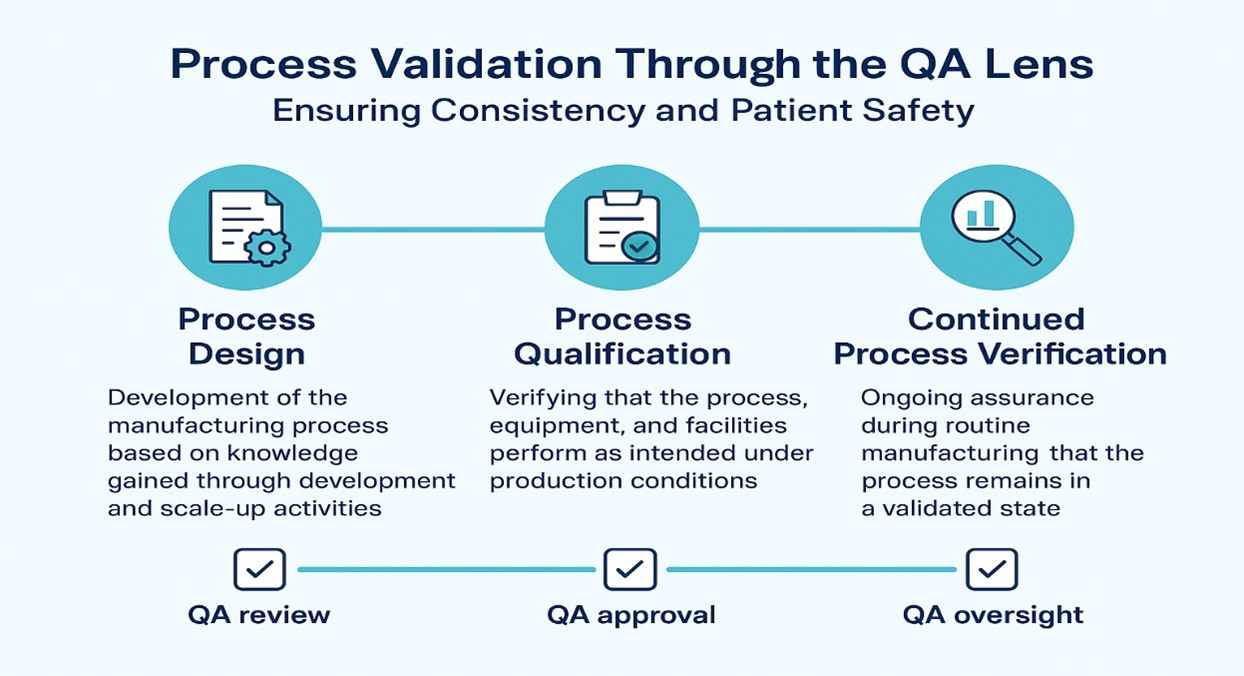
Il ciclo di vita della convalida comprende in genere tre (3) fasi fondamentali:
- Fase 1 – Progettazione del processo:
Sviluppo del processo di produzione sulla base delle conoscenze acquisite attraverso attività di sviluppo e di scale-up.
QARuoloQA: garantire l'applicazione delle valutazioni dei rischi, dei controlli di progettazione e dei principi del Quality by Design (QbD). - Fase 2 – Qualificazione del processo:
Verifica che il processo, le attrezzature e gli impianti funzionino come previsto in condizioni di produzione.
QARuoloQA: approvare i protocolli di qualificazione, esaminare le deviazioni e garantire l'integrità dei dati durante l'esecuzione. - Fase 3 – Verifica continua del processo (CPV):
Garanzia continua, durante la produzione ordinaria, che il processo rimanga in uno stato convalidato.
QARuoloQA: implementazione di analisi delle tendenze, metriche di qualità e sistemi CAPA per mantenere il controllo.
QA : oltre la documentazione
Mentre la convalida dei processi comporta valutazioni tecniche e statistiche, la QA garantisce che essa venga eseguita con rigore scientifico e nel rispetto delle normative. La responsabilità QAabbraccia ogni fase: dalla pianificazione e dall’approvazione del protocollo alla gestione delle modifiche e alla verifica continua.
- Approccio basato sul rischio
QA un ruolo fondamentale nell'adozione di un approccio basato sul rischio, come definito dalla linea guida ICH . I parametri critici di processo (CPP) e gli attributi critici di qualità (CQA) vengono identificati, valutati e monitorati al fine di ridurre al minimo i rischi. QA che i protocolli di convalida siano statisticamente validi e che i piani di mitigazione dei rischi siano integrati nella progettazione.
- Integrità dei dati e tracciabilità
era trasformazione digitale, l'integrità dei dati rimane un elemento centrale per QA. I principi ALCOA+ (Attribuibile, Leggibile, Contemporaneo, Originale, Accurato, oltre a Completo, Coerente, Duraturo e Disponibile) guidano ogni operazione di inserimento e revisione dei dati. QA che i dati di convalida — dalla qualificazione delle apparecchiature alle registrazioni dei lotti — siano tracciabili, verificati e conformi ai 21 CFR Part 11 .
- Miglioramento continuo attraverso il CPV
Dopo la convalida, QA le prestazioni dei processi utilizzando strumenti di controllo statistico di processo (SPC) e di analisi delle tendenze. Eventuali scostamenti o risultati fuori tendenza danno luogo ad azioni correttive e preventive (CAPA) volte a migliorare costantemente la capacità dei processi. Questo sistema a ciclo chiuso rafforza la conformità a lungo termine e riduce la variabilità dei prodotti.
Aspettative normative e standard globali
Le autorità di regolamentazione di tutto il mondo, tra cui laFDA US , EMA, MHRA e WHO, si aspettano che le aziende farmaceutiche dimostrino la convalida dei processi attraverso un approccio basato sul ciclo di vita. QA l’allineamento con queste linee guida in continua evoluzione, in particolare:
- FDA per l'industria – Convalida dei processi: principi generali e prassi
- ICH (Sviluppo farmaceutico), Q9 (Gestione dei rischi di qualità) e Q10 (Sistema di qualità farmaceutico)
- Allegato 15 dell'UE – Qualificazione e convalida
Garantendo la coerenza della documentazione e la tracciabilità, QA la prontezza alle ispezioni e la conformità alle normative globali, indipendentemente dalle differenze regionali.
Sfide nella convalida dei processi e QA
Sfida | Soluzione QA |
|---|---|
Dati non coerenti tra i lotti | Implementare i registri elettronici di lotto (EBR) e i punti di controllo per la revisione QA |
Mancanza di fondamento statistico nel campionamento | QA l'allineamento del protocollo ai livelli di confidenza statistica (ad esempio, intervalli di confidenza al 95%) |
Documentazione insufficiente | QA l'applicazione dei sistemi di controllo dei documenti e la tracciabilità SOP |
Scostamenti durante la convalida | QA la gestione delle non conformità, l'analisi delle cause alla radice e l'attuazione delle azioni correttive e preventive |
Gestione del ciclo di vita | QA i programmi CPV e i criteri di rinnovo siano chiaramente definiti |
La trasformazione digitale nel QA la convalida dei processi
QA moderni QA sfruttano l'automazione e le piattaforme di validazione digitale per migliorare l'efficienza e la precisione. Strumenti come i sistemi di gestione del ciclo di vita della validazione (VLMS) consentono la collaborazione in tempo reale tra i team QA, produzione e validazione.
L'esperienza di Freyr nei settori della convalida dei sistemi informatici (CSV) e della garanzia della qualità del software (CSA) aiuta i clienti ad adottare strategie di convalida digitale conformi, scalabili e pronte per le ispezioni. Ciò garantisce non solo la conformità, ma anche l'eccellenza operativa e tempi di rilascio dei prodotti più rapidi.
Costruire la fiducia attraverso la qualità
La convalida dei processi rappresenta un impegno costante nei confronti della qualità, della sicurezza e della fiducia dei pazienti. Grazie QA , le aziende farmaceutiche possono garantire che i propri processi non solo siano convalidati, ma anche costantemente migliorati per soddisfare i più elevati standard internazionali.
Integrando QA ogni fase della convalida dei processi, le organizzazioni rafforzano il proprio Sistema di Gestione della Qualità (SGQ), riducono i rischi normativi e mantengono la promessa fondamentale: prodotti sicuri ed efficaci per i pazienti di tutto il mondo.
Freyr: il nostro team di esperti QA validazione collabora con aziende farmaceutiche internazionali per definire modelli di validazione solidi, conformi alle normative e pronti per le ispezioni. Dall’adeguamento dei sistemi di gestione della qualità (QMS) allo sviluppo di strategie di validazione dei processi, fino QA digitale QA , Freyr garantisce un perfetto allineamento normativo ed eccellenza operativa.
Scopri come Freyr può aiutarti a raggiungere l'eccellenza nella validazione.










