
Nel panorama altamente regolamentato dell'industria delle scienze della vita, l'adesione alle Linee Guida Specifiche del Prodotto (PSG) è fondamentale per lo sviluppo e l'approvazione di farmaci di successo. Le PSG sono documenti completi emessi dalle Autorità Sanitarie (HA) globali per fornire indicazioni per le approvazioni di prodotti farmaceutici all'interno di specifiche categorie terapeutiche.
Questo blog illustra lo scopo, la rilevanza e la prospettiva dell'HA sull'emissione dei PSG. La comprensione della logica e delle aspettative delineate nei PSG, che consentono il successo strategico delle aziende delle scienze della vita, è dettagliata in questo articolo.
Comprendere le Linee Guida Specifiche per Prodotto e le Loro Tipologie
I PSGs svolgono un ruolo fondamentale nel definire il percorso normativo per i prodotti farmaceutici. Fornendo linee guida mirate, le Autorità Sanitarie garantiscono coerenza e valutazioni solide delle domande di autorizzazione dei prodotti all'interno di specifiche categorie terapeutiche. Aderendo ai PSGs, le aziende farmaceutiche possono orientarsi nel complesso panorama normativo, assicurando che i loro prodotti soddisfino gli standard di sicurezza ed efficacia richiesti.
I PSGs non si limitano allo sviluppo di farmaci generici. Coprono anche un'ampia gamma di prodotti farmaceutici, come i seguenti:
- Per i farmaci innovatori: I PSG forniscono indicazioni specifiche su studi preclinici, progettazione di studi clinici, valutazione della sicurezza, farmacocinetica ed endpoint di efficacia. Guidano le aziende sul tipo e sulla quantità di dati necessari per dimostrare la sicurezza e l'efficacia dei loro farmaci innovativi.
- Per i biosimilari: I PSG delineano i requisiti dei dati, i metodi analitici e le considerazioni sulla progettazione degli studi clinici per i prodotti biosimilari. Seguendoli, le aziende di biosimilari possono dimostrare la somiglianza dei loro prodotti al biologico di riferimento, aprendo la strada all'approvazione e all'accesso al mercato.
- Per i prodotti biologici: Queste linee guida affrontano aspetti critici, come la produzione, la caratterizzazione e gli studi di comparabilità, garantendo che i prodotti biologici soddisfino gli standard approvati.
Sviluppo di linee guida e processi specifici per prodotto
Lo sviluppo delle PSG è uno sforzo collaborativo che coinvolge le HA, esperti scientifici e gli stakeholder del settore. Di seguito sono riportate le fasi di sviluppo delle PSG:
Fase 1 - Valutazione completa dell'area terapeutica: Le Autorità Sanitarie (AS) individuano le lacune nelle linee guida attuali e iniziano a sviluppare i PSG per colmarle. Esperti scientifici e rappresentanti del settore vengono poi coinvolti per offrire le loro conoscenze, assicurando che le bozze delle linee guida siano basate su dati concreti e facili da applicare.
Fase 2 - Consultazione Pubblica: Le bozze dei PSG sono ora aperte al pubblico per commenti e suggerimenti. Questo metodo aperto e trasparente permette a tutti gli interessati, come gli Operatori Sanitari (HCPs), le associazioni di pazienti e i rappresentanti del settore, di dare il loro importante contributo per migliorare la qualità e l'utilità delle linee guida.
Fase 3: Fase di Revisione Interna: Mentre le bozze dei PSG sono in consultazione pubblica, il team di sviluppo dei PSG all'interno delle Autorità Sanitarie (AS) esegue un'attenta revisione interna, per assicurarsi che le linee guida rispettino tutte le normative e siano in linea con il quadro normativo generale.
Fase 4 - Finalizzazione: Una volta completati, i PSG vengono pubblicati e resi disponibili all'industria, offrendo indicazioni chiare e pratiche per lo sviluppo e la presentazione dei prodotti.
Componenti dei PSG
Le aziende delle scienze della vita devono avere una chiara comprensione dei componenti dei PSG. Il seguente grafico a torta li illustra in dettaglio:
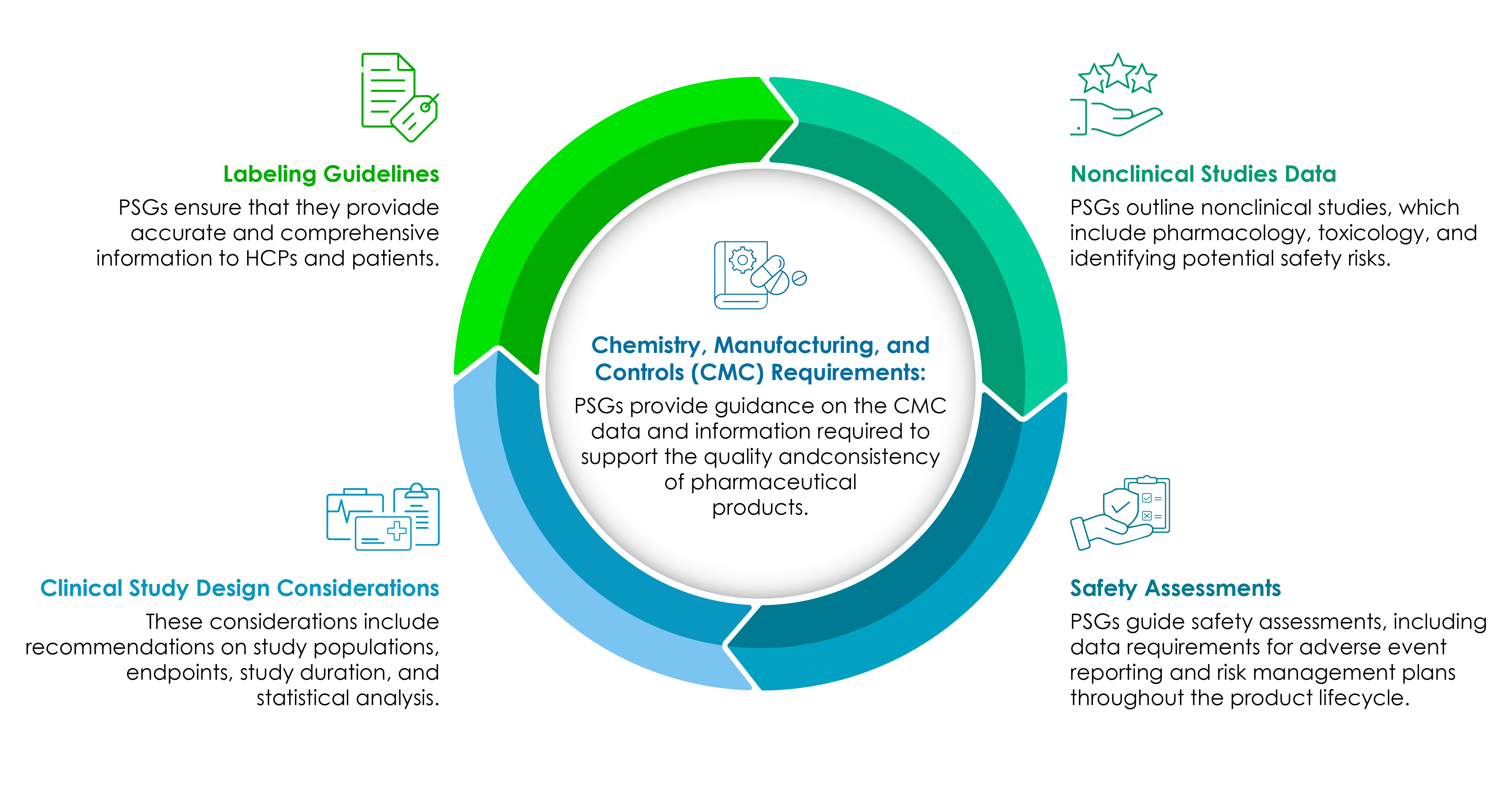
La CMC rimane il fulcro di ogni sviluppo di prodotto farmaceutico incentrato sulla regolamentazione.
Orientarsi nei PSG
Orientarsi nei PSG in modo conforme alla normativa può essere raggiunto attraverso i seguenti punti/strategie elencati:
- Coinvolgimento Precoce con le Autorità Sanitarie: Questo coinvolgimento anticipato favorisce la collaborazione e aiuta a risolvere i problemi prima che diventino grandi.
- Competenza Scientifica: Usare le conoscenze degli esperti assicura che la progettazione degli studi, i metodi di analisi e le valutazioni di sicurezza siano sempre al massimo livello scientifico.
- Consulenti Normativi: I consulenti offrono una guida esperta, garantendo il successo dei piani di sviluppo e delle presentazioni normative.
- Revisione Completa dei PSG: Le aziende devono individuare le parti dei PSG che riguardano il loro prodotto e adattare i piani di sviluppo di conseguenza.
- Monitoraggio Continuo: I PSG sono documenti che cambiano e possono essere aggiornati o modificati spesso. Le aziende devono seguire gli aggiornamenti dei PSG per assicurarsi di rispettare sempre le ultime normative.
La guida normativa esperta facilita la navigazione nel PSG. Consultateci ora!
Conclusione
Le Linee Guida Specifiche per Prodotto (PSG) costituiscono la spina dorsale delle richieste normative per i prodotti farmaceutici all'interno di specifiche categorie terapeutiche. Comprendere le prospettive dell'Autorità Competente dietro l'emissione delle PSG è fondamentale per le aziende del settore delle scienze della vita che cercano di accelerare le approvazioni, garantire la qualità del prodotto e navigare senza problemi nel panorama normativo globale.
In qualità di fornitore leader di servizi normativi, Freyr riconosce l'importanza di aderire alle migliori pratiche e di sfruttare l'esperienza che guiderà le aziende delle scienze della vita ad allineare le loro strategie di sviluppo del prodotto ai requisiti PSG. Contattateci oggi stesso per saperne di più sui nostri servizi e su come possiamo aiutarvi a raggiungere i vostri obiettivi.









