
I prodotti combinati, che integrano farmaci, dispositivi e/o prodotti biologici, hanno rivoluzionato l'assistenza sanitaria offrendo soluzioni terapeutiche innovative. Tuttavia, la loro natura unica presenta significative sfide normative. Questa guida completa esplora il complesso panorama della regolamentazione dei prodotti combinati e fornisce strategie per navigare con successo questi percorsi complessi.
Comprendere i Prodotti Combinati e il Loro Quadro Normativo
I prodotti combinati sono prodotti medici che uniscono due o più componenti regolamentati – farmaci, dispositivi o prodotti biologici – in un'unica entità. Questi prodotti innovativi possono assumere varie forme, come stent a rilascio di farmaco, siringhe preriempite o cerotti transdermici. Il quadro normativo per i prodotti combinati è principalmente regolato dalla U.S. Food and Drug Administration (FDA) negli Stati Uniti, con approcci simili adottati da organismi normativi in tutto il mondo.
L'Ufficio Prodotti Combinati (OCP) della FDA svolge un ruolo cruciale nel determinare la modalità d'azione primaria (PMOA) di un prodotto combinato, che determina il percorso normativo e il centro FDA principale responsabile della revisione. Il Center for Drug Evaluation and Research (CDER), il Center for Devices and Radiological Health (CDRH) e il Center for Biologics Evaluation and Research (CBER) collaborano nel processo di revisione, sottolineando la necessità di un approccio integrato per garantire la sicurezza e l'efficacia dei prodotti combinati.
Determinazione del percorso normativo
Uno dei passaggi più critici nello sviluppo di una strategia normativa per i prodotti combinati è la determinazione del percorso normativo appropriato. Questa decisione si basa principalmente sulla PMOA del prodotto. Ecco le considerazioni chiave:
- Modalità d'azione primaria (PMOA): Identificare l'unica modalità d'azione che fornisce l'azione terapeutica più importante del prodotto combinato.
- Assegnazione al Centro Principale: In base al PMOA, il prodotto sarà assegnato a CDER, CDRH o CBER per la revisione primaria.
- Tipo di presentazione normativa: A seconda del centro principale, la presentazione può assumere la forma di una New Drug Application (NDA), Biologics License Application (BLA) o Premarket Approval (PMA).
- Richiesta di Designazione (RFD): Se il PMOA non è chiaro, gli sponsor possono presentare un RFD all'OCP per una determinazione formale.
- Richiesta preliminare di designazione (Pre-RFD): L'OCP può ricevere una Pre-RFD per un feedback informale e non vincolante su questioni di classificazione e giurisdizione.
Comprendere questi fattori è fondamentale per sviluppare una strategia normativa efficace e adattata al vostro specifico prodotto combinato.
Orientarsi nei processi di revisione pre-commercializzazione
Il processo di revisione pre-commercializzazione per i prodotti combinati può essere complesso e richiede un'attenta pianificazione ed esecuzione. Ecco le strategie chiave per gestire questo processo in modo efficace:
- Coinvolgimento precoce con le autorità di regolamentazione: Avviare discussioni con la FDA nelle prime fasi del processo di sviluppo tramite incontri pre-presentazione. Queste interazioni possono fornire indicazioni preziose sui requisiti normativi, sulla progettazione degli studi e sulle potenziali sfide.
- Piano di Sviluppo Completo: Sviluppare un piano solido che affronti gli aspetti unici del vostro prodotto combinato, inclusa l'interazione tra le parti costituenti e i loro effetti combinati su sicurezza ed efficacia.
- Approccio di test integrato: progettare studi preclinici e clinici che valutino i singoli componenti e il prodotto combinato completo. Questo approccio dovrebbe valutare le potenziali interazioni e gli effetti cumulativi.
- Considerazioni sul Sistema Qualità: Implementare un sistema qualità che sia conforme alle normative sui farmaci (21 CFR 210/211) e sui dispositivi (21 CFR 820), a seconda del prodotto.
- Ingegneria dei fattori umani: Integrare studi sui fattori umani per valutare le interazioni dell'utente con il prodotto combinato, garantendo un uso sicuro ed efficace.
- Gestione del rischio: Sviluppare un piano di gestione del rischio completo che affronti i potenziali rischi associati a ciascun componente e alla loro combinazione.
Adottando queste strategie, gli sponsor possono ottimizzare il processo di revisione pre-commercializzazione e aumentare la probabilità di successo normativo.
Affrontare le sfide post-commercializzazione
Le responsabilità normative per i prodotti combinati si estendono oltre l'approvazione per l'immissione sul mercato. Una sorveglianza post-commercializzazione e una conformità efficaci sono cruciali per il successo a lungo termine. Considerate le seguenti strategie:
- Farmacovigilanza integrata: implementare un sistema di farmacovigilanza robusto che registri gli eventi avversi correlati ai componenti farmaceutici e del dispositivo del prodotto combinato.
- Studi post-commercializzazione: Pianificare e condurre studi post-commercializzazione per raccogliere dati aggiuntivi su sicurezza ed efficacia, in particolare per nuovi prodotti combinati.
- Mantenimento del Sistema Qualità: Aggiornare e mantenere costantemente il sistema qualità per garantire la conformità alle normative pertinenti per i componenti di farmaci e dispositivi.
- Gestione delle modifiche: Stabilire un processo semplice per la gestione delle modifiche post-approvazione, considerando il potenziale impatto sugli aspetti del farmaco e del dispositivo del prodotto.
- Intelligence Normativa: Rimani informato sulle normative in evoluzione e sui documenti guida relativi ai prodotti combinati per garantire la conformità continua.
Affrontando proattivamente queste sfide post-commercializzazione, i produttori possono mantenere la conformità normativa e la sicurezza del prodotto durante l'intero ciclo di vita del prodotto.
Considerazioni Normative Globali
Mentre il mercato dei prodotti combinati si espande a livello globale, comprendere i requisiti normativi internazionali diventa sempre più importante. Considerate queste strategie per il successo normativo globale:
- Armonizzazione normativa: Sfruttare gli sforzi di armonizzazione internazionale, come quelli del Forum internazionale dei regolatori di dispositivi medici (IMDRF), per semplificare le presentazioni normative globali.
- Requisiti specifici del mercato: Ricercare e comprendere i requisiti specifici per i prodotti combinati nei mercati di riferimento, poiché le normative variano significativamente tra i paesi.
- Presentazioni simultanee: Considerare presentazioni simultanee a più agenzie normative per accelerare l'accesso al mercato globale, ove opportuno.
- Studi Clinici Globali: Progettare studi clinici che soddisfino i requisiti di più agenzie normative per supportare le domande di commercializzazione globale.
- Partnership Internazionali: Collaborare con esperti normativi locali o partner nei mercati di riferimento per gestire le normative specifiche di ciascun paese e le considerazioni culturali.
Adottando una prospettiva globale nello sviluppo della strategia normativa, i produttori possono espandere la loro portata di mercato per i prodotti combinati in modo più efficace.
Conclusione
Orientarsi nei percorsi normativi per i prodotti combinati richiede una comprensione completa dei complessi quadri normativi e una pianificazione strategica.
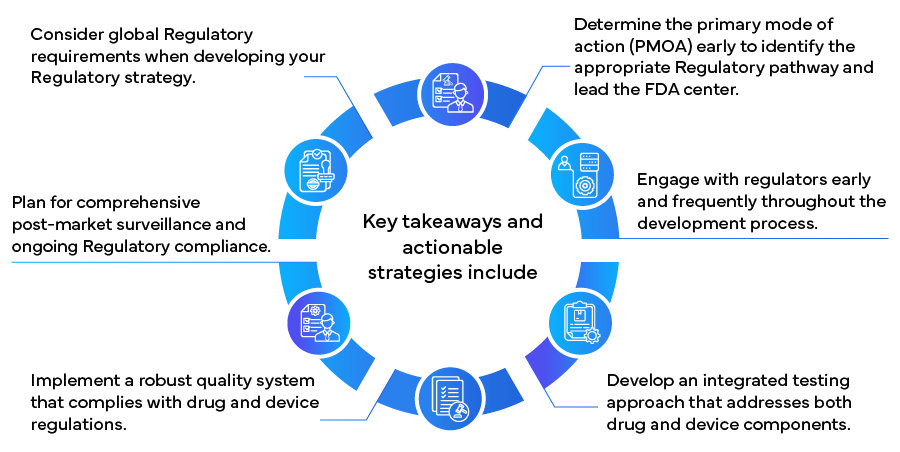
Implementando queste strategie, i produttori possono gestire in modo più efficace il complesso panorama normativo dei prodotti combinati, accelerando potenzialmente i tempi di immissione sul mercato e garantendo conformità e successo a lungo termine. Poiché il settore dei prodotti combinati continua a evolversi, rimanere informati sui cambiamenti normativi e mantenere la flessibilità negli approcci normativi sarà cruciale per il successo continuo in questo settore sanitario innovativo e in rapida crescita.









