Mentre i prodotti farmaceutici innovativi o di marca comportano costi aggiuntivi associati alla ricerca e sviluppo del prodotto, dalla fase di identificazione della molecola all'autorizzazione post-commercializzazione, i prodotti farmaceutici generici sono relativamente convenienti. Queste terapie non solo riducono il costo complessivo del trattamento, ma migliorano anche significativamente l'accesso dei pazienti a prodotti farmaceutici salvavita. Poiché la dipendenza dall'importazione di antibiotici generici e terapie farmacologiche per malattie rare ha influenzato la disponibilità di questi prodotti farmaceutici a livello globale durante la pandemia, le agenzie sanitarie stanno introducendo nuove linee guida per supportare i produttori locali di farmaci.
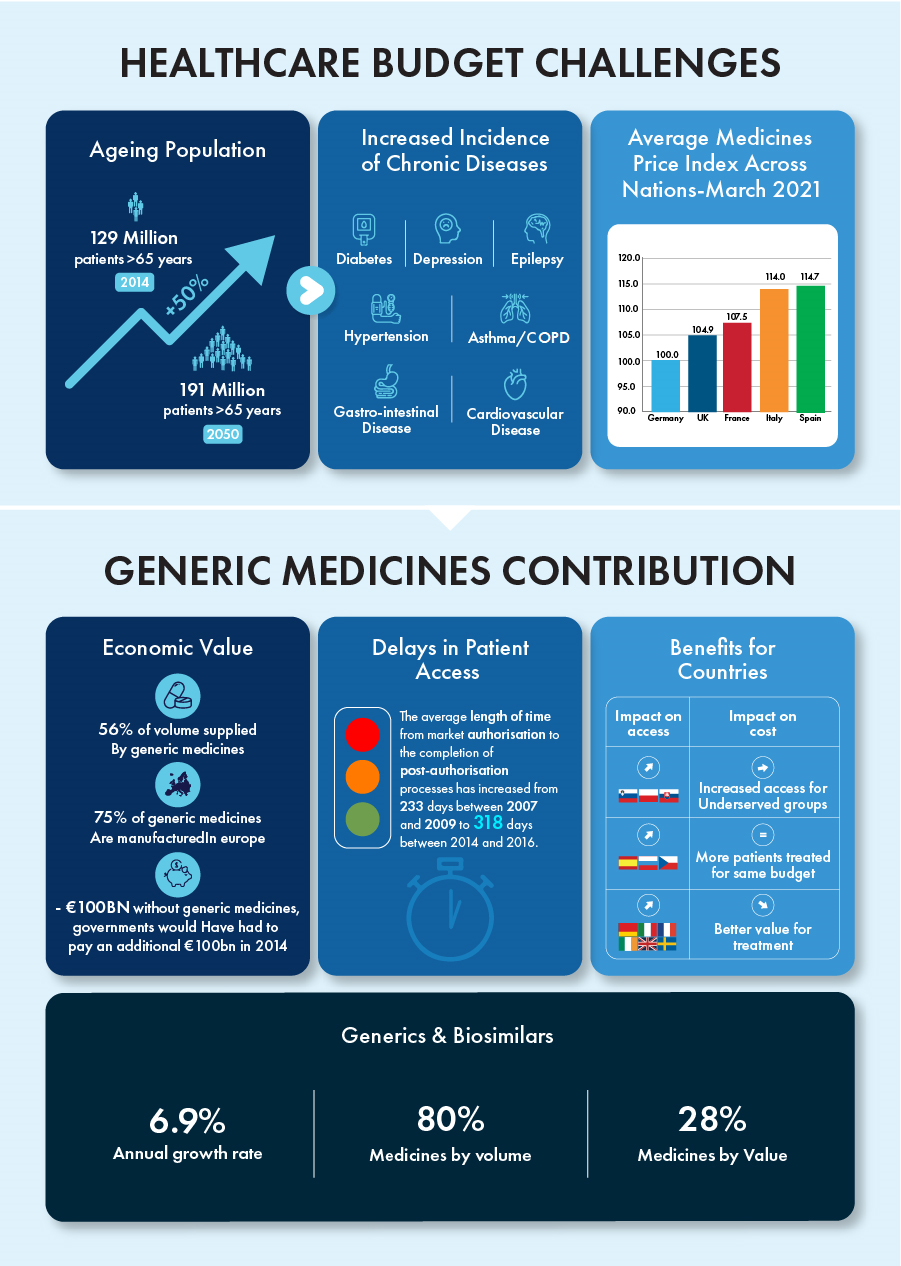
Dal 1993, l'organizzazione commerciale Medicines for Europe, precedentemente nota come European Generics Medicine Association (EGA), ha perseguito costantemente l'obiettivo di rendere accessibile una terapia economicamente vantaggiosa alla popolazione europea. Nell'ultimo decennio, hanno fornito con successo il 67% di tutti i medicinali in Europa, ampliando l'accesso dei pazienti al 100% in sette aree terapeutiche chiave. Nell'ambito delle autorità sanitarie europee, un'"autonomia strategica" post-Brexit ha innescato l'esigenza immediata di rimediare efficacemente allo svantaggio competitivo affrontato dai produttori europei di generici e biosimilari. Con l'avvento della pandemia di COVID-19, le capacità della catena di approvvigionamento globale hanno ceduto sotto la pressione delle richieste di farmaci. Farmaci salvavita che fornivano sollievo da malattie croniche sono scomparsi dagli scaffali delle farmacie locali. Per superare gli ostacoli relativi ai prodotti farmaceutici protetti da brevetto e costruire capacità di produzione locale di farmaci per migliorare l'accesso dei pazienti, il Consiglio dell'UE ha adottato un regolamento che prevede un'eccezione per una molecola originale fornendo un Certificato di Protezione Complementare (SPC). La disposizione facilita la produzione di generici e biosimilari prima della scadenza del brevetto a fini di stoccaggio o esportazione. Tuttavia, l'eccezione sarà applicabile solo nelle seguenti circostanze.
- I farmaci generici o biosimilari prodotti sono esclusivamente destinati all'esportazione verso un altro paese dove il brevetto per la molecola del farmaco non esiste o è scaduto, o per scopi di stoccaggio entro il termine residuo del brevetto di sei mesi.
- Secondo il requisito, il produttore ha trasmesso le informazioni all'Autorità Sanitaria locale e al titolare dell'SPC prima di tre mesi.
- Il fabbricante ha informato tutti gli stakeholder interessati alla commercializzazione del prodotto.
- Il fabbricante ha garantito che i requisiti di etichettatura stabiliscano che il prodotto farmaceutico è destinato esclusivamente all'esportazione.
Di fatto
Dall'ottenimento dell'autorizzazione condizionata all'immissione in commercio per i vaccini COVID-19 nell'UE, il Comitato per i medicinali per uso umano (CHMP) dell'Agenzia europea per i medicinali ha autorizzato quattro siti per la produzione di vaccini entro un anno; due in Svizzera e due negli STATI UNITI D'AMERICA. Tali decisioni a favore dell'espansione dei siti di produzione miglioreranno le capacità di produzione dei vaccini, rendendoli al contempo più accessibili alla popolazione europea.
I farmaci generici e i biosimilari hanno contribuito da soli a un tasso di crescita annuale del 6,9%, rappresentando l'80% di tutti i medicinali in volume e il 28% in valore nell'ultimo decennio. Il termine del brevetto per alcuni prodotti biologici, valutati circa 90 miliardi di euro, scadrà entro il 2023, creando un ambiente competitivo per questi prodotti con un enorme potenziale di crescita.
L'implementazione di una deroga SPC porterebbe benefici all'Unione Europea attraverso:
- Aggiungendo circa 90,5 miliardi di euro in più all'anno.
- Generare venticinquemila nuove opportunità di lavoro con duemila posti di lavoro diretti per l'industria degli API dell'UE. L'iniziativa aiuterà i Member States dell'UE a risparmiare 3,1 miliardi di euro sulle spese sanitarie.
- Accumulare alternative più economiche ai farmaci innovativi brevettati per consentirne l'ingresso sul mercato immediatamente dopo la scadenza della Proprietà Intellettuale (IP), migliorando l'accesso dei pazienti.
Per un produttore di farmaci con sede nell'Unione Europea, l'implementazione della deroga SPC è una delle iniziative più vantaggiose a favore dei farmaci generici. Poiché l'Autorità Sanitaria dell'UE regolamenta i medicinali per uso umano e veterinario attraverso una procedura centralizzata o decentralizzata, orientarsi tra i requisiti locali specifici può essere complesso. Un esperto, a conoscenza dei requisiti locali relativi a varie presentazioni e documenti di licenza, può aiutarvi a concentrare i vostri sforzi sui protocolli di produzione essenziali piuttosto che fissarvi su complessi ostacoli normativi. Re-immaginate il vostro potenziale aziendale sperimentando conformità e qualità. Contattate Freyr.









