
Le etichette dei medicinali fungono da guida diretta per gli utenti e contribuiscono a un uso corretto dei prodotti. Pertanto, è estremamente importante che le informazioni disponibili sulle etichette siano coerenti, facili da leggere, prive di errori e in linea con gli standard globali. Per allinearsi a ciò, la Therapeutic Goods Administration (TGA) ha introdotto alcune modifiche al modo in cui le informazioni sull'etichettatura sono presentate sui prodotti. Lo scopo di queste modifiche è migliorare la chiarezza e la coerenza delle informazioni fornite agli operatori sanitari.
Quali sono le nuove modifiche all'etichetta?
Sebbene le nuove informazioni siano già state prese in considerazione e implementate per i produttori, è consigliabile conoscerle in dettaglio per una presentazione completa. Di seguito sono elencati alcuni aspetti su cui i produttori devono lavorare quando definiscono le etichette dei loro medicinali.
1. Informazioni sul principio attivo
Secondo la nuova norma, i principi attivi dovrebbero essere:
- Posizionato in modo più evidente sul lato frontale della confezione del medicinale
- Dovrebbe essere posizionato sotto o accanto al nome del medicinale sulla parte anteriore della confezione del medicinale
- Deve essere facilmente confrontabile tra i medicinali
2. Informazioni sui medicinali
Per garantire che gli utenti e gli operatori sanitari prendano una decisione informata, le informazioni sul medicinale dovrebbero essere più chiare in termini di:
- Informazioni sanitarie critiche nelle etichette distintive
- Tutte le informazioni obbligatorie devono essere presentate in modo più chiaro e riconoscibile rispetto al colore di sfondo per migliorarne la leggibilità.
- Le sostanze dichiarabili, come gli allergeni, devono essere menzionate sull'etichetta
3. Informazioni sanitarie critiche
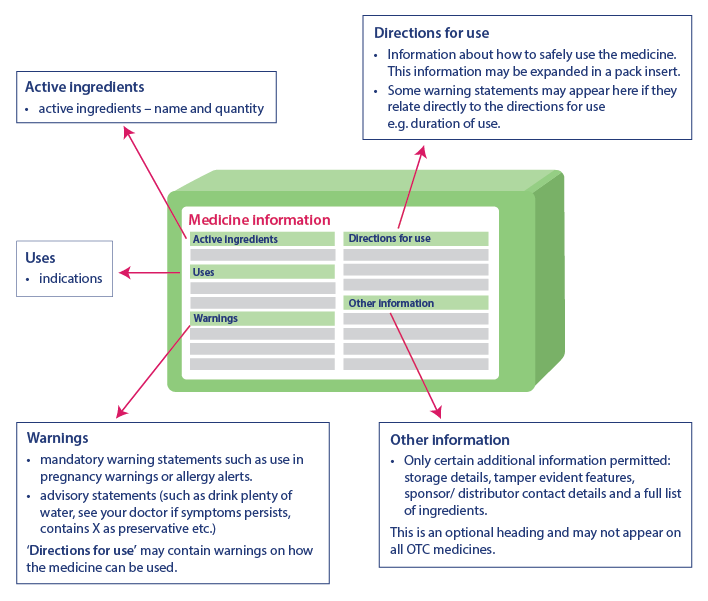
Le informazioni sanitarie critiche aiutano i consumatori a usare il medicinale in sicurezza fornendo informazioni importanti. Le informazioni presenti nella tabella delle informazioni sanitarie critiche saranno sempre nello stesso ordine, anche se potrebbe esserci una leggera differenza nella rappresentazione delle informazioni. Le informazioni sanitarie critiche presentano le seguenti intestazioni e informazioni nello stesso ordine:
- Principi attivi: Nome del principio attivo e sua quantità
- Indicazioni: Uso del medicinale
- Avvertenze: Include dichiarazioni di avvertimento, dichiarazioni consultive e avvertenze aggiuntive sull'uso del medicinale sotto 'Istruzioni per l'uso'
- Istruzioni per l'uso: Include informazioni sull'uso sicuro del medicinale
- Altre Informazioni: Include informazioni come dettagli di conservazione, caratteristiche antimanomissione, dettagli di contatto dello sponsor, elenco degli ingredienti, ecc. Questa parte potrebbe non apparire su ogni medicinale.
Fonte: TGA
4. Dispensazione Farmaceutica
Secondo la nuova norma, vengono apportate le seguenti modifiche ai dispensatori di medicinali:
- Per migliorare l'identificazione dei medicinali, le confezioni dei medicinali soggetti a prescrizione devono riportare il loro nome sui tre lati non opposti
- Le etichette dei medicinali soggetti a prescrizione devono avere uno spazio dedicato di 70x30 millimetri, a meno che non siano forniti in una confezione primaria o di avvio.
5. Informazioni sugli allergeni
I medicinali devono dichiarare le seguenti informazioni sulle etichette:
- Se presenti nel medicinale, tutte le sostanze devono essere dichiarate sull'etichetta.
- Sostanze aggiuntive, come crostacei, pesce, uova, soia, latte e frutta a guscio, devono essere dichiarate sull'etichetta
- Nel caso di nuovi allergeni, i produttori potrebbero non includerli fino alla fine del periodo di transizione di quattro anni.
Sebbene la TGA abbia pubblicato queste informazioni per i professionisti sanitari, consideriamo questo un requisito fondamentale anche per i produttori, affinché etichettino i loro prodotti in modo completo. In questo modo, i professionisti sanitari possono consultare le informazioni aggiornate senza alcuna confusione e guidare i pazienti per un consumo sicuro. È noto che la TGA ha concesso ai produttori un periodo di transizione di quattro anni per implementare queste modifiche. Dopo la data definita, le etichette dei medicinali devono essere conformi ai nuovi requisiti di etichettatura. Rimanete informati. Rimanete conformi.










