
La ricerca clinica è un pilastro del progresso medico, fornendo le prove necessarie a supportare la sicurezza e l'efficacia di nuovi trattamenti e interventi. Al centro di questa ricerca si trova il protocollo di sperimentazione clinica, un documento che delinea gli obiettivi, la progettazione, la metodologia e l'organizzazione di una sperimentazione clinica. Lo sviluppo di un protocollo di sperimentazione clinica solido è fondamentale e la revisione tra pari svolge un ruolo vitale nel garantirne la validità scientifica e l'integrità etica.
Comprendere i protocolli degli studi clinici.
Un protocollo di studio clinico non è solo un progetto per condurre la ricerca; è un contratto tra gli sperimentatori, gli sponsor e gli enti regolatori. Esso descrive in dettaglio ogni aspetto dello studio, dall'ipotesi e dagli obiettivi ai criteri di eleggibilità, alle procedure e al piano di analisi statistica. Il protocollo deve affrontare le questioni di sicurezza, le considerazioni etiche e la fattibilità complessiva dello studio.
Il ruolo della revisione paritaria
La revisione paritaria è un processo essenziale in cui esperti del settore valutano criticamente il protocollo di uno studio clinico prima che lo studio abbia inizio. Questo esame approfondito serve a diversi scopi chiave:
- Garantire il rigore scientifico: i revisori paritari valutano la logica scientifica alla base dello studio, la chiarezza della domanda di ricerca e l'adeguatezza della metodologia. Si assicurano che il disegno dello studio possa rispondere alla domanda di ricerca e che il piano di analisi statistica sia adeguato per interpretare i risultati.
- Protezione della sicurezza dei partecipanti: I revisori valutano i potenziali rischi e benefici per i partecipanti, assicurando che le misure di sicurezza siano in atto e che lo studio aderisca agli standard etici. Confermano che i diritti, la sicurezza e il benessere dei soggetti dello studio sono prioritari rispetto agli interessi della scienza e della società.
- Migliorare la credibilità: Un protocollo sottoposto a una rigorosa revisione paritaria acquisisce credibilità tra le parti interessate, incluse le autorità di regolamentazione, i comitati etici e i potenziali partecipanti. Ciò dimostra un impegno per la qualità e l'integrità nel processo di ricerca.
- Agevolare l'approvazione normativa: gli organismi di regolamentazione spesso richiedono prove della revisione paritaria nell'ambito del processo di richiesta di sperimentazione clinica. Un protocollo ben revisionato ha maggiori probabilità di soddisfare i requisiti rigorosi per l'approvazione della sperimentazione e la successiva registrazione del farmaco o del dispositivo.
- Promuovere la collaborazione: La revisione tra pari incoraggia la collaborazione e la condivisione delle conoscenze tra i ricercatori. Può portare all'identificazione di potenziali problemi e all'incorporazione di suggerimenti che rafforzano il protocollo.
Il processo di revisione paritaria
Il processo di revisione paritaria prevede tipicamente i seguenti passaggi:
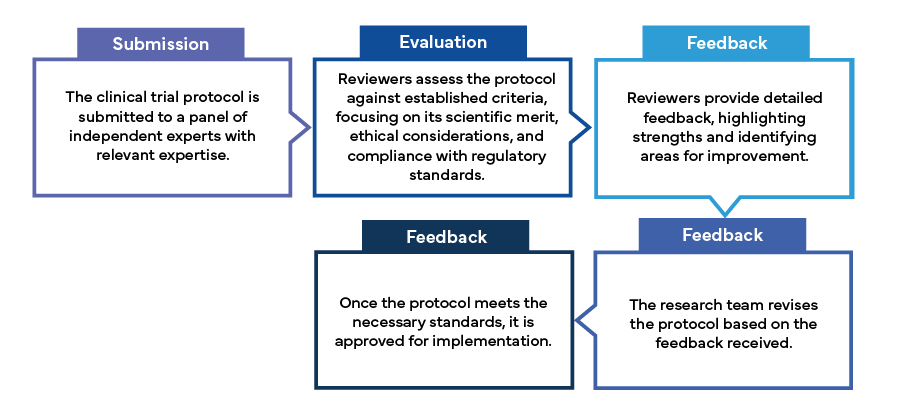
Conclusione
La revisione tra pari è un elemento fondamentale nello sviluppo dei protocolli di sperimentazione clinica, garantendo rigore scientifico, sicurezza dei partecipanti e conformità normativa. Collaborare con Freyr Solutions per i servizi di revisione tra pari offre ulteriori vantaggi, tra cui l'accesso a un team di professionisti esperti con diverse competenze negli affari regolatori, nella redazione medica e nella ricerca clinica. L'approccio collaborativo di Freyr e il suo impegno per la garanzia della qualità possono aiutare a semplificare il processo di revisione tra pari, accelerare l'approvazione del protocollo e migliorare il successo complessivo delle sperimentazioni cliniche.










