KGMP sta per Korea Good Manufacturing Practice, che si basa sulla ISO 13485:2016. È lo standard accettato a livello internazionale per il Quality Management System (QMS) dei dispositivi medici. Tutti i produttori di dispositivi medici che commercializzano i loro dispositivi in Corea del Sud devono rispettare gli standard KGMP.
Il Certificato KGMP è obbligatorio per tutti i dispositivi?
I dispositivi medici e diagnostici in vitro (IVD) rientranti nelle Classi II, III e IV devono essere conformi ai regolamenti KGMP e devono ottenere il certificato KGMP. I dispositivi di Classe I sono esenti dalla certificazione KGMP ma devono aderire ai regolamenti GMP sui dispositivi medici MFDS. I produttori di Classe I possono optare volontariamente per il “riconoscimento della conformità GMP dei dispositivi medici di Classe I”.
Quali sono gli Organismi di Legge Coinvolti nell'Ispezione KGMP?
I dispositivi di classe II sono soggetti a revisione da parte di terzi da parte di organismi di audit accreditati MFDS, mentre i dispositivi di Classe III e IV richiedono un'ispezione combinata da parte del revisore terzo e dell'MFDS.
Chi può richiedere il Certificato KGMP?
I produttori nazionali possono presentare direttamente le loro domande all'organizzazione di audit di terze parti. Per i produttori esteri, il rappresentante autorizzato locale del produttore estero è tenuto a ottenere una licenza.
Qual è la procedura per ottenere un certificato KGMP?
Per la prima volta, la domanda (richiedenti - AR locale del produttore straniero e produttori nazionali) deve essere presentata a revisori terzi accreditati MFDS. Il processo per ottenere un certificato KGMP è descritto di seguito:
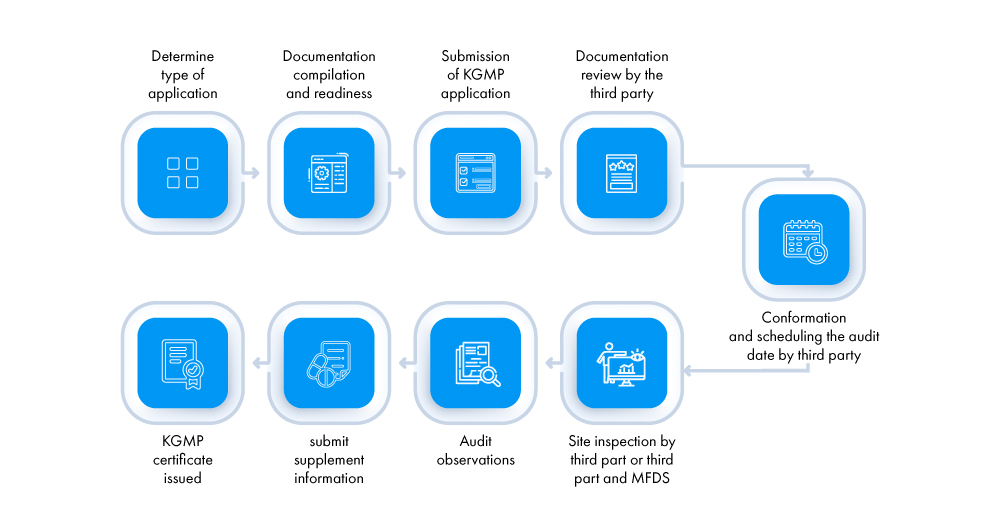
Quali sono i diversi tipi di ispezioni per ottenere un certificato KGMP?
A seconda della classe di rischio del dispositivo e del tipo di domanda (nuova, regolare o di modifica), può trattarsi di un'ispezione in loco o di una revisione della documentazione. Prima di richiedere la certificazione KGMP, i produttori devono comprendere i possibili tipi di ispezioni e il tipo applicabile al loro scenario. I fattori chiave da considerare sono:
- Se i dispositivi fabbricati nel sito sono già registrati e commercializzati in Corea o se il dispositivo in questione è il primo ad essere lanciato nel mercato coreano.
- Se un nuovo dispositivo (un'altra categoria) viene introdotto nello stabilimento di produzione già certificato KGMP.
- Se il sito di produzione del dispositivo viene modificato
Ispezione iniziale: L'ispezione iniziale viene condotta quando un dispositivo in fase di lancio è fabbricato in una struttura non certificata KGMP o se il certificato KGMP esistente è scaduto prima del suo rinnovo.
Ispezione Regolare: L'ispezione regolare viene eseguita ogni tre anni per una valutazione periodica al fine di garantire che i produttori continuino a rispettare gli standard GMP.
Ispezione Aggiuntiva: Se un produttore certificato GMP aggiunge e produce un dispositivo medico corrispondente a una nuova categoria, dovrà sottoporsi a un'ispezione aggiuntiva per la nuova categoria di prodotto. In base all'esito dell'ispezione regolare, un'ispezione aggiuntiva può essere parziale o completa. La validità del certificato rilasciato tramite ispezione aggiuntiva sarà allineata con il certificato KGMP rilasciato inizialmente.
Valutazione del cambiamento: La valutazione viene eseguita quando il sito di produzione viene modificato. Si fa un'eccezione per i magazzini e i laboratori, che hanno un impatto insignificante sulla qualità del prodotto.
Come viene condotta la valutazione KGMP?
Il sito di produzione sarà sottoposto a revisione documentale o a ispezione in loco da parte dei revisori di terze parti o del MFDS.
Revisione documentale: La revisione documentale viene eseguita quando il produttore possiede un certificato QMS valido o quando è disponibile un rapporto di ispezione del sito valido rilasciato da agenzie certificate. Quando un altro importatore desidera ottenere un certificato KGMP per un produttore che ha già un certificato KGMP valido da un'altra importazione.
Ispezione in loco: L'ispezione in loco viene effettuata per i dispositivi medici di Classe II, III e IV. L'ispezione del sito può essere eseguita da revisori esterni o congiuntamente da revisori esterni e MFDS.
Quali sono le Tempistiche per Ottenere un Certificato KGMP?
A seconda della correttezza del documento presentato e della preparazione del produttore per l'ispezione in loco, l'MFDS rilascia il certificato KGMP entro due-tre mesi dalla presentazione della domanda. La tempistica potrebbe estendersi ulteriormente se gli auditor sollevano domande durante l'ispezione, e i produttori potrebbero anche impiegare più tempo per rispondere alle domande.
Qual è la validità del Certificato KGMP?
Dopo un'ispezione approfondita, l'MFDS rilascia un certificato KGMP valido per tre anni, che deve essere rinnovato alla scadenza del periodo.
Qual è la procedura per il rinnovo di un certificato KGMP?
Se il certificato KGMP è in scadenza, il titolare della licenza può importare i dispositivi ma non deve distribuirli fino al rinnovo del certificato KGMP. Il richiedente deve presentare la domanda di rinnovo 90 giorni prima della scadenza del certificato KGMP. La domanda sarà esaminata da auditor accreditati MFDS e la documentazione presentata durante i tre anni di validità del certificato originale sarà revisionata. Una volta completata l'ispezione, il certificato KGMP viene rinnovato. La valutazione per il rinnovo del certificato KGMP dipende dalla classe dei dispositivi.
Tipo di ispezione | Classe II | Classe III | Classe IV |
Ispezione Iniziale | Ispezione in loco da parte di un revisore terzo | Ispezione congiunta in loco (terza parte e MFDS) | Ispezione congiunta in loco (Terza Parte e MFDS) |
Ispezione Regolare | Ispezione in loco da parte di un revisore terzo* | Ispezione in loco da parte di un revisore terzo* | Ispezione congiunta in loco (terza parte e MFDS) |
Ispezione aggiuntiva | Revisione documentale da parte di terzi | Revisione documentale da parte di terzi | Revisione documentale da parte di terzi |
Valutazione del Cambiamento | Revisione documentale da parte di terzi | Revisione documentale da parte di terzi | Revisione documentale da parte di terzi |
*Soggetto a ispezione congiunta in caso di preoccupazioni relative alla sicurezza e all'efficacia durante il periodo di tre anni
I produttori che intendono entrare in Corea del Sud devono comprendere a fondo i requisiti KGMP stabiliti dal MFDS. I produttori sono tenuti a mantenere sempre la documentazione dettagliata e il sito di produzione in conformità con gli standard KGMP. Ottenere la certificazione KGMP può essere difficile per i produttori a causa del rigoroso quadro normativo stabilito dal MFDS. I produttori possono optare per un partner normativo esperto per una strategia appropriata e ottenere un certificato KGMP.
Per saperne di più sulle Buone Pratiche di Fabbricazione della Corea, contattate il nostro Esperto Normativo.
