I dispositivi medici innovativi sono essenziali per migliorare i risultati sanitari, affrontare le esigenze mediche in evoluzione e fornire soluzioni economicamente vantaggiose per pazienti e operatori sanitari. La strategia SAKIGAKE è un processo di revisione e approvazione accelerato per i dispositivi medici innovativi in Giappone. Questa strategia è stata avviata dal Ministero della Salute, del Lavoro e del Welfare (MHLW) del Giappone nel 2015, con l'obiettivo di accelerare lo sviluppo e la commercializzazione di dispositivi medici innovativi in Giappone.
Nell'ambito della strategia SAKIGAKE, i dispositivi medici che soddisfano determinati criteri di innovazione possono ricevere una revisione e un'approvazione prioritarie da parte della Pharmaceuticals and Medical Devices Agency (PMDA), l'Agenzia normativa responsabile delle approvazioni dei dispositivi medici in Giappone. I criteri di designazione per l'innovazione includono i seguenti:
- Dispositivi con efficacia notevole; il dispositivo è previsto che fornisca un significativo beneficio clinico con un meccanismo d'azione innovativo e un miglioramento radicale per i pazienti rispetto ai dispositivi medici esistenti.
- In primo luogo, il dispositivo è idoneo per le approvazioni in Giappone o contemporaneamente in Giappone e in altri paesi.
- Il dispositivo ha il potenziale per rispondere a esigenze mediche insoddisfatte in Giappone. La condizione medica target dovrebbe essere grave, potenzialmente letale o con sintomi persistenti.
Nell'ambito della strategia SAKIGAKE, i produttori di dispositivi medici possono ricevere una serie di vantaggi, tra cui:
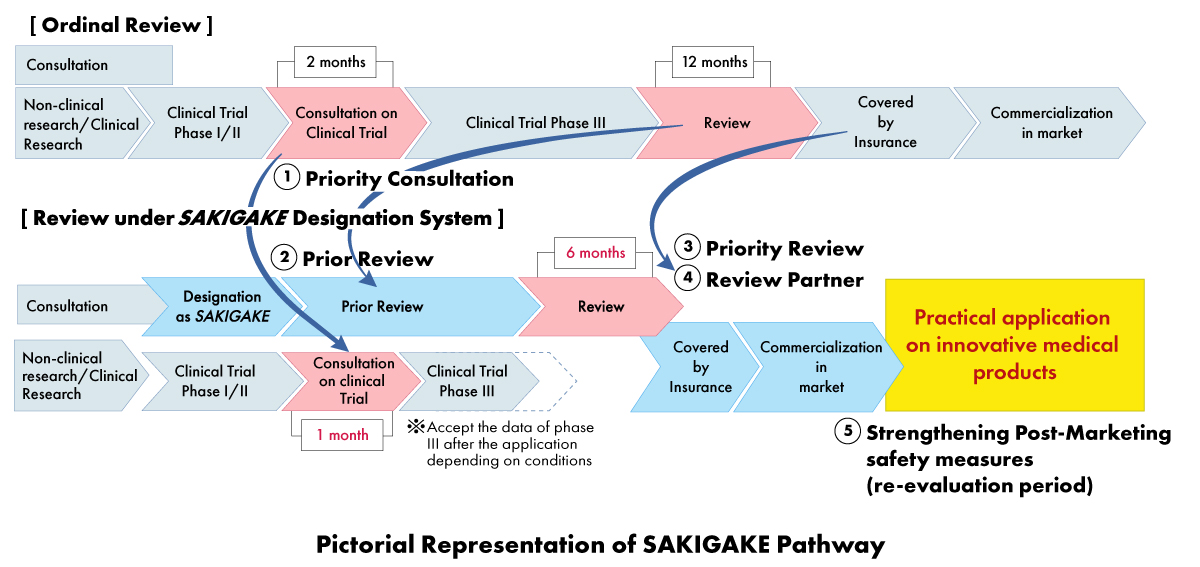
- Consultazione Prioritaria: Riduzione del tempo di attesa per la consultazione sugli studi clinici a un mese.
- Revisione Prioritaria: I prodotti designati SAKIGAKE ricevono una revisione prioritaria, con l'obiettivo di completare il processo di revisione entro sei mesi anziché 12 mesi.
- Revisione Efficace prima della Domanda: Incoraggiare la consultazione e accettare materiali in inglese.
- Partner di revisione dedicato: A ogni prodotto designato SAKIGAKE viene assegnato un responsabile di revisione dedicato per l'intero processo di approvazione.
- Rafforzamento delle Misure di Sicurezza Post-commercializzazione: Estensione del periodo di riesame e facilitazione del collegamento con le società scientifiche.
Come presentare la domanda?
- Da parte del richiedente: Il richiedente sta presentando la domanda alla Divisione di Valutazione e Licenze (ELD) della PMDA.
- Da PMDA-ELD: L'ELD si sta avvicinando a un potenziale richiedente.
P.C- PMDA, Giappone.
Nel complesso, il sistema SAKIGAKE fornisce un percorso accelerato per lo sviluppo e l'approvazione di dispositivi medici innovativi in Giappone. Mira a migliorare gli esiti dei pazienti e a promuovere l'innovazione nell'industria dei dispositivi medici. Il produttore deve consultare la PMDA all'inizio del processo di sviluppo per discutere i requisiti normativi e ricevere feedback sui propri piani di sviluppo del prodotto.
Per saperne di più sui percorsi di registrazione dei dispositivi medici in Giappone, contattate subito un esperto normativo! Rimanete informati. Rimanete conformi.
