Jednostka Oceniająca Zgodność (CAB) przeprowadza ocenę zgodności różnych podmiotów w systemie łańcucha dostaw wyrobów medycznych. Jednostka Oceniająca Zgodność (CAB) w Malezji przeprowadza szczegółowe audyty i ocenia wszystkie obowiązujące elementy ustalone przez Urząd ds. Wyrobów Medycznych (MDA) w Malezji, a także weryfikuje zgodność wyrobu z odpowiednimi normami.
Ta część serii blogów przeprowadzi Państwa przez rolę CAB w rejestracji i zatwierdzaniu wyrobów medycznych w Malezji. Mogą Państwo również zapoznać się z wymogiem MDA dotyczącym certyfikacji CAB, który został omówiony w pierwszej części.
Ocena zgodności to systematyczne i ciągłe badanie dowodów i procedur w celu zapewnienia bezpieczeństwa, działania, korzyści i ryzyka wyrobów medycznych. Zapewnia również zgodność produkcji z Zasadniczymi Wymaganiami Bezpieczeństwa i Działania (EPSP) oraz wymogami Ustawy o Wyrobach Medycznych z 2012 roku (Ustawa 737). Klasyfikacja wyrobu medycznego określa procedury oceny zgodności, które należy przeprowadzić. Ocena zgodności staje się bardziej rygorystyczna wraz ze wzrostem ryzyka związanego z wyrobem medycznym; dlatego ocena ryzyka wyrobu medycznego jest niezbędna.
Jednostki oceniające zgodność (CAB) przeprowadzają różne rodzaje ocen w zależności od działalności prowadzonej przez organizację i zakresu zastosowania. Obejmują one:
- Ocena dokumentacji technicznej
- Ocena systemów QMS pod kątem zgodności z ISO 13485
- Certyfikacja Dobrej Praktyki Dystrybucyjnej dla wyrobów medycznych (GDPMD)
- Pełna ocena zgodności dla rejestracji wyrobów
- Uproszczona weryfikacja rejestracji wyrobów
Jednostki oceniające zgodność (CAB) odgrywają kluczową rolę dla każdego uczestnika systemu łańcucha dostaw, w tym producentów wyrobów, importerów, dystrybutorów, upoważnionych przedstawicieli (AR) i innych.
Importerzy, dystrybutorzy i upoważnieni przedstawiciele wymagają, aby ich placówki były zarejestrowane w MDA w celu prowadzenia działalności. Certyfikat GDPMD jest niezbędnym warunkiem wstępnym, który należy złożyć wraz z wnioskiem o licencję na prowadzenie działalności. CAB-y przeprowadzają ocenę zgodności systemów jakości tych podmiotów z przepisami GDPMD ustanowionymi przez MDA przed wydaniem certyfikatu. Ocena ta obejmuje przegląd dokumentacji technicznej oraz audyt obiektów na miejscu.
Producenci urządzeń są również zależni od CABów w celu zarejestrowania ich urządzenia w MDA, Malezja. Krajowi producenci wymagają, aby ich zakłady produkcyjne były zarejestrowane w MDA. CAB.
Oprócz rejestracji zakładu, CABs również odgrywają swoją rolę w rejestracji wyrobów w MDA. Wyroby medyczne z zatwierdzeniami z krajów referencyjnych podlegają weryfikacji przez CAB, natomiast wyroby bez zatwierdzeń z krajów referencyjnych podlegają pełnej ocenie przez CAB.
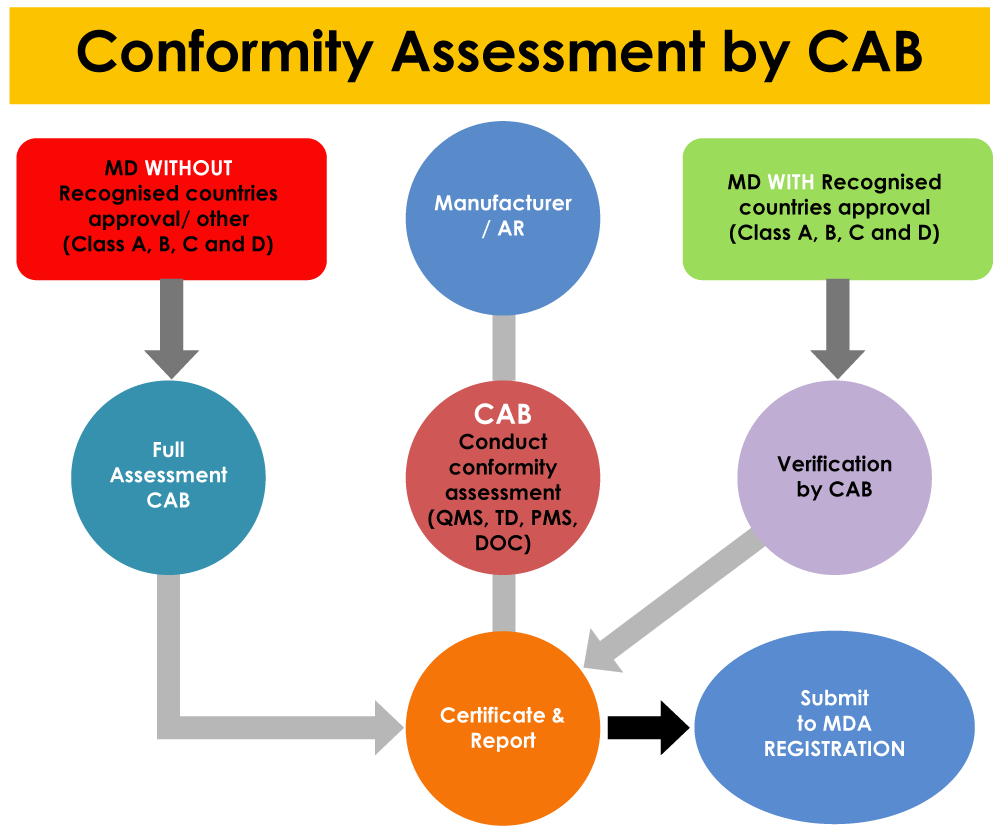
Jeśli w systemie QMS, systemie PMS i kompletnej dokumentacji wyrobu (w tym w każdym raporcie z badań) zostaną stwierdzone jakiekolwiek niezgodności, istnieje duże prawdopodobieństwo odrzucenia wniosku przez CAB.
Przeczytaj część 1 artykułu, aby poznać wymagania MDA i procedury zatwierdzania certyfikacji CAB.
Czy zamierzasz wprowadzić swoje wyroby medyczne lub IVD na rynek malezyjski? Chcesz dowiedzieć się więcej o rolach i obowiązkach CAB w zakresie rejestracji wyrobów? Skontaktuj się z ekspertem ds. regulacji. Bądź na bieżąco. Zachowaj zgodność.









