
Rozporządzenie Unii Europejskiej (UE) w sprawie wyrobów medycznych (MDR) jest na ustach wszystkich od pewnego czasu. MDR zastąpiło Dyrektywę o wyrobach medycznych (MDD) oraz Dyrektywę o aktywnych wyrobach medycznych do implantacji (AIMDD). Początkowo całe przejście miało wejść w życie do maja 2020 r.; jednak z powodu pandemii COVID-19 wdrożenie zostało przesunięte na 26 maja 2021 r. Zgodnie z tym harmonogramem, do 26 maja 2024 r. wszystkie certyfikaty MDD stracą ważność, a producenci wyrobów medycznych będą musieli dostosować się do EU MDR. Ponadto, wyroby MDD legalnie wprowadzone do obrotu zgodnie z dyrektywami 90/385/EWG i 93/42/EWG przed 26 maja 2020 r., oraz wyroby wprowadzone do obrotu od 26 maja 2020 r. na podstawie certyfikatu, będą nadal dostępne na rynku do 27 maja 2025 r. Harmonogramy przedstawiono poniżej –
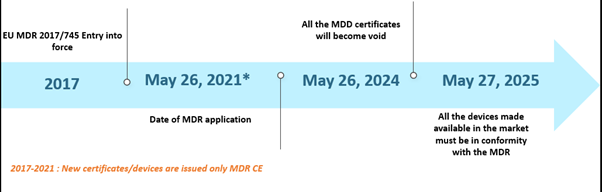
Terminy przeszłych scenariuszy EU MDR
Jednakże ograniczona zdolność Jednostek Notyfikowanych (NB) oraz nieprzygotowanie producentów stworzyły pewne wyzwania we wdrożeniu MDR zgodnie z ustalonym harmonogramem. Według stanu na październik 2022 roku, istnieje łącznie trzydzieści osiem (38) Jednostek Notyfikowanych (NB), które otrzymały około 8120 wniosków o certyfikację EU MDR, z czego wydano 1990 certyfikatów. Zgodnie z ich szacunkami, przy początkowym harmonogramie, można było przetworzyć tylko 7000 certyfikatów, co doprowadziło do przedłużenia terminu. Ponadto, jednym z innych prawdopodobnych powodów przedłużenia było zapewnienie dalszej dostępności bezpiecznych wyrobów medycznych, których certyfikaty już wygasły lub mają wygasnąć przed 26 maja 2024 roku. Obecny scenariusz dla przedłużonego terminu przedstawiono poniżej-
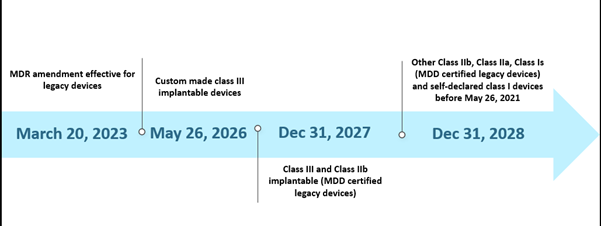
Terminy przeszłych scenariuszy EU MDR
Nowe rozszerzenie ma zastosowanie do starszych wyrobów spełniających artykuł 120 (3e) z ważnym oznakowaniem CE MDD lub odstępstwem na dzień 20 marca 2023 r. i pozostanie na rynku wraz z wyrobami oznakowanymi CE MDR. Do 26 maja 2024 r. producenci starszych wyrobów powinni mieć wdrożony system zarządzania jakością (QMS) i złożyć wniosek do jednostki notyfikowanej (NB) wyznaczonej zgodnie z MDR o ocenę zgodności, a do 26 września 2024 r. producenci starszych wyrobów powinni mieć zawartą umowę z jednostką notyfikowaną (NB) wyznaczoną zgodnie z MDR.
Teraz przyjrzyjmy się wpływowi, jaki to przedłużenie może mieć na producentów.
Możliwości, jakie producenci zyskują dzięki temu rozszerzeniu:
- Rozszerzony dostęp do rynku dla producentów wyrobów medycznych posiadających certyfikaty MDD/AIMDD, którzy już podjęli inicjatywy w zakresie zgodności z MDR.
- Producenci posiadający certyfikat MDR, których certyfikaty CE MDD/AIMDD nie zostały cofnięte, mogą wprowadzać na rynek wyroby dotychczasowe do końca okresu przejściowego, oprócz swoich wyrobów zgodnych z MDR.
- Producenci, którzy posiadają krajowe odstępstwo na dzień 20 marca 2023 r., mogą skorzystać z okresu przejściowego.
- Okres przedłużenia daje więcej czasu na lepsze zrozumienie zasad i przepisów, co pomaga usprawnić proces i osiągnąć zgodność z MDR.
Wyzwania, które mogą pojawić się dla producentów w związku z tym rozszerzeniem:
- Producenci starszych wyrobów, którzy nie chcieli przestrzegać MDR, nie odniosą z tego tytułu korzyści rynkowych.
- Przedłużenie MDR może spowodować przeciąganie się procesów certyfikacji i opóźnienie wprowadzania produktów na rynek, co jest bezpośrednim wynikiem zaległości w przeglądach dokonywanych przez jednostki notyfikowane.
Jakie działania powinni podjąć producenci?
- Konieczne jest, aby producenci określili klasę ryzyka MDR swojego wyrobu medycznego, aby szybko zidentyfikować odpowiedni harmonogram przejściowy zgodnie ze zmienionymi przepisami MDR.
- Aby zapewnić zgodność z przepisami MDR, kluczowe jest zidentyfikowanie i nawiązanie komunikacji z wyznaczonymi przez MDR NBs posiadającymi specyficzne kompetencje wymagane do klasyfikacji Twojego wyrobu medycznego.
- Kluczowe jest przeprowadzenie kompleksowej oceny luk dla wyrobu medycznego certyfikowanego zgodnie z MDD/AIMDD, zidentyfikowanie i usunięcie wszelkich niezgodności z przepisami MDR oraz zapewnienie terminowej zgodności.
Dla producentów kluczowe jest podjęcie natychmiastowych działań w celu zapewnienia zgodności z MDR. Wydłużony harmonogram oferuje producentom pewne możliwości osiągnięcia zgodności z MDR, ale stwarza również wyzwania, takie jak opóźnione procesy certyfikacji i koszty zgodności. Aby sprostać tym wyzwaniom i wykorzystać możliwości, pozwól naszemu zespołowi profesjonalistów pomóc Ci w procesie zgodności z MDR i zapewnić sukces w tym wymagającym środowisku regulacyjnym. Umów się na spotkanie z nami już dziś, aby dowiedzieć się więcej o tym, jak możemy pomóc Ci osiągnąć zgodność z MDR i być na bieżąco. Bądź na bieżąco. Zachowaj zgodność.









