
Un régimen de terapia farmacológica es diverso para los medicamentos que pueden ser aprobados para usarse en combinación con un medicamento previamente aprobado o para dos nuevos medicamentos desarrollados simultáneamente, que mejoran sinérgicamente la eficacia. Las terapias contra el cáncer con un solo fármaco mostraron significativamente la resistencia a los medicamentos como una amenaza importante para los pacientes que reciben tratamientos con medicamentos contra el cáncer. Considerando la diversidad en la terapia combinada adoptada para los tratamientos contra el cáncer, los regímenes de dos fármacos están reemplazando gradualmente la monoterapia como estándar de atención en los pacientes. Durante la última década, la terapia combinada ha ofrecido un mejor alcance de tratamiento.
Si es una organización consciente del cambio de paradigma en el desarrollo de fármacos contra el cáncer, desde el desarrollo de un solo fármaco hasta combinaciones novedosas, debe saber que este avance ha llevado a un aumento de las solicitudes para conceder solicitudes de etiquetado cruzado por parte del solicitante. Al reconocer las conversaciones, las últimas tendencias de la industria y su comprensión actual de los requisitos de un patrocinador, la Administración de Alimentos y Medicamentos de US (USFDA) ha concedido un conjunto de directrices para proporcionar apoyo con los cambios de etiquetado para regímenes de medicamentos con productos farmacéuticos previamente aprobados.
¡Enhorabuena! Su solicitud de orientación sobre etiquetado cruzado ha sido concedida, si:
(a) La indicación para el régimen de combinación solicitado está aprobada bajo una indicación de medicamento similar.
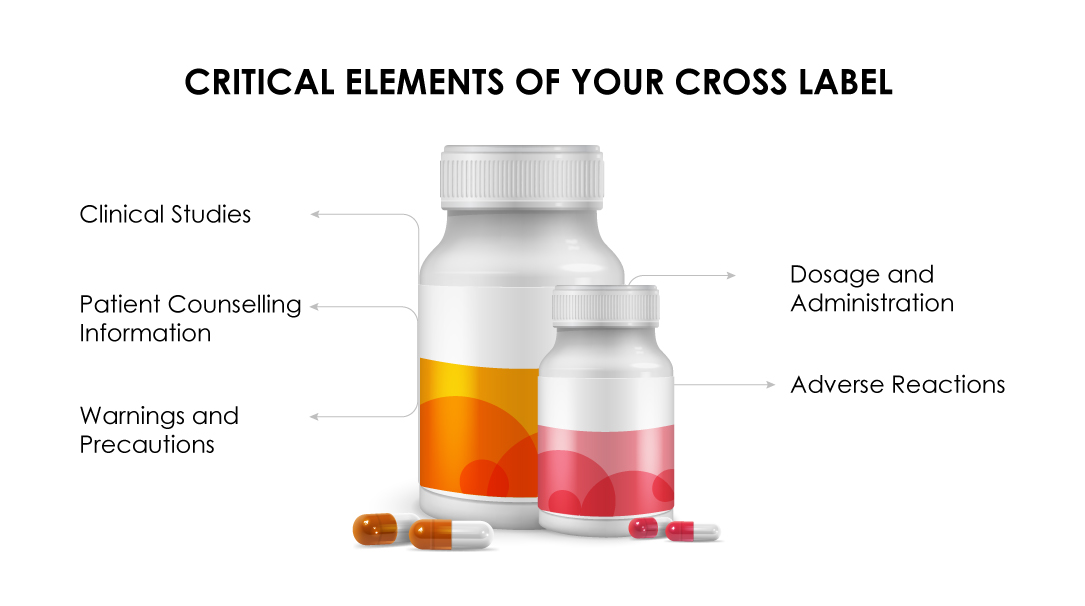
(b) La sección de Posología y Administración debe destacar la dosis recomendada para el medicamento del patrocinador en un régimen de combinación.
(c) Los datos del estudio clínico deben justificar los beneficios de la combinación para todos los medicamentos del régimen.
(d) En la sección «Advertencias y precauciones» debe indicarse el carácter único del régimen combinado basándose en datos clínicamente significativos.
(e) Las Reacciones adversas deben destacarse tal como se observaron en los ensayos clínicos.
(f) El folleto informativo para el paciente debe limitarse a los efectos tóxicos específicos de la formulación.
La información relacionada únicamente con el medicamento del patrocinador debe ocupar las secciones restantes de la etiqueta, a menos que sea necesario mencionar algunos factores farmacocinéticos únicos.
La guía aprobada para el etiquetado cruzado se dirige específicamente a los productos de terapia anticancerígena para establecer la comprensión fundamental del etiquetado cruzado. Para ayudar a los patrocinadores con los obstáculos operativos y reglamentarios relacionados con el cambio de etiqueta, la guía establece:
- Plazos
Se espera que los solicitantes propongan el contenido preliminar para el etiquetado cruzado con una justificación basada en la evidencia del papel de cada producto mencionado en el régimen, en su propuesta de etiquetado cruzado de un nuevo fármaco anticancerígeno en una solicitud pre-NDA o BLA.
Se espera que el etiquetado cruzado se identifique para cada medicamento bajo el régimen al mismo tiempo. Sin embargo, la aprobación puede concederse una tras otra, en secuencia, debido a la diferencia en el cronograma del medicamento.
- Presentación reglamentaria
Cada solicitante que busque una etiqueta cruzada debe presentar una solicitud original o un suplemento de eficacia para el etiquetado cruzado.
Un solicitante puede optar por referenciar datos de otras solicitudes para justificar los beneficios sinérgicos del régimen de combinación.
Al hacer referencia a los datos, el solicitante:
- debe asegurarse de que los datos de referencia cruzada ya han sido presentados por la FDA.
- debe anotar cada sección de los datos del solicitante a la que se hace referencia cruzada.
- debe incluir (en la sección inferior) solo información relevante para el medicamento del solicitante:
- ADVERTENCIA EN RECUADRO (Si corresponde)
- FORMAS FARMACÉUTICAS Y CONCENTRACIONES
- CONTRAINDICACIONES
- INTERACCIONES MEDICAMENTOSAS
- USO EN POBLACIONES ESPECÍFICAS
- SOBREDOSIS
- DESCRIPCIÓN
- FARMACOLOGÍA CLÍNICA
- TOXICOLOGÍA NO CLÍNICA
- REFERENCIAS
- PRESENTACIÓN, ALMACENAMIENTO Y MANIPULACIÓN
El etiquetado cruzado para medicamentos contra el cáncer puede ayudar a educar a la población de pacientes sobre la dosificación, la eficacia y los beneficios de los resultados del tratamiento. Con el aumento exponencial de la terapia combinada como método estándar, las etiquetas cruzadas pueden resultar beneficiosas para mejorar o introducir los métodos terapéuticos actuales. Nuestros expertos experimentados en Freyr están bien versados en los desafíos dinámicos del etiquetado y pueden ofrecer soluciones a sus consultas de etiquetado. Experimente el mejor soporte profesional en etiquetado. ¡Contacte con Freyr!










