
A partir del 31 de enero de 2022, la nueva regulación farmacéutica de la Unión Europea (UE) para el Reglamento de Ensayos Clínicos (CTR) ha pasado a ser obligatoria, derogando la Directiva de Ensayos Clínicos 2001/20/CE. El reglamento armoniza los protocolos para la evaluación y supervisión de los ensayos clínicos en toda la UE. Las directrices se revisaron para promover un enfoque uniforme de la investigación clínica, al tiempo que se enfatiza la seguridad de los participantes en los ensayos clínicos y una mayor divulgación pública.
El reglamento establece un nuevo sistema de evaluación en dos partes para todos los ensayos clínicos de la UE. La Parte I consiste en una evaluación científica de la documentación principal del ensayo clínico, y la Parte II consiste en una evaluación ética de la documentación a nivel nacional. Tras esta evaluación en dos partes, cada Estado miembro tomará una decisión unificada sobre el ensayo y notificará al promotor a través del Sistema de Información de Ensayos Clínicos.
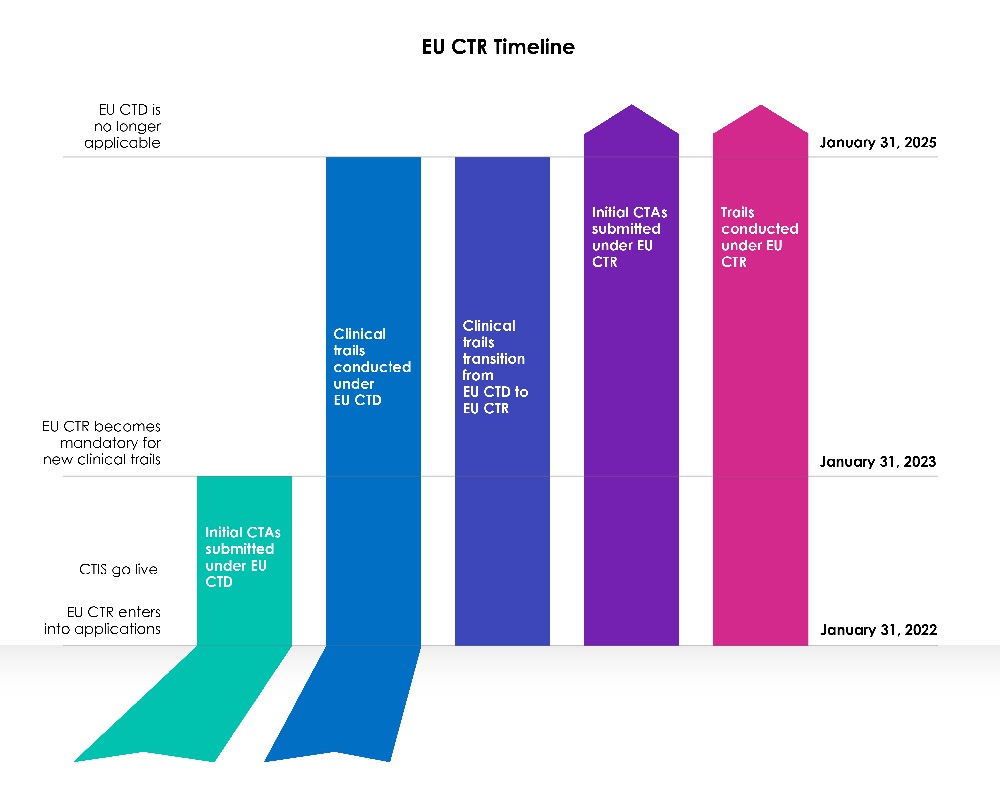
Plazos de transición para nuevos solicitantes
Una fase de transición de tres (03) años comenzó con la fecha de puesta en marcha del CTIS de la UE.
Año 1 (31 de enero de 2022 al 30 de enero de 2023):
La Directiva de Ensayos Clínicos 2001/20/CE de la Unión Europea (UE) (EU-CTD) ha regido los ensayos clínicos en la UE desde 2004. Se esforzó por estandarizar las normas y mejoró significativamente la seguridad de los pacientes en los ensayos clínicos. Sin embargo, en la práctica, creó consecuencias no deseadas. Durante el primer año, tras la implementación del CTIS, se permitió a los promotores elegir si solicitaban una nueva Solicitud de Ensayo Clínico (CTA) en el Sistema de Información de Ensayos Clínicos (CTIS) en virtud de la Directiva de Ensayos Clínicos (CTD: Directiva 2001/20/CE), o si utilizaban el CTIS de acuerdo con la legislación vigente, el Reglamento de Ensayos Clínicos (UE) n.º 536/2014.
Ambas ideas eran viables, y los patrocinadores tuvieron la oportunidad de elegir qué legislación seguir.
Los miembros estaban listos para usar el Clinical Trial Information System (CTIS) y aceptaron solicitudes bajo la nueva legislación, Clinical Trials Regulation (EU CTR), el primer día de funcionamiento del CTIS.
Años 2 y 3 (31 de enero de 2023 al 31 de enero de 2025):
A partir del 31 de enero de 2023, todas las nuevas solicitudes de ensayos clínicos deben presentarse a través del CTIS conforme a la nueva legislación (CTR).
No se permite la presentación de nuevas solicitudes de ensayos clínicos (CT) en EudraCT bajo la Directiva de Ensayos Clínicos (CTD). La Directiva de Ensayos Clínicos de la UE ya no permite la admisión de nuevos Member States después del 31 de enero de 2023. Los ensayos realizados bajo la CTD deben ser primero transicionados, después de lo cual se puede presentar una solicitud adicional relacionada con un Member State a través de EU CTIS.
Para Solicitantes Existentes
Las solicitudes de ensayos clínicos presentadas antes del 30 de enero de 2023, bajo la antigua legislación (CTD) utilizando EudraCT, se les permitirá continuar hasta su finalización bajo esa Directiva ((CTD: Directiva 2001/20/CE), hasta el 30 de enero de 2025. Los procedimientos permanecerán inalterados, y los patrocinadores podrán presentar modificaciones significativas y avisos de finalización del ensayo según lo exija la reglamentación. EudraCT permanecerá activo durante el período de transición para permitir que estos ensayos continúen.
Sin embargo, es importante señalar que las solicitudes de transición pueden presentarse en cualquier momento durante el periodo de transición de tres (03) años, y se anima a los patrocinadores a completar el proceso con suficiente antelación en el periodo de transición para asegurar la continuidad de los ensayos clínicos de la UE más allá del 30 de enero de 2025, considerando los días festivos legales y la interrupción de dos (02) semanas en invierno.
Ensayos no transferibles
- Los ensayos que ya han concluido o que concluirán justo antes del final del período de transición de la UE/EEA no deben ser objeto de transición.
- Si se ha completado una notificación de finalización del ensayo en todos los países miembros de la UE/EEA, pero aún no se ha notificado la finalización global del ensayo, el estudio no debería ser objeto de transición. Según la Directiva, la finalización global del ensayo y los resultados resumidos del ensayo deberían publicarse a través de EudraCT.
- Los ensayos que comenzaron antes de la implementación de la Directiva 2001/20/CE no se benefician de dicho procedimiento de transición. Si son intervencionales y deben seguir operando después de que finalice la fase de transición del CTR, debe presentarse una nueva solicitud de ensayo clínico (CT Application) bajo el CTR.
- Los ensayos pediátricos realizados fuera de la UE/EEA, pero a los que se les ha asignado un número EudraCT, tampoco deben convertirse.
- Los ensayos que están en espera después de que haya finalizado el período de transición no pueden pasar por el proceso de transición. Reiniciar el ensayo en estas circunstancias requeriría la presentación de una nueva solicitud de ensayo clínico (CT Application) bajo el CTR.
El CTIS de la UE recibe actualizaciones técnicas de la EMA regularmente para mejorar sus características y funcionalidades. Cuando se realizan cambios importantes en el CTIS, la EMA emite notas de lanzamiento que describen lo que ha cambiado en el sistema. Las actualizaciones pueden incluir mejoras en las características y funcionalidades existentes, la adición de nuevas características y mejoras funcionales y técnicas. Un socio reglamentario experimentado puede abordar los desafíos potenciales y ayudar a los patrocinadores con la transición de ensayos para los ensayos existentes y futuros como parte de las estrategias de desarrollo clínico. Haga clic aquí para obtener más información sobre el CTIS y la experiencia de Freyr en el área: https://www.freyrsolutions.com/medical-devices/regulatory-affairs.










