
La Administración de Alimentos y Medicamentos de US (US FDA) publicó una guía en diciembre de 2022, una revisión de la guía titulada ‘Falta de respuesta a una Carta de Respuesta Completa (CRL) de ANDA dentro del plazo normativo: Guía para la industria,’ de julio de 2022. Tiene como objetivo guiar a los solicitantes de Solicitudes Abreviadas de Nuevos Medicamentos (ANDAs) presentadas bajo la sección 505(j) de la Ley Federal de Alimentos, Medicamentos y Cosméticos (FD&C Act) (21 U.S.C. 355(j)). Una respuesta completa y relevante a una CRL es crucial para la aprobación del medicamento genérico. El documento de guía ofrece recomendaciones sobre las repercusiones de recibir una CRL y las acciones que la FDA puede tomar si no se responde a la CRL dentro del plazo especificado.
La FDA debe asegurar que los medicamentos genéricos aprobados cumplan con los estándares de seguridad, calidad, eficacia y asequibilidad. Si la ANDA no cumple con los requisitos normativos de la FDA, se envía una CRL al solicitante, que incluye las deficiencias identificadas durante su evaluación.
A continuación se presenta una descripción figurativa de lo que un solicitante puede hacer en el plazo de un año tras recibir el CRL:
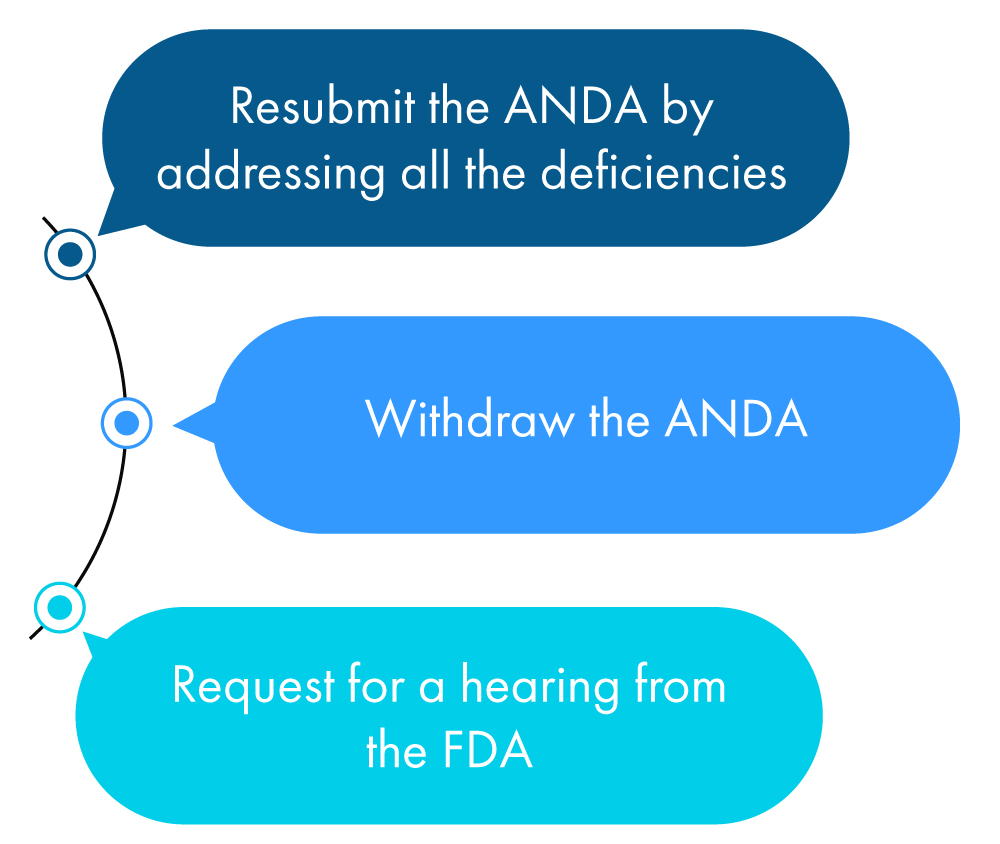
Si el solicitante no toma ninguna de las acciones anteriores, la FDA lo considera una solicitud para retirar la ANDA, a menos que el solicitante haya solicitado una prórroga para verificar todas las discrepancias mencionadas en la CRL.
¿Qué sucede después de un (01) año de la emisión de la CRL?
La FDA envía una notificación por escrito de que el solicitante tiene treinta (30) días a partir de la notificación para lo siguiente:
- Indique las razones por las que la ANDA no debería ser retirada
- Solicitud de prórroga para abordar todas las deficiencias mencionadas en la CRL
Una vez que la FDA recibe una solicitud de prórroga del solicitante, considera varios factores como se menciona a continuación y, posteriormente, decide sobre la solicitud:
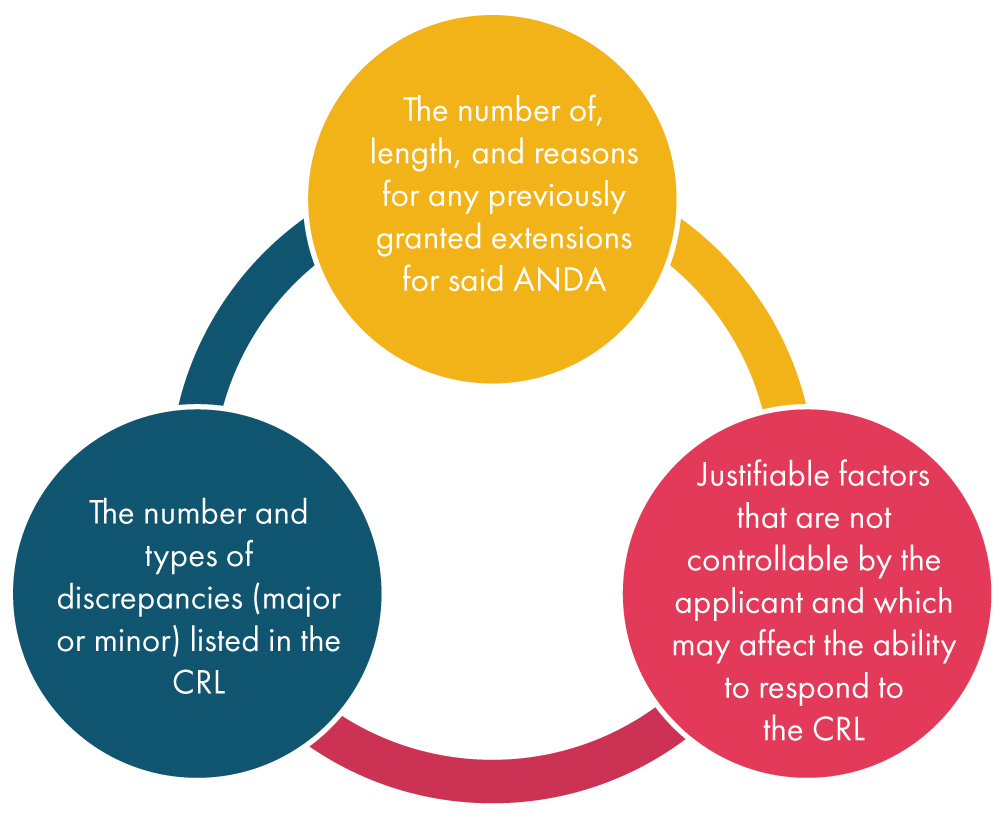
¿Qué es una enmienda?
El solicitante debe presentar una solicitud de prórroga para responder a un CRL a través de una enmienda. La FDA clasifica una enmienda como mayor o menor según el efecto que tenga en el proceso de aprobación.
Recomendaciones vitales de la FDA que los solicitantes deben conocer:
- La FDA reclasificará una enmienda menor como una mayor si la enmienda se presenta después de un año de la CRL, a menos que la ANDA sea para un producto en la lista de escasez de medicamentos según la sección 506E de la Ley FD&C (21 U.S.C. 356e), o sea objeto de una respuesta a una Emergencia de Salud Pública según lo declarado por el Secretario del Departamento de Salud y Servicios Humanos de los US según la sección 319 de la Ley de Servicio de Salud Pública (42 U.S.C. 247d), o se anticipe que estará sujeta a los mismos criterios que se aplican a dicha declaración, en el momento de la presentación.
- Si el solicitante no aborda las discrepancias en el CRL dentro del período extendido otorgado por la FDA, esta última puede considerar retirar la ANDA.
- Si el solicitante necesita más del período de extensión de treinta (30) días, puede solicitar una extensión adicional. La enmienda debe incluir entonces nueva información que permita a la FDA determinar si la extensión puede ser concedida o no.
Recibir una CRL de la FDA puede ser bastante desalentador para los solicitantes de ANDA. Desde abordar las discrepancias hasta citar las razones/información correctas para una extensión, todos los requisitos relevantes deben cumplirse para asegurar una aprobación más rápida del medicamento. Freyr es un experto reglamentario probado con amplio conocimiento en la respuesta a las CRL y en asegurar el cumplimiento de los requisitos de la FDA. Contáctenos ahora para obtener soporte estratégico End-to-End (de principio a fin) en las presentaciones de ANDA.










