
La comunicación efectiva siempre ha garantizado la seguridad y la calidad de la atención a los pacientes. A lo largo de los años, sigue existiendo la necesidad insatisfecha de proporcionar traducciones de etiquetas a personas que no dominan el inglés. La demanda de etiquetas de productos en múltiples idiomas regionales ha crecido exponencialmente a medida que los fabricantes farmacéuticos buscan impulsar el cambio hacia la localización y una mejor comunicación.
Satisfacer estas demandas mejorará la seguridad del paciente al tiempo que permite el cumplimiento de los requisitos normativos específicos de cada país. La ausencia de información médica importante en los documentos regionales supone una carga adicional para los farmacéuticos y profesionales de la salud a la hora de superar la barrera del idioma.
La Autoridad Reguladora de Productos Sanitarios (HPRA) supervisa el cumplimiento reglamentario en Irlanda. La HPRA facilita y trabaja conjuntamente con las partes interesadas adhiriéndose a la guía de mejores prácticas sobre etiquetado multilingüe publicada por el Grupo de Coordinación para el Reconocimiento Mutuo y los Procedimientos Descentralizados – Humano (CMDh). Además, la HPRA también flexibilizó ciertas condiciones de etiquetado, que incluyen:
- Uso de mL en Irlanda (IE) frente a ml en otros estados de la UE.
- Uso de puntos decimales en el volumen o la concentración del producto y un punto en Irlanda frente a una coma en la UE. Los fabricantes de medicamentos pueden superar esta discrepancia agrupando el nombre inventado, la concentración y la forma farmacéutica como una sola unidad en cada idioma.
- Uso de separador en la concentración o volumen del producto: un punto en la UE frente a una coma en IE. Se permite el uso de comas como separador en el envase exterior inmediato para evitar cualquier riesgo de confusión en la población de pacientes irlandesa.
- Las unidades de envasado primario pequeñas, es decir, envases con un tamaño inferior o igual a 50 ml, tienen una limitación de espacio y pueden incluir la información mínima requerida en ellos, siempre que esté justificado, para más de dos (02) idiomas.
- Información de terceros países: donde las condiciones de la información del producto son similares en el Reino Unido e Irlanda, los envases multicountry son aceptables. Los requisitos adicionales específicos de cada país se colocan en un 'recuadro azul'.
- Coordinación de la evaluación con los demás Member States - Las evaluaciones de maquetas realizadas por los Member States aseguran el cumplimiento del etiquetado. Los solicitantes pueden coordinar con los Member States para obtener claridad sobre los cambios requeridos antes de las presentaciones a la HPRA.
- Nombres conjuntos - La propuesta de nombre inventado a los Member States debe ser comunicada a la HPRA.
La HPRA presenta Sugerencias Adicionales para el Etiquetado Multilingüe, como sigue:
- La información mencionada en inglés debe agruparse en un bloque.
- Mencionar los requisitos de la "caja azul" para todos los países en el mismo panel, siempre que varios países compartan un mismo envase.
- La información dirigida a los pacientes irlandeses debe indicarse claramente en un código ovalado.
- Los solicitantes pueden incluir una sección perforada en el envase, siempre que los datos extraíbles no estén en inglés. Esto debe mencionarse en la presentación.
- Los solicitantes deben presentar un PDF del prospecto a la HPRA al final del proceso para actualizarlo en el sitio web.
Criterios para un envase multilingüe:
- El nombre del producto y su concentración deben ser los mismos en todos los idiomas.
- La información del etiquetado y del prospecto debe estar de acuerdo con los Resúmenes de las Características del Producto (SmPC).
- La información impresa en el etiquetado y el prospecto debe ser precisa y legible.
- La situación legal del medicamento debe ser similar en ambos países.
Un ejemplo de empaque multilingüe sería:
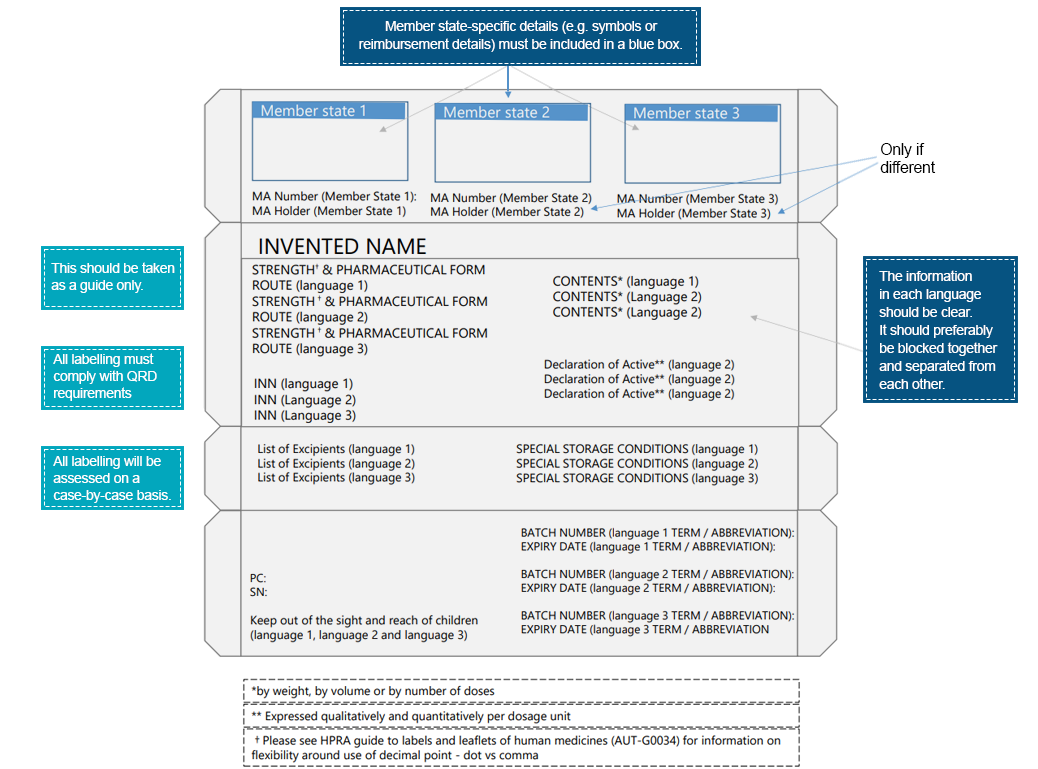
Los pacientes interactúan con las etiquetas de los medicamentos mucho antes de interactuar con el producto farmacéutico. Estas interacciones resaltan aún más la importancia de transmitir información esencial a través de varios elementos en la etiqueta del medicamento. Para garantizar una mejor legibilidad y la mejora de los elementos de la etiqueta, las empresas farmacéuticas deben tomar las medidas necesarias. Los idiomas regionales proporcionan un medio para transmitir instrucciones médicas relevantes para el producto farmacéutico que prometen el uso seguro y eficaz del producto prescrito. Expertos reglamentarios específicos de cada país pueden ayudar con la traducción de la información de etiquetado en cumplimiento con las regulaciones locales/regionales. Los expertos de Freyr están bien equipados para proporcionar asistencia para cerrar las brechas entre la información médica y el idioma. Contáctenos para obtener una vía de etiquetado conforme a la normativa.










