
La publicidad farmacéutica, incluida la publicidad directa al consumidor, está regulada por la Oficina de Promoción de Medicamentos Recetados (OPDP) de la Administración de Alimentos y Medicamentos de los Estados Unidos (US FDA), la Subdivisión de Etiquetado Publicitario y Promocional (APLB) del Centro de Evaluación e Investigación de Medicamentos (CDER), y el Centro de Evaluación e Investigación de Productos Biológicos (CBER) respectivamente. La información presentada a la OPDP y a la APLB debe ser precisa, ética y no engañosa. Debe incluirse información adicional sobre los beneficios y riesgos del producto en la presentación. Las Oficinas también revisan los materiales promocionales presentados a la Agencia.
En abril de 2022, la US FDA publicó una guía sobre las presentaciones de etiquetado y material publicitario promocional. La guía ayuda a comprender la presentación electrónica en el Módulo 1 del eCTD, utilizando la versión 3.3 o superior del archivo troncal regional de US. En el documento se enumeran los tipos de materiales promocionales no sujetos a la presentación electrónica obligatoria según la sección 745A. Se aceptarán copias en papel de todos los tipos de presentación promocional hasta veinticuatro (24) meses después de la publicación de la guía.
Excepción
El documento establece que las presentaciones bajo la sección 505(b), (i) o (j) de la Ley Federal de Alimentos, Medicamentos y Cosméticos (FD&C Act) y las presentaciones bajo la sección 47 351(a) o (k) de la Ley de Servicios de Salud Pública (PHS Act) deben presentarse en formato electrónico según lo definido por la FDA. Este documento no está sujeto a las restricciones habituales de las regulaciones de buenas prácticas de orientación de la FDA, ya que no establece legalmente responsabilidades exigibles. Por lo tanto, la parte de esta guía que establece el requisito de presentaciones electrónicas bajo la sección 745A(a) de la FD&C Act tiene un efecto vinculante, como lo indica el uso de las palabras "debe", "será" o "requerido".
La FDA revisa el material promocional redactado en un plazo de cuarenta y cinco (45) días a partir de la presentación voluntaria por parte de los patrocinadores. Para cualquier consulta relacionada con el producto planteada por profesionales de la salud, consumidores, patrocinadores de medicamentos o bufetes de abogados, la OPDP concede a los patrocinadores un plazo de treinta (30) días naturales para acusar recibo de la misma.
Definición de Material Promocional
La expresión "material promocional" se refiere al etiquetado promocional y a los materiales publicitarios, independientemente del formato, la forma o el medio a través del cual se comuniquen. La FDA generalmente supervisa dos (02) tipos de etiquetado para medicamentos:
- Etiquetado exigido por la FDA
- Etiquetado promocional.
Según la sección 201(m) de la FDA, el etiquetado se define como “todas las etiquetas, además de las escritas, impresas o gráficas en relieve en cualquier envase, envoltorio o en cualquier artículo o que acompañen a dicho artículo”. El lenguaje utilizado en ‘que acompañen a dicho artículo’ se considera una interpretación o explicación del material promocional, según lo declarado por la Corte Suprema de los US.
Criterios para la presentación de material promocional para revisión
- Inclusión de números adecuados de NDA, ANDA o BLA
- En los casos en que los solicitantes requieran una revisión inmediata, dirijan las presentaciones al Gerente de Proyecto de OPDP.
- Del formulario FDA 2253, asigne el tipo de material más específico para representar el material promocional
- Diferentes tipos de materiales deben presentarse por separado
- No mezcle otras presentaciones con material promocional
- El material promocional dirigido a profesionales de la salud debe presentarse por separado del que se dirige a los consumidores.
Las métricas siguientes aclaran el recuento de los formularios 2253 presentados y los materiales incluidos en estas presentaciones.
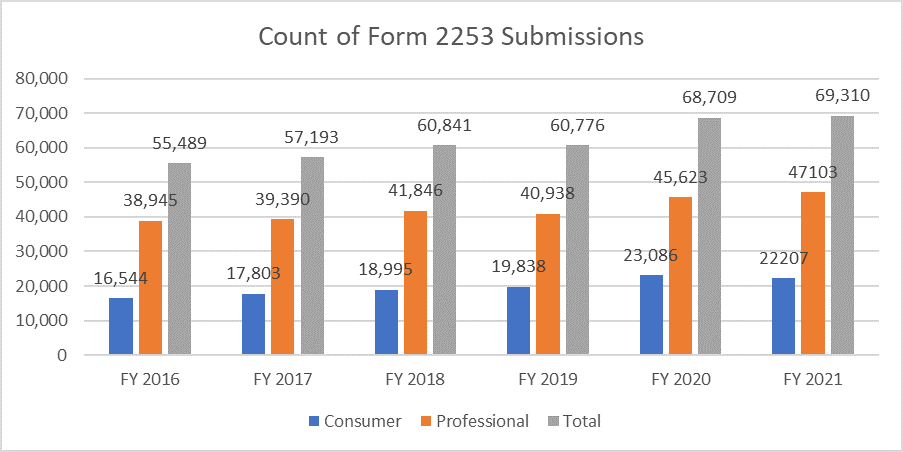
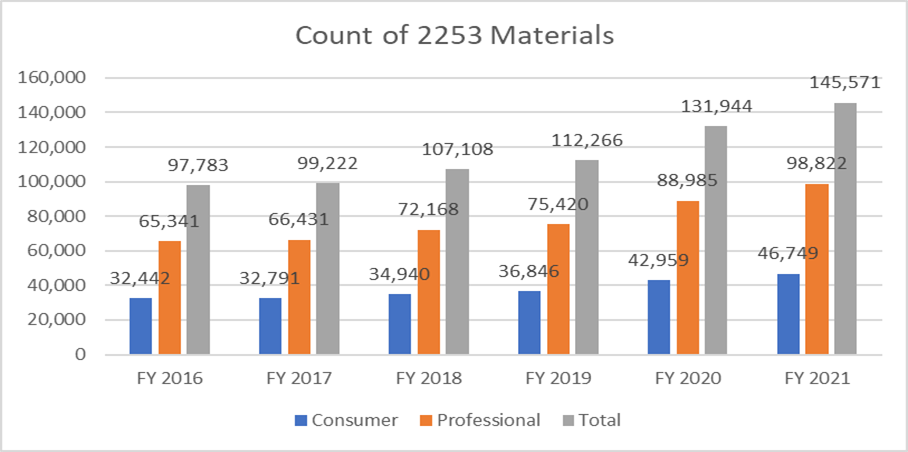
Es de suma importancia que los patrocinadores elaboren su material promocional según la guía proporcionada por la FDA para evitar múltiples ciclos de revisión, dado el costo del proceso. Contar con recursos que puedan ayudar a facilitar el proceso de envío de material promocional sin problemas puede permitir a los patrocinadores alcanzar sus objetivos comerciales y mantenerse al día con los requisitos reglamentarios. Un socio reglamentario probado como Freyr puede garantizar una revisión completa del material promocional y no promocional antes de la presentación, ya sea en formato electrónico o no electrónico. Contacte con Freyr hoy para elaborar material promocional claro, conciso y conforme a la primera.










