
Introducción
El auge de los biofármacos ha sido una verdadera revolución en el ámbito de las ciencias de la vida. Estos fármacos complejos de moléculas grandes han transformado el panorama de la atención médica, ofreciendo tratamientos dirigidos y eficaces para una variedad de enfermedades. A medida que los biofármacos siguen aumentando, la Administración de Alimentos y Medicamentos de los Estados Unidos (US FDA) desempeña un papel fundamental para garantizar su seguridad y eficacia.
En este blog, profundizamos en el notable ascenso de los biofarmacéuticos y obtenemos información sobre la perspectiva de la FDA de US sobre este campo transformador. Además, comprendemos el papel crucial de los proveedores reglamentarios para navegar las complejidades de la regulación biofarmacéutica.
Revolución de los productos biofarmacéuticos
Debido al auge en investigación y desarrollo, la industria biofarmacéutica ha experimentado un crecimiento notable. A diferencia de los fármacos tradicionales de molécula pequeña, los biofármacos se derivan de organismos vivos o procesos biológicos, incluyendo proteínas, ácidos nucleicos y células. Estas moléculas grandes y complejas ofrecen varias ventajas, como una alta especificidad y efectos secundarios reducidos, lo que los hace ideales para tratar una variedad de enfermedades, desde el cáncer hasta los trastornos autoinmunes.
El papel en evolución de la FDA
A medida que la industria biofarmacéutica florece, la FDA de US ha adaptado su enfoque reglamentario para adaptarse a estas terapias innovadoras. La perspectiva de la agencia refleja un compromiso con la facilitación de la innovación, manteniendo al mismo tiempo los más altos estándares de seguridad del paciente.
- Equilibrar la innovación y la seguridad:
Uno de los principales desafíos que enfrenta la FDA al regular los biofarmacéuticos es encontrar el delicado equilibrio entre fomentar la innovación y salvaguardar el bienestar del paciente. El desarrollo biofarmacéutico puede ser largo y costoso, y los procesos reglamentarios deben ser ágiles para seguir el ritmo de los avances científicos.
- Vías reglamentarias para biofármacos:
La FDA ofrece diversas vías normativas adaptadas a las características únicas de los productos biofarmacéuticos. Esto incluye vías para biosimilares, que son similares pero no idénticos a los productos biofarmacéuticos ya aprobados, y programas de revisión acelerada para terapias innovadoras que muestran una promesa significativa en el tratamiento de enfermedades graves.
- Garantizar la calidad y eficacia:
La perspectiva de la FDA sobre los biofármacos se extiende a garantizar la calidad y eficacia de estos tratamientos. La fabricación de biofármacos es muy compleja y exige un control de calidad riguroso. La FDA colabora estrechamente con los fabricantes para establecer y mantener altos estándares, incluidos procesos y controles robustos para minimizar las variaciones en los productos farmacéuticos.
- Seguimiento de la seguridad y Vigilancia Post-Comercialización:
Más allá de la aprobación inicial, el papel de la FDA en el monitoreo de la seguridad y eficacia de los biofármacos continúa post-comercialización. Esto incluye la notificación de eventos adversos, inspecciones y evaluaciones de seguridad continuas para identificar y abordar riesgos potenciales. La perspectiva de la agencia está firmemente arraigada en el compromiso de asegurar que los beneficios de los biofármacos sigan superando cualquier riesgo.
- Mantenimiento de enfoques centrados en el paciente:
La perspectiva de la US FDA está en consonancia con la tendencia de la industria hacia una atención médica centrada en el paciente. Fomenta la participación de las comunidades de pacientes y las partes interesadas en el proceso reglamentario, asegurando que la voz del paciente sea escuchada y que sus necesidades sean consideradas en la evaluación de los productos biofarmacéuticos.
- Fomentar la colaboración global:
El auge de los biofármacos ha trascendido las fronteras nacionales. La FDA colabora activamente con agencias reglamentarias internacionales para establecer directrices armonizadas para el desarrollo biofarmacéutico y la aprobación de estas terapias. Estas colaboraciones ayudan a agilizar el desarrollo global de biofármacos, haciendo que estos tratamientos innovadores sean accesibles a una población de pacientes más amplia.
Papel de los proveedores reglamentarios
Los proveedores reglamentarios pueden actuar como socios estratégicos en la era de los biofarmacéuticos, ayudando a las empresas farmacéuticas a navegar por el complejo panorama:
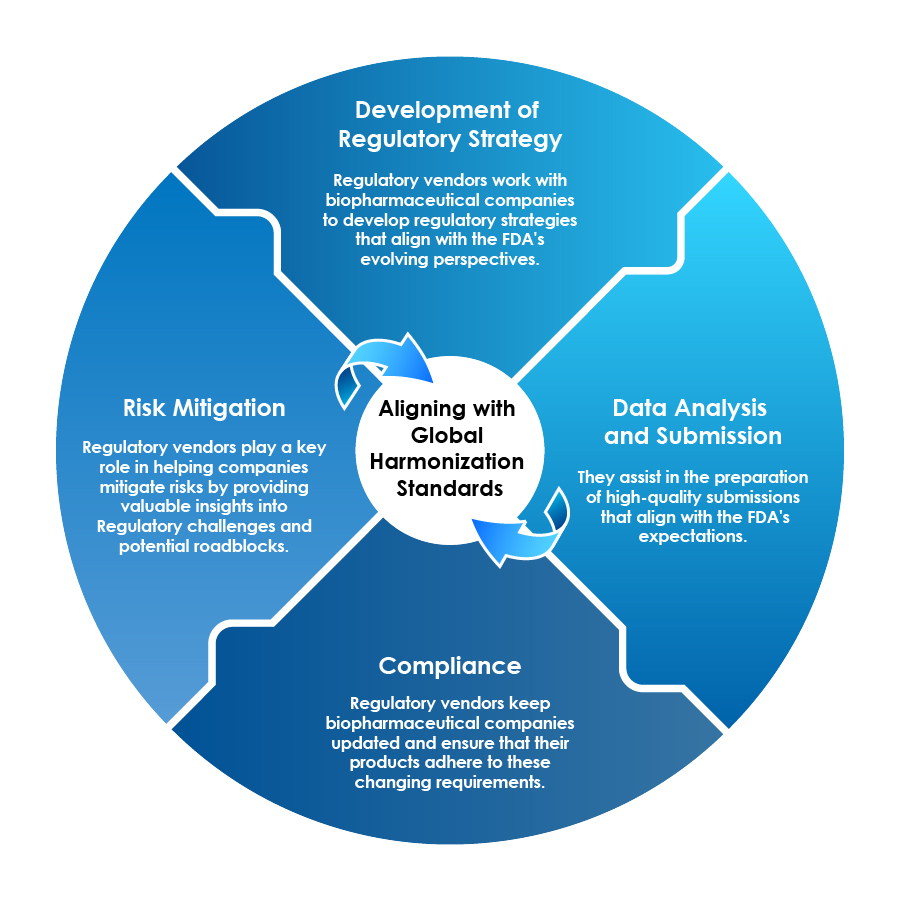
Los proveedores de servicios reglamentarios aseguran la alineación con los estándares globales.
Conclusión
El auge de los productos biofarmacéuticos representa un cambio monumental en la atención médica, al ofrecer tratamientos dirigidos y efectivos para diversas enfermedades. La perspectiva de la FDA muestra una adaptación e innovación continuas en los enfoques reglamentarios hacia el desarrollo biofarmacéutico. Además, los proveedores reglamentarios, actuando como socios cruciales, aseguran que las empresas biofarmacéuticas naveguen con éxito por el intrincado panorama, facilitando el camino desde la innovación hasta la disponibilidad en el mercado.
La sinergia entre la FDA y los proveedores reglamentarios permite a la industria satisfacer las demandas cambiantes de la atención al paciente e impulsar un futuro de innovaciones biofarmacéuticas pioneras. Nuestros expertos en Freyr están bien versados en el manejo de tales imperativos reglamentarios; contáctenos para obtener más información.










