
A la mayoría de las organizaciones de ciencias de la vida les resulta difícil optimizar su proceso de presentaciones reglamentarias debido a los cambios frecuentes en las directrices de presentación. Según un análisis reciente realizado por la Administración de Alimentos y Medicamentos de US (USFDA), el 32% de las presentaciones con datos de estudio tuvieron problemas críticos de conformidad de datos. El proceso requiere una comprensión profunda de la colaboración entre las partes interesadas internas y externas. Dentro de la organización, los departamentos de fabricación, investigación y desarrollo, investigación clínica/no clínica, QA/QC, marketing y ventas deben trabajar en armonía para acelerar el proceso de aprobación desde el desarrollo inicial hasta que el medicamento llega al mercado. El departamento de Asuntos Regulatorios y las Autoridades Sanitarias (HA) están en constante correspondencia para garantizar y evaluar la seguridad y eficacia de los medicamentos para uso humano. Veamos qué medidas preliminares deben tomar las organizaciones farmacéuticas para establecer la excelencia en las presentaciones reglamentarias:
Asignar y desplegar recursos para agilizar, estandarizar y acelerar las presentaciones desorganizadas.
Un especialista en presentaciones participa de forma contractual y puede comprender más de un (01) tipo de presentación, mientras ha estado asociado a programas de desarrollo a lo largo de los años, ayudando a elaborar narrativas convincentes para el expediente. Hacerlo facilita a las organizaciones:
- Eliminar errores equilibrando la colaboración entre las partes interesadas internas y externas
- Reducir el ciclo de revisión de la HA del proceso de creación y aprobación de documentos
- Establecer expedientes completos y conformes para cumplir con los requisitos reglamentarios cambiantes de los diferentes mercados.
- Confirmar las presentaciones afectadas por una Autoridad Reguladora
- Estar al tanto del estado de la elaboración, revisión y aprobación de las presentaciones.
- Mejora del protocolo de presentación actual.
Simplifique la metodología de presentación de expedientes
La elaboración de un expediente es fundamental para la preparación de las presentaciones. Se observa que las Solicitudes de Licencia de Productos Biológicos (BLAs) y las Solicitudes de Nuevos Fármacos (NDAs) contienen muchísimas páginas, lo que dificulta a los reguladores comprender la narrativa del expediente. Contar con una representación estructurada de una idea general puede mejorar la capacidad del equipo para preparar las presentaciones y la de las agencias para revisarlas.
El uso de módulos para agilizar las presentaciones permite a los expertos analizar qué debe incluirse en cada sección o módulo del expediente. Dicha práctica facilita:
- Inicio temprano de la redacción acelerando la preparación de la presentación de la organización
- Uso de datos relevantes requeridos para la elaboración de los envíos
- Uso de recursos adecuados sin la necesidad de redactar documentos extensos desde cero para cada envío
Trabajar en colaboración con las Autoridades Reglamentarias
Toda organización debe realizar reuniones periódicas con las Autoridades Sanitarias (AA.SS.) como práctica durante la etapa temprana del desarrollo del producto. Esto asegura una revisión y retroalimentación oportunas, lo que resulta en una resolución acelerada de los comentarios por parte de la AA.SS. y, en consecuencia, del proceso de aprobación. No solo fomenta una buena relación entre las organizaciones y la AA.SS., sino que también ayuda a obtener claridad en una etapa temprana de la planificación de la presentación.
Optimizar el contenido y los datos en el Sistema de Gestión Documental (DMS)
Se espera que un sólido repositorio de contenido gestione todos los datos de las diferentes áreas funcionales, incluida la documentación e información creada previamente. Un repositorio de contenido y datos estructurados proporciona acceso sin interrupciones a los documentos de diversas áreas funcionales sin esfuerzo adicional ni necesidad de duplicación. Los documentos almacenados en el DMS se convierten en la única fuente de información para todas las partes interesadas internas (ciencia clínica, CMC, no clínica, farmacocinética, farmacodinámica, redacción médica y operaciones clínicas). Dicho contenido y datos pueden utilizarse para crear contenido local basado en los requisitos regionales. Optimización de los envíos reglamentarios mediante la gestión estructurada de contenido y datos
Adoptar tecnología y automatización para reducir el trabajo repetitivo y los errores
Las organizaciones pueden utilizar la tecnología aprovechando su función de actualización automática y control de calidad de las tablas, listados y figuras (TLF) en el texto con respecto a los datos de origen para acelerar el proceso de documentación. De esta manera, cada vez que se realizan cambios en las tablas de origen existentes, se actualizan las TLF en el texto. Esto ayuda a eliminar horas de trabajo en general, ahorrar tiempo en la ruta crítica y mejorar la precisión de los datos.
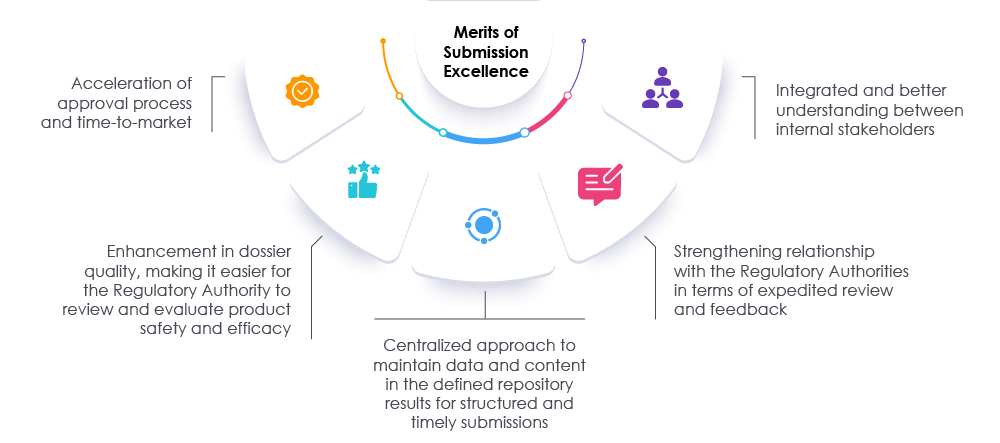
La adopción de medidas adecuadas junto con revisiones oportunas de los expedientes y los datos puede ayudar tanto a los organismos reguladores como a las organizaciones a acelerar el proceso de presentación. Este enfoque acelera el tiempo de comercialización para satisfacer las necesidades tanto de los pacientes como de la industria. Un socio reglamentario probado puede ayudar a las organizaciones a replantear, reevaluar y modificar los enfoques actuales para la preparación de las presentaciones. Nuestros expertos en Freyr pueden facilitar un camino hacia la excelencia en las presentaciones reglamentarias aumentando la visibilidad en toda la organización y promoviendo el cumplimiento general, lo que permite a la organización tener éxito en el mercado actual de las ciencias de la vida. Consulte a Freyr.










