
Nel settore della produzione di dispositivi medici, in continua evoluzione e altamente regolamentato, garantire la qualità dei prodotti e la sicurezza dei pazienti non è solo un obbligo legale, ma anche un imperativo strategico. Sistemi efficaci di gestione dei reclami e di vigilanza, conformi alla norma ISO 13485:2016, costituiscono la colonna portante di qualsiasi Sistema di Gestione della Qualità (SGQ) solido. Questi meccanismi assicurano la conformità alle normative internazionali e rafforzano la fiducia dei clienti e la credibilità del marchio.
Vediamo in che modo la gestione dei reclami e la vigilanza svolgono un ruolo fondamentale nel garantire la qualità e la conformità normativa nel settore dei dispositivi medici, con approfondimenti in linea con ISO 13485:2016 e supportati dai quadri normativi internazionali.
Comprendere la gestione dei reclami secondo ISO 13485:2016
ISO 13485:2016 definisce un reclamo come qualsiasi comunicazione scritta, orale o elettronica che segnali difetti relativi all'identità, alla qualità, alla durata, all'affidabilità, all'usabilità, alla sicurezza o alle prestazioni di un dispositivo medico. Tale norma richiede alle aziende produttrici di dispositivi medici di stabilire procedure documentate per la gestione dei reclami, comprese la valutazione, l'indagine e la risoluzione degli stessi, nell'ambito di un efficace sistema di gestione della qualità.
Un sistema di gestione dei reclami è fondamentale per garantire la conformità, mantenere la soddisfazione dei clienti e migliorare la qualità dei dispositivi. Il processo deve essere organizzato e tracciabile, e comprendere le seguenti fasi:
- Ricezione e documentazione dei reclami
Tutti i reclami devono essere registrati senza indugio, fornendo il maggior numero possibile di dettagli riguardo alla natura del problema, alle specifiche e al modello del dispositivo, alle condizioni di utilizzo e alle eventuali conseguenze subite dall'utente o dal paziente. - Valutazione dell'obbligo di segnalazione
Una volta registrati, i reclami devono essere valutati per stabilire se si tratti di incidenti soggetti a segnalazione. Ad esempio, negli Stati Uniti, produttori di dispositivi medici produttori tenuti a segnalare determinati problemi relativi ai dispositivi nell'ambito del sistema di segnalazione dei dispositivi medici (MDR) regolamentato dalla FDA. I produttori devono attenersi alle norme vigenti in materia di tempistiche di segnalazione. - Indagine e analisi delle cause profonde
In caso di reclami fondati, è necessario procedere a un'indagine approfondita. Individuare la causa profonda è fondamentale per attuare azioni correttive e preventive (CAPA) efficaci. - Azioni correttive e preventive (CAPA)
Sulla base dei risultati relativi ai dispositivi medici, le aziende devono avviare azioni CAPA per risolvere sia il problema immediato che i casi di recidiva e per prevenire il ripetersi di tali eventi in futuro. - Circuito di retroazione e chiusura
Una volta risolto il problema, il reclamo dovrebbe essere formalmente chiuso con la documentazione completa e una comunicazione al reclamante, se applicabile per il dispositivo medico.
Vigilanza: un pilastro fondamentale della sorveglianza post-commercializzazione
La vigilanza consiste nel monitoraggio e nella segnalazione di eventi e incidenti avversi una volta che un dispositivo medico è stato immesso sul mercato. Ai sensi della ISO 13485:2016 e delle corrispondenti normative internazionali, questa sorveglianza continua è fondamentale per l'individuazione tempestiva di potenziali rischi e l'attuazione di interventi tempestivi.
Il sistema di vigilanza dell'Unione Europea, aggiornato in base al regolamento sui dispositivi medici (EU MDR), impone produttori di dispositivi medici produttori disporre di piani di sorveglianza post-commercializzazione. Tali piani devono includere procedure per la raccolta e l'analisi dei dati relativi all'utilizzo dei dispositivi nel mondo reale.
Analogamente, in India, Central Drugs Standard Control Organization CDSCO) disciplina le procedure di vigilanza e di gestione dei reclami relative ai dispositivi medici. Essa incoraggia la segnalazione di eventi avversi e di difetti dei prodotti al fine di migliorare costantemente la sicurezza e l'efficacia dei dispositivi medici.
Tra gli elementi fondamentali di un sistema di vigilanza efficace figurano:
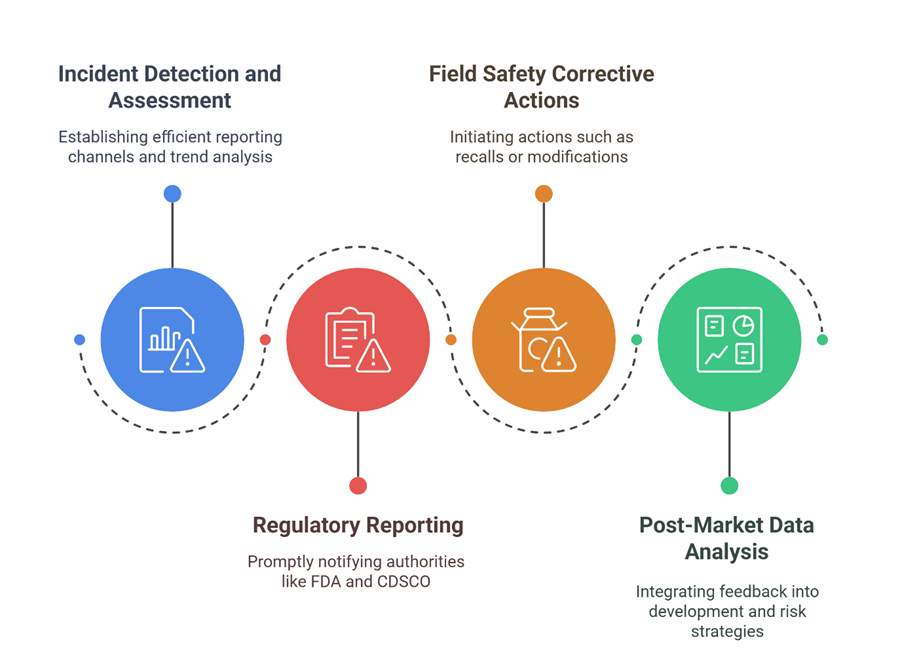
Sviluppo di una strategia integrata di gestione dei reclami e di vigilanza
produttori di dispositivi medici produttori migliorare il proprio sistema di gestione della qualità integrando la gestione dei reclami e la vigilanza in un unico sistema coerente. Ecco alcune buone pratiche:
Procedure operative standard (SOP) e definizioni dei ruoli chiare
Le procedure operative standard (SOP) dovrebbero descrivere le fasi relative alla ricezione, alla valutazione, alla segnalazione e alla risoluzione dei reclami. Esse definiscono chi è responsabile in ciascuna fase, al fine di evitare ritardi e lacune.
- Formazione e sensibilizzazione del personale
Una formazione regolare del personale garantisce che i dipendenti sappiano come identificare e gestire in modo efficace i reclami e gli eventi avversi. - Strumenti digitali e automazione
L'utilizzo di un software per la gestione della qualità (QMS) consente di semplificare il monitoraggio dei reclami, la documentazione e la rendicontazione. L'automazione migliora la tracciabilità e la conformità alla norma ISO 13485:2016. - Cultura della qualità e miglioramento continuo
Promuovere una filosofia che valorizzi il feedback incoraggia la segnalazione proattiva dei problemi e favorisce l'innovazione nel miglioramento della qualità.
Conformità e oltre: un vantaggio competitivo nel marketing
L'implementazione di sistemi conformi ISO 13485:2016 per la gestione dei reclami e la vigilanza non solo garantisce il rispetto delle normative, ma contribuisce anche a posizionare l'azienda come un'entità affidabile e attenta alla qualità. In un settore in cui la sicurezza e le prestazioni hanno un impatto diretto sulla vita delle persone, tale impegno può rivelarsi un potente strumento di marketing.
Secondo FDA l'allineamento agli standard internazionali migliora l'accesso ai mercati globali, rafforza la fiducia dei clienti e riduce il rischio di costosi richiami o contenziosi.
| Regione | Quadro Normativo | Numero di riferimento/Articolo relativo alla gestione dei reclami | Numero della clausola di riferimento / Articolo relativo alla vigilanza / Segnalazione di eventi avversi |
| Unione Europea | EU MDR 2017/745 | Articolo 83, allegato III (sistema PMS); articolo 10, paragrafo 9 | Articoli 87–92 (Sistema di vigilanza), Allegato III |
| Stati Uniti (FDA) | 21 CFR Parte 820 (QSR) | §820.198 – Fascicoli relativi ai reclami | 21 CFR Parte 803 – Segnalazione dei dispositivi medici (MDR) |
| India (CDSCO) | Regolamento sui dispositivi medici del 2017 (MDR) | Capitolo VII, Regole 25 e 26 | Capitolo VII, Regola 27 |
| A livello globale (norma ISO) | ISO 13485:2016 | Clausola 8.2.2 – Gestione dei reclami | Clausola 8.2.3 – Segnalazioni alle autorità di regolamentazione |
Conclusione
Nell'odierno panorama normativo, caratterizzato da una forte concorrenza nel settore dei dispositivi medici, l'efficacia dei sistemi di gestione dei reclami e di vigilanza è un requisito imprescindibile. In linea con ISO 13485:2016, questi processi non solo tutelano i pazienti, ma contribuiscono anche a costruire un marchio solido e attento alla propria reputazione. Investendo in procedure sistematiche, formazione continua e vigilanza post-commercializzazione, produttori trasformare i requisiti normativi in opportunità di crescita e leadership di mercato.










