
Un regime di terapia farmacologica è diversificato per i farmaci che possono essere approvati per l'uso in combinazione con un farmaco precedentemente approvato o per due nuovi farmaci sviluppati simultaneamente, che migliorano sinergicamente l'efficacia. Le terapie antitumorali con un singolo farmaco hanno evidenziato in modo significativo la resistenza ai farmaci come una minaccia importante per i pazienti sottoposti a trattamenti con farmaci antitumorali. Considerando la diversità della terapia combinata adottata per i trattamenti antitumorali, i regimi a due farmaci stanno gradualmente sostituendo la monoterapia come standard di cura nei pazienti. Nel corso del decennio, la terapia combinata ha offerto un migliore ambito di trattamento.
Se siete un'organizzazione ben consapevole del cambiamento di paradigma nello sviluppo di farmaci oncologici, dal singolo farmaco a nuove combinazioni, dovete sapere che questo progresso ha portato a un aumento delle richieste di concessione di richieste di cross-labeling da parte del richiedente. Riconoscendo le conversazioni, le ultime tendenze del settore e la sua attuale comprensione delle esigenze di uno sponsor, la US Food and Drug Administration (USFDA) ha concesso una serie di linee guida per fornire supporto con le modifiche all'etichettatura per i regimi farmacologici con prodotti farmaceutici precedentemente approvati.
Congratulazioni! La tua richiesta di guida per il cross-labeling è stata accolta, se:
(a) L'indicazione per il regime di combinazione richiesto è approvata con un'indicazione farmacologica simile.
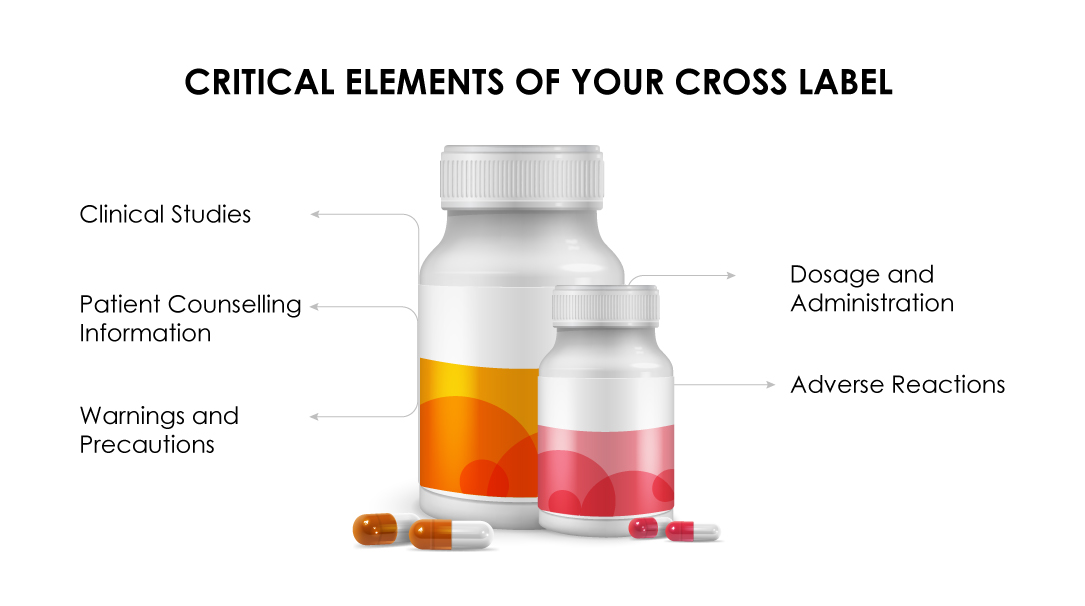
(b) La sezione Posologia e somministrazione deve evidenziare la posologia raccomandata per il farmaco dello sponsor in un regime di combinazione.
(c) I dati degli studi clinici devono giustificare i benefici della combinazione per tutti i farmaci del regime.
(d) La sezione «Avvertenze e precauzioni» deve indicare l'unicità del regime terapeutico combinato sulla base di dati clinicamente significativi.
(e) Le reazioni avverse devono essere evidenziate come osservato negli studi clinici.
(f) Il foglietto illustrativo destinato ai pazienti deve limitarsi alle tossicità specifiche della formulazione.
Le informazioni relative al solo farmaco dello sponsor devono occupare le sezioni rimanenti dell'etichetta, a meno che non sia necessario menzionare fattori farmacocinetici unici.
La guida approvata per il cross-labeling si rivolge specificamente ai prodotti per la terapia antitumorale per stabilire la comprensione fondamentale del cross-labeling. Per aiutare gli sponsor con gli ostacoli operativi e normativi relativi al cambio di etichetta, la guida afferma:
- Tempistiche
Ci si aspetta che i richiedenti propongano il contenuto della bozza per il cross-labeling con una giustificazione basata sull'evidenza del ruolo di ciascun prodotto menzionato nel regime, nella loro proposta per il cross-labeling di un nuovo farmaco antitumorale in una domanda pre-NDA o BLA.
Si prevede che l'etichettatura incrociata venga identificata per ogni farmaco sotto il regime di trattamento contemporaneamente. Tuttavia, l'approvazione può essere concessa una dopo l'altra, in sequenza, a causa della differenza nella tempistica del farmaco.
- Sottomissione Regolatoria
Ogni richiedente che cerca un'etichettatura incrociata deve presentare domanda tramite una domanda originale o un supplemento di efficacia per l'etichettatura incrociata.
Un richiedente può scegliere di fare riferimento ai dati di altre domande per giustificare i benefici sinergici del regime combinato.
Nel fare riferimento ai dati, il richiedente:
- deve garantire che i dati di riferimento incrociato siano già stati depositati dalla FDA.
- deve annotare ogni sezione dei dati del richiedente a cui si fa riferimento incrociato.
- dovrebbe includere (sezione sottostante) solo le informazioni pertinenti al farmaco del richiedente:
- AVVERTENZA CON RIQUADRO (Se applicabile)
- FORME FARMACEUTICHE E DOSAGGI
- CONTROINDICAZIONI
- INTERAZIONI CON ALTRI FARMACI
- USO IN POPOLAZIONI SPECIFICHE
- SOVRADOSAGGIO
- DESCRIZIONE
- FARMACOLOGIA CLINICA
- TOSSICOLOGIA NON CLINICA
- BIBLIOGRAFIA
- COME FORNITO/CONSERVAZIONE E MANIPOLAZIONE
L'etichettatura incrociata per i farmaci antitumorali può aiutare a informare la popolazione di pazienti su dosaggio, efficacia e vantaggi dei risultati del trattamento. Con un aumento esponenziale della terapia di combinazione come metodo standard, le etichette incrociate possono rivelarsi utili nel miglioramento o nell'introduzione di metodi terapeutici attuali. I nostri esperti di Freyr sono ben preparati nelle sfide dell'etichettatura dinamica e possono fornire soluzioni alle vostre domande sull'etichettatura. Sperimentate il supporto professionale per l'etichettatura al suo meglio. Contattate Freyr!










