
Una comunicazione efficace ha sempre garantito la sicurezza e la qualità dell'assistenza ai pazienti. Nel corso degli anni, rimane un'esigenza insoddisfatta di fornire traduzioni delle etichette a individui che non parlano fluentemente l'inglese. La domanda di etichette di prodotto in più lingue regionali è cresciuta esponenzialmente, poiché i produttori farmaceutici intendono promuovere il cambiamento verso la localizzazione e una migliore comunicazione.
Soddisfare queste richieste migliorerà la sicurezza dei pazienti, consentendo al contempo la conformità ai requisiti normativi specifici di ciascun paese. L'assenza di importanti informazioni mediche nelle lingue regionali impone un onere aggiuntivo ai farmacisti e agli operatori sanitari per superare la barriera linguistica.
L'Autorità Regolatoria per i Prodotti Sanitari (HPRA) è responsabile della conformità normativa in Irlanda. L'HPRA facilita e collabora con le parti interessate aderendo alle linee guida sulle migliori pratiche per l'etichettatura multilingue rilasciate dal Gruppo di Coordinamento per le Procedure di Mutuo Riconoscimento e Decentrate – Umane (CMDh). Inoltre, l'HPRA ha anche allentato alcune condizioni di etichettatura, che includono:
- Uso di ML in Irlanda (IE) rispetto a ML in altri stati dell'UE.
- Uso dei punti decimali nel volume o nella concentrazione del prodotto e un punto in Irlanda (IE) rispetto a una virgola nell'UE. I produttori di farmaci possono superare questa discrepanza raggruppando il nome inventato, la concentrazione e la forma farmaceutica come un'unica unità in ogni lingua.
- Utilizzo del separatore nella concentrazione o nel volume del prodotto - Un punto nell'UE rispetto a una virgola in Irlanda. L'uso delle virgole come separatore è consentito sull'imballaggio esterno immediato per evitare qualsiasi rischio di confusione nella popolazione di pazienti irlandesi.
- Le piccole unità di imballaggio primario, ovvero i contenitori con dimensioni inferiori o uguali a 50 ml, hanno un vincolo di spazio e possono contenere le informazioni minime richieste su di essi, ove giustificato, per più di due lingue.
- Informazioni sul paese terzo – laddove le condizioni delle informazioni sul prodotto siano simili nel REGNO UNITO e in Irlanda, sono accettabili confezioni multi-paese. Requisiti aggiuntivi specifici per paese sono inseriti in una “casella blu”.
- Coordinamento della valutazione con gli altri Member States - Le valutazioni di mock-up effettuate dai Member States garantiscono la conformità dell'etichettatura. I richiedenti possono coordinarsi con i Member States per ottenere chiarezza sulle modifiche richieste prima delle presentazioni all'HPRA.
- Nomi congiunti - La segnalazione del nome inventato proposto ai Member States deve essere comunicata all'HPRA.
L'HPRA propone ulteriori suggerimenti per l'etichettatura multilingue come segue:
- Le informazioni menzionate in inglese devono essere raggruppate in un blocco.
- Menzionare i requisiti "blue-box" per tutti i paesi sullo stesso pannello, laddove più paesi condividano una confezione.
- Le informazioni destinate ai pazienti irlandesi devono essere chiaramente indicate in un codice ovale.
- I richiedenti possono includere una sezione perforata sulla confezione, a condizione che i dati rimovibili non siano in inglese. Ciò deve essere menzionato nella domanda.
- I richiedenti devono presentare un PDF del foglietto illustrativo all'HPRA al termine del processo per il suo aggiornamento sul sito web.
Criteri per un pacchetto multilingue:
- Il nome del prodotto e la sua concentrazione devono essere gli stessi in tutte le lingue.
- Le informazioni sull'etichettatura e sul foglietto illustrativo devono essere conformi ai Riassunti delle Caratteristiche del Prodotto (SmPC).
- Le informazioni stampate sull'etichettatura e sul foglietto illustrativo devono essere accurate e leggibili.
- Lo status legale del farmaco deve essere simile in entrambi i paesi.
Un esempio di confezionamento multilingue sarebbe:
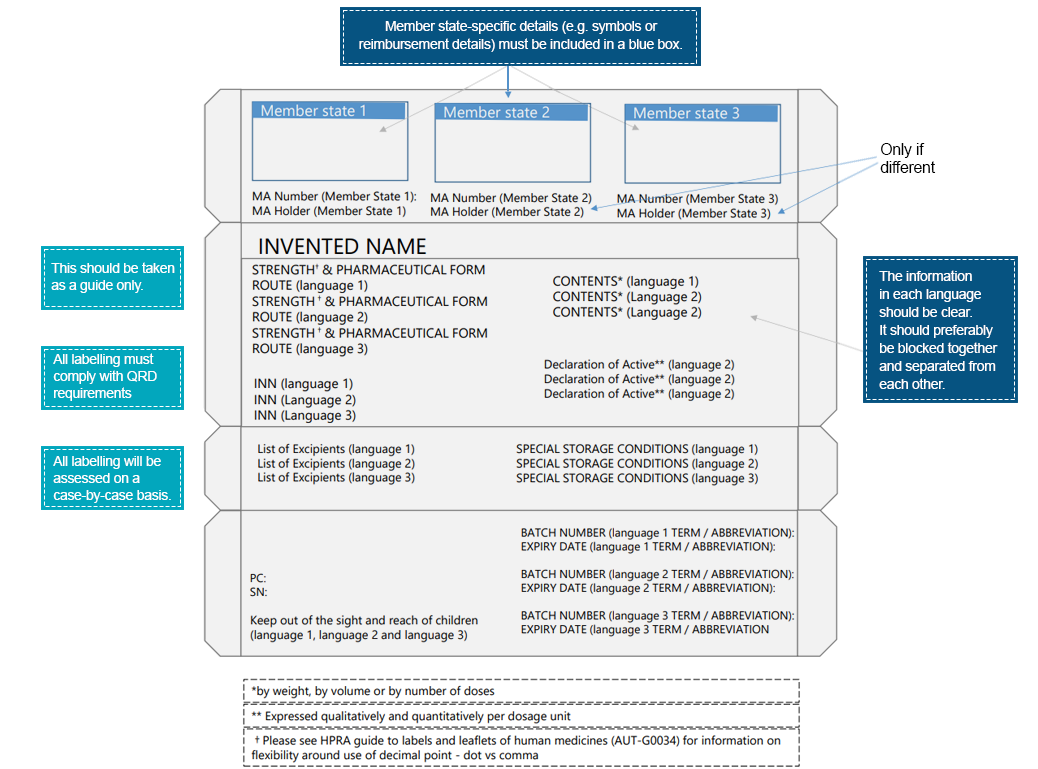
I pazienti interagiscono con le etichette dei farmaci molto prima di interagire con il prodotto farmaceutico stesso. Tali interazioni sottolineano ulteriormente l'importanza di trasmettere informazioni essenziali attraverso i vari elementi dell'etichetta del farmaco. Per garantire una migliore leggibilità e un miglioramento degli elementi dell'etichetta, le aziende farmaceutiche devono adottare le misure necessarie. Le lingue regionali offrono un mezzo per trasmettere istruzioni mediche pertinenti al prodotto farmaceutico che garantiscono l'uso sicuro ed efficace del prodotto prescritto. Esperti normativi specifici per paese possono assistere nella traduzione delle informazioni di etichettatura in conformità con le normative locali/regionali. Gli esperti Freyr sono ben attrezzati per fornire assistenza nel colmare le lacune tra le informazioni mediche e il linguaggio. Contattateci per un percorso di etichettatura conforme.










