
A Hong Kong, il processo di approvazione per i farmaci orfani destinati a malattie rare, in particolare quelli contenenti Nuove Entità Chimiche o Biologiche (NCEs) per malattie potenzialmente letali o gravemente debilitanti, è gestito dal Pharmacy and Poisons Board di Hong Kong. Di seguito è riportata una guida passo-passo per affrontare il processo:
Guida dettagliata all'approvazione dei farmaci orfani per le malattie rare
Preparazione e presentazione
Preparare la domanda allegando i documenti essenziali:
- Relazioni di valutazione degli esperti e documenti CTD sulla sicurezza, efficacia e qualità
- Piani di gestione del rischio (RMP)
- Etichette dei prodotti e foglietti illustrativi
- Relazioni di valutazione del rischio di impurità elementari
- Record mondiale di iscrizioni
Presentare la domanda di registrazione tramite il Pharmaceuticals Registration System 2.0 (PRS 2.0) sul sito web del Drug Office. Questo è un primo passo fondamentale per coloro che registrano farmaci orfani per malattie rare a Hong Kong.
Pagamento delle tariffe
Pagare la tassa di iscrizione tramite:
- PRS 2.0 (online) – tramite carta di credito o PPS
- Di persona – in contanti o con assegno presso l'Ufficio Farmaci
- Screening e Valutazione
- Il Drug Office esamina tutti i documenti presentati prima di accettare la domanda per la valutazione.
- Se i documenti sono incompleti, verrà emessa una lettera di carenza.
- Meccanismo di Rifiuto della Presentazione (RTF)
- A partire dal 1° luglio 2024, il meccanismo RTF garantisce che solo le domande complete e debitamente documentate passino alla fase di valutazione. Ai richiedenti viene concesso un periodo di 60 giorni per colmare eventuali lacune individuate durante la selezione iniziale.
- Le domande incomplete saranno respinte in fase di selezione. La mancata risposta entro 60 giorni comporterà il rifiuto automatico della domanda.
Procedure migliorate per i prodotti NCE
Per NCE che rientrano nel«meccanismo 1+»(destinati alle malattie potenzialmente letali o gravemente invalidanti), il Consiglio ha approvato una serie di miglioramenti volti a facilitare e accelerare il processo di registrazione, con particolari benefici per i farmaci destinati alle malattie rare.
- Requisiti post-approvazione
- Dopo la registrazione del prodotto:
- Conformarsi ai requisiti di farmacovigilanza
- Segnalare reazioni avverse gravi ai farmaci (ADR)
- Attuare e mantenere i piani di gestione del rischio
- Dopo la registrazione del prodotto:
Ricorsi
Se leso da una decisione del comitato, il richiedente può ricorrere al Pharmacy and Poisons Appeal Tribunal.
Tempistiche
Il Dipartimento della Salute mira a completare il processo di registrazione entro circa 9 mesi dalla presentazione, a condizione che tutti i documenti siano completi. Questo aiuta a portare i farmaci per le malattie rare sul mercato in modo efficiente.
Consultazione e feedback
Il Consiglio può condurre consultazioni con le parti interessate e gli esperti del settore durante le fasi di valutazione e attuazione delle politiche.
Aggiornamenti continui
Rimani aggiornato controllando regolarmente:
- Il sito web ufficiale del Consiglio
- Annunci del Drug Office
Diagramma di flusso
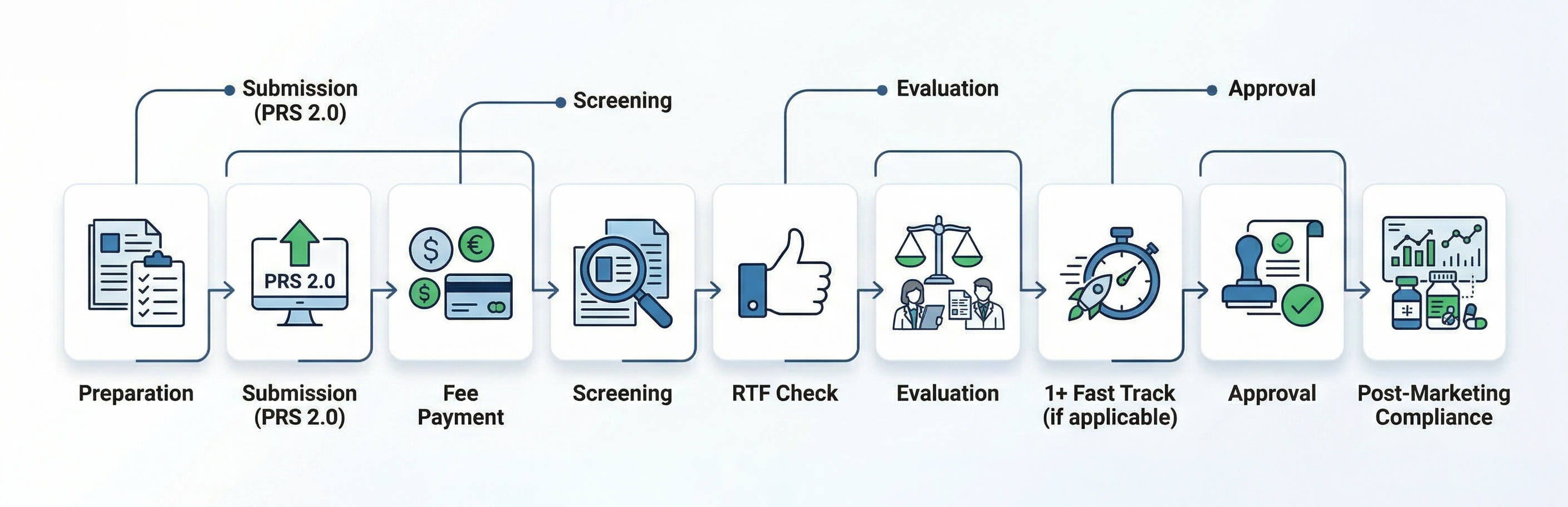
Come Freyr può essere d'aiuto
Freyr offre supporto End-to-End per la registrazione di farmaci orfani a Hong Kong, inclusa la preparazione del dossier, la navigazione nel PRS 2.0 e la conformità post-approvazione. Con l'esperienza locale e un approccio strategico, aiutiamo a garantire un ingresso sul mercato più rapido e conforme per i farmaci orfani per le malattie rare.









