Shonin (Approvazione Pre-Commercializzazione) è il percorso normativo per la registrazione dei dispositivi medici in Giappone. Il percorso Shonin è principalmente per la registrazione dei dispositivi medici di Classe II e III per i quali non sono disponibili gli standard di classificazione della PMDA. Anche per i dispositivi di Classe IV ad alto rischio, i produttori devono presentare la domanda Shonin. La PMDA è responsabile della revisione e dell'approvazione della domanda Shonin.
Quali sono le altre vie di registrazione dei dispositivi in Giappone?
Oltre a Shonin, i percorsi Todokede e Ninsho sono utilizzati anche per le approvazioni di dispositivi medici in Giappone. I produttori di dispositivi medici possono scegliere uno di essi a seconda della classe di rischio del dispositivo e della disponibilità di prodotti equivalenti in Giappone. Il produttore deve identificare la classificazione del dispositivo e ricercare la disponibilità dello Standard Industriale Giapponese (JIS) prima di determinare il percorso di registrazione applicabile.
- Todokede (Presentazione Pre-Commercializzazione) – È applicabile ai dispositivi di Classe I e richiede ai produttori di presentare una notifica pre-commercializzazione alla PMDA per l'approvazione.
- Ninsho (Certificazione Pre-Immissione sul Mercato) - Si applica ai dispositivi generici di Classe II e III che rispettano specifici standard di certificazione (Standard JIS). L'Organismo di Certificazione Registrato (RCB) si occupa di esaminare e approvare la richiesta.
Quali sono i prerequisiti per la registrazione Shonin?
I produttori che registrano i loro dispositivi attraverso il percorso Shonin devono pianificare meticolosamente le presentazioni. Devono garantire quanto segue:
- Presentazione dei dati generali del dispositivo, quali categoria del dispositivo medico, uso previsto, dati di analisi del rischio di efficacia, dati clinici, ecc.
- Fornitura del riepilogo della documentazione tecnica (STED).
- Fornitura di documenti solo in lingua giapponese.
- I produttori stranieri devono obbligatoriamente nominare un Marketing Authorization Holder (MAH) o un Designated Marketing Authorization Holder (DMAH)
- I produttori esteri devono ottenere il certificato di Registrazione del produttore estero (FMR) per i loro stabilimenti di produzione.
Quali sono i requisiti QMS per la registrazione dei dispositivi nell'ambito del percorso Shonin?
I produttori devono rispettare tutti i requisiti QMS definiti dall'Ordinanza 169. Lo sponsor o il DMAH o il MAH devono presentare domanda al PMDA. Il PMDA effettua un'ispezione dettagliata del QMS presso lo stabilimento del produttore e rilascia il certificato previa soddisfacente implementazione del QMS.
Qual è il processo di registrazione per l'approvazione dei dispositivi nell'ambito del percorso Shonin?
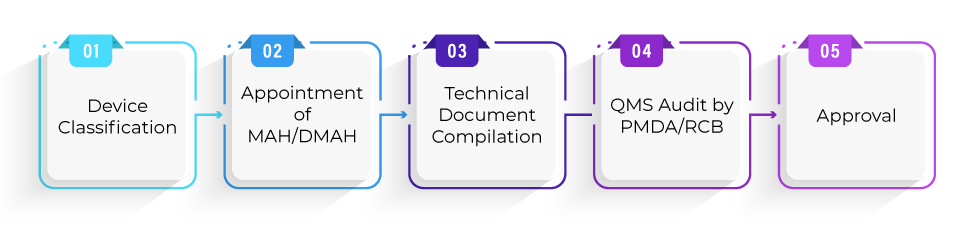
Qual è la tempistica media richiesta per l'approvazione dei dispositivi nell'ambito del percorso Shonin?
La PMDA richiede solitamente 12 mesi per la valutazione tecnica dalla data di ricezione della domanda Shonin. Il produttore deve considerare il tempo necessario per preparare i documenti di presentazione o condurre studi clinici nelle tempistiche del proprio progetto.
Esiste una scadenza per la registrazione dei dispositivi nell'ambito del percorso Shonin?
La registrazione dei dispositivi medici non scade, ma lo sponsor dovrebbe rinnovare i certificati del Sistema di Gestione della Qualità (QMS) ogni cinque anni.
Il Giappone è un mercato redditizio ma comporta intrinsecamente complessità normative e barriere linguistiche. I produttori devono considerare questi fattori e pianificare proattivamente la loro strategia di immissione sul mercato (GTM) per il Giappone. I produttori di dispositivi medici e IVD possono scegliere di esternalizzare tutte le sfumature normative a un partner normativo affidabile e utilizzare le risorse per concentrarsi su altri componenti essenziali.
Per saperne di più sull'approvazione dei dispositivi medici Shonin in Giappone o su qualsiasi altra normativa PMDA Japan, contattate oggi stesso gli esperti normativi di Freyr.
