
Jaka jest rola cyberbezpieczeństwa w wyrobach medycznych?
Proces zatwierdzania 510(k) to ścieżka regulacyjna stosowana przez Amerykańską Agencję ds. Żywności i Leków (US FDA) w celu oceny i wydania zgody na komercyjną dystrybucję wyrobów medycznych. Proces ten ma na celu zapewnienie, że wyroby medyczne są bezpieczne i skuteczne w użyciu dla pacjentów. US FDA definiuje cyberbezpieczeństwo jako „proces zapobiegania nieautoryzowanemu dostępowi, modyfikacji, niewłaściwemu użyciu lub odmowie użycia, a także nieautoryzowanemu wykorzystaniu informacji, które są przechowywane, dostępne lub przesyłane z wyrobu medycznego do zewnętrznego odbiorcy”.
Wyroby medyczne są coraz częściej podłączane do sieci i tym samym są podatne na zagrożenia cyberbezpieczeństwa, takie jak włamania, wycieki danych i ataki złośliwego oprogramowania. Zajęcie się cyberbezpieczeństwem na etapie projektowania i rozwoju jest kluczowe, aby zapewnić, że wyroby medyczne posiadają odpowiednie mechanizmy kontroli bezpieczeństwa. Zagrożeń i luk w zabezpieczeniach nie da się całkowicie wyeliminować, a zmniejszenie ryzyka cyberbezpieczeństwa jest szczególnie trudne. Jeśli cyberbezpieczeństwo nie jest odpowiednio utrzymywane, może to prowadzić do naruszenia funkcjonalności urządzeń, utraty danych osobowych lub medycznych oraz możliwości rozprzestrzeniania się zagrożeń bezpieczeństwa na inne połączone sieci lub urządzenia.
Incydenty spowodowane naruszeniem cyberbezpieczeństwa
Incydenty cyberbezpieczeństwa spowodowały, że wyroby medyczne i sieci szpitalne stały się niezdatne do użytku, co doprowadziło do zakłóceń w świadczeniu opieki nad pacjentami w placówkach opieki zdrowotnej w US. Takie cyberataki i exploity mogą również prowadzić do szkód u pacjentów z powodu zagrożeń klinicznych, na przykład opóźnienia w diagnozie i/lub leczeniu pacjentów.
Poniżej przedstawiono kluczowe incydenty w sektorze opieki zdrowotnej, które podkreślają znaczenie cyberbezpieczeństwa dla bezpieczeństwa pacjentów.
- W 2017 roku atak ransomware WannaCry dotknął systemy szpitalne i wyroby medyczne na całym świecie.
- W 2020 roku atak ransomware na niemiecki szpital uwydatnił potencjalne osiemdziesiąt trzy (83) skutki opóźnionej opieki nad pacjentami, ponieważ atak zmusił pacjentów do przekierowania do innego szpitala.
Kluczowe aspekty cyberbezpieczeństwa dla uzyskania zgody 510(k)
Poniżej przedstawiono ogólne zasady cyberbezpieczeństwa dla producentów wyrobów medycznych, zgodnie z wytycznymi US FDA dotyczącymi cyberbezpieczeństwa, specyficznymi dla zgłoszeń przed wprowadzeniem na rynek.
- Rozporządzenie w sprawie Systemu Jakości (QSR).: Producenci powinni zajmować się kwestiami cyberbezpieczeństwa już na etapie projektowania i rozwoju wyrobu medycznego, ponieważ może to prowadzić do bardziej solidnego i skutecznego zmniejszenia ryzyka dla pacjentów. Producenci powinni określić dane wejściowe do projektu związane z cyberbezpieczeństwem dla swojego urządzenia oraz podejście do zarządzania lukami w cyberbezpieczeństwie jako część walidacji oprogramowania i analizy ryzyka, wymaganej przez 21 CFR 820.30(g).
- Bezpieczeństwo projektu: Producenci wyrobów muszą zapewnić, że ich produkty są projektowane z uwzględnieniem bezpieczeństwa wyrobu. US FDA oceni adekwatność zabezpieczeń, opierając się na zdolności wyrobu do zapewnienia i wdrożenia celów bezpieczeństwa, takich jak autentyczność, autoryzacja, dostępność, poufność i bezpieczeństwo, oraz terminowa możliwość aktualizacji w całej architekturze systemu.
- Przejrzystość: Brak informacji o cyberbezpieczeństwie urządzenia, takich jak informacje niezbędne do integracji urządzenia ze środowiskiem użytkowania, a także informacje potrzebne użytkownikom do utrzymania cyberbezpieczeństwa przez cały cykl życia urządzenia, może wpłynąć na jego bezpieczeństwo i skuteczność. Aby rozwiać te obawy, ważne jest, aby użytkownicy urządzeń mieli dostęp do informacji dotyczących kontroli cyberbezpieczeństwa, potencjalnych zagrożeń i innych istotnych informacji.
- Dokumentacja zgłoszeniowa: Projektowanie i dokumentacja cyberbezpieczeństwa urządzenia powinny być dostosowane do poziomu ryzyka cybernetycznego danego urządzenia. Producenci powinni brać pod uwagę szerszy system, w którym urządzenie może być używane.
Rysunek 1: Typowe wyzwania i rozwiązania w zakresie cyberbezpieczeństwa 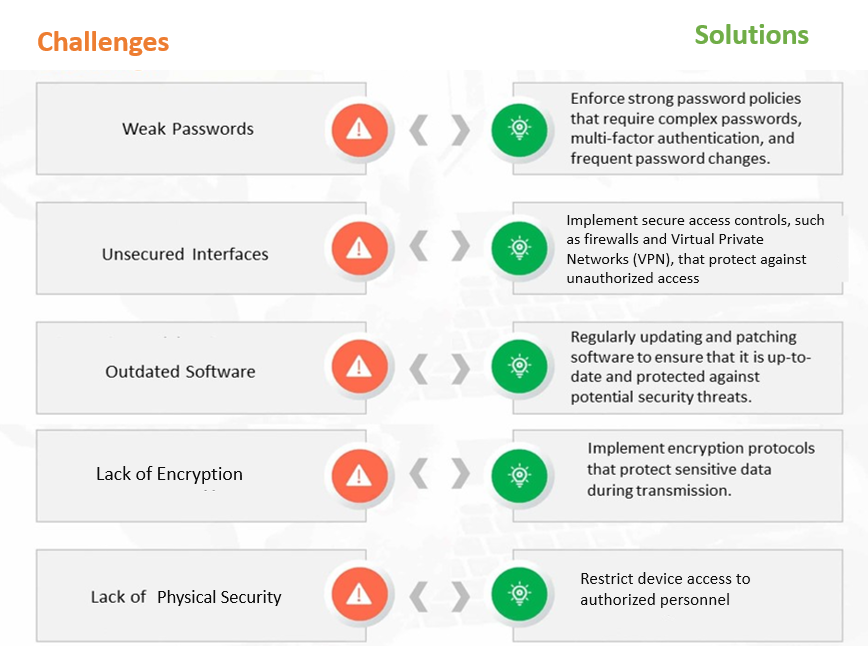
Podsumowanie
Podsumowując, cyberbezpieczeństwo w wyrobach medycznych jest kluczowe dla zapewnienia bezpieczeństwa pacjentów i zapobiegania incydentom, które mogą zakłócić świadczenie opieki zdrowotnej. Przepisy US FDA dotyczące cyberbezpieczeństwa podkreślają potrzebę, aby producenci zajmowali się kwestiami cyberbezpieczeństwa podczas projektowania i rozwoju wyrobów medycznych oraz dostarczali przejrzystych informacji na temat kontroli cyberbezpieczeństwa. QSR, bezpieczeństwo projektu, przejrzystość i dokumentacja zgłoszeniowa to kluczowe kwestie dla uzyskania zgody 510(k). Ważne jest również, aby rozwiązywać typowe wyzwania związane z cyberbezpieczeństwem, takie jak luki w komponentach stron trzecich i ataki ransomware, oraz wdrażać rozwiązania, takie jak solidna analiza ryzyka i regularne aktualizacje oprogramowania.
Aby przejść bezproblemowy i zgodny z przepisami proces zatwierdzania 510(k), skontaktuj się z naszymi ekspertami regulacyjnymi. Bądź na bieżąco! Zachowaj zgodność!









