
En el panorama farmacéutico actual, altamente regulado, mantener el cumplimiento de las buenas prácticas (GxP) no es solo una obligación legal, sino un compromiso con la seguridad de los pacientes y la calidad de los productos. A medida que las autoridades reguladoras de todo el mundo, incluidas la FDA EMA, intensifican su atención en los controles de fabricación y la uniformidad de los productos, la verificación continua de procesos (CPV) se ha convertido en una metodología transformadora para garantizar GxP continuo GxP a lo largo de todo el ciclo de vida del producto.
Comprender la verificación de procesos continuos
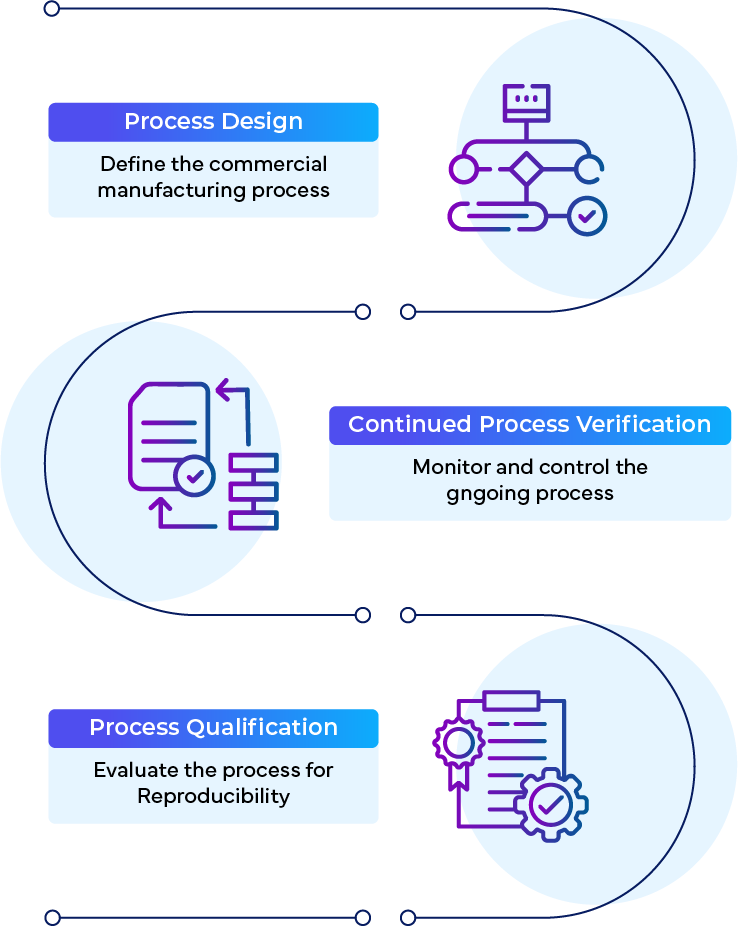
La CPV es una (1) de las tres (3) fases de la guía de validación de procesos FDA:
- Diseño de procesos
- Calificación de procesos
- Verificación continua del proceso
A diferencia de los enfoques de validación tradicionales, que a menudo se basan en gran medida en datos limitados procedentes de lotes previos a la comercialización, la CPV hace hincapié en la recopilación de datos en tiempo real y el análisis de tendencias durante la producción rutinaria. Este cambio de una gestión de la calidad reactiva a una proactiva permite a los fabricantes detectar desviaciones en los procesos, mitigar los riesgos de forma temprana y mantener un estado validado a lo largo de toda la vida comercial del producto.
Por qué el CPV supone un cambio revolucionario
- Control de calidad en tiempo real
Al recopilar y analizar datos durante cada ciclo de producción, CPV facilita la detección inmediata de anomalías. Esta información en tiempo real permite tomar decisiones más rápidas, lo que reduce el riesgo de comercializar productos que no cumplen los estándares y evita costosas retiradas del mercado. - Mejorado Cumplimiento normativo
Las autoridades reguladoras esperan cada vez más que las empresas farmacéuticas apliquen enfoques basados en el ciclo de vida para la validación. CPV respalda esta expectativa demostrando un estado de control continuo, alineándose con las directrices ICH , Q9 y Q10, y garantizando el cumplimiento de los requisitos de conformidad globales. - Optimización de costes
Aunque la implementación de CPV requiere una inversión inicial en tecnologías analíticas y formación, a la larga reduce los costes a largo plazo. Minimiza la necesidad de revalidaciones frecuentes, reduce los rechazos de lotes y mejora la eficiencia de la fabricación. - Toma de decisiones basada en datos
CPV utiliza herramientas estadísticas avanzadas y procesos automatizados para procesar grandes volúmenes de datos. Este enfoque estructurado de la gestión de datos contribuye a la planificación estratégica, la mejora continua y la gestión informada de riesgos, pilares fundamentales de los sistemas de calidad modernos.
Buenas prácticas de implementación
1. Definir los parámetros críticos del proceso (CPP)
Empiece por identificar y establecer los CPP y los atributos críticos de calidad (CQA) basándose en datos históricos y experimentales. Estas métricas sirven de base para la monitorización en tiempo real.
2. Aprovecha las herramientas digitales y la automatización
Integra el software CPV con tus sistemas de ejecución de la fabricación (MES) y tus sistemas de gestión de la información de laboratorio (LIMS). La automatización mejora la precisión de los datos, la frecuencia de los registros y la visualización de tendencias.
3. Colaboración interfuncional
Para que la implementación de la CPV tenga éxito, es necesaria la coordinación entre los equipos de control de calidad, fabricación y TI. El establecimiento de una estrategia unificada de CPV garantiza la coherencia y la responsabilidad compartida.
4. Desarrollar modelos sólidos de análisis de datos
Utilizar el control estadístico de procesos (SPC), el análisis multivariante y los algoritmos de aprendizaje automático para analizar tendencias, predecir desviaciones y contribuir a la mejora continua.
5. Adaptación a la normativa
Documenta todos los aspectos de tu proceso de CPV y asegúrate de que tu sistema esté preparado para una auditoría. Adapta tu documentación y tus prácticas a las expectativas normativas internacionales.
El CPV en la práctica: un ejemplo de caso
Pensemos en una empresa farmacéutica que fabrica inyectables estériles. Antes de la implantación del CPV, sus actividades de validación se centraban principalmente en tres (3) lotes previos a la comercialización. Las variaciones posteriores a la comercialización solían pasar desapercibidas hasta que surgían reclamaciones sobre el producto.
Al pasar al CPV, la empresa instaló sensores de temperatura y presión en tiempo real a lo largo de toda su línea de producción. Los datos se analizaron de forma continua mediante gráficos de control estadístico (SPC). Como resultado, detectaron una desviación leve pero recurrente en el volumen de llenado, con la suficiente antelación como para tomar medidas correctivas antes de que la desviación afectara a la calidad del producto. Este cambio no solo garantizó GxP , sino que también redujo significativamente el tiempo de inactividad y la necesidad de reelaborar el producto.
Conclusión
La verificación continua de procesos es más que un simple requisito normativo. Se trata de un enfoque estratégico para garantizar una calidad constante del producto, la eficiencia operativa y el cumplimiento de GxP en constante evolución. Con las herramientas adecuadas, la mentalidad correcta y el asesoramiento de expertos, las empresas farmacéuticas pueden transformar sus programas de validación e impulsar un cumplimiento normativo sostenido.
Deja que Freyr te guíe en tu experiencia con CPV
En Freyr, nos especializamos en servicios end-to-end y cumplimiento normativo para el sector farmacéutico. Tanto si acaba de iniciar la implementación de su sistema de CPV como si desea mejorar su sistema actual, nuestros expertos pueden ayudarle a diseñar, implementar y validar marcos de CPV sólidos y adaptados a sus necesidades.
¿Estás listo para mejorar tu GxP ? Póngase en contacto con Freyr hoy mismo para descubrir cómo podemos ayudarle a preparar sus operaciones farmacéuticas para el futuro.










