A nivel mundial, las Agencias de Salud exigen a los fabricantes extranjeros de Dispositivos Médicos e IVD que designen un representante local. En Japón, bajo la Ley revisada de Productos Farmacéuticos y Dispositivos Médicos (PMD), el sistema de Cuidador en el País (ICC) fue reemplazado por el sistema de Titular de Autorización de Comercialización (MAH). Bajo este sistema, las empresas deben obtener una licencia de MAH para conseguir la aprobación del dispositivo y comercializar los dispositivos en Japón.
El Titular de Autorización de Comercialización (MAH) debe ser una entidad local ubicada en Japón. Los fabricantes nacionales pueden obtener directamente la licencia de MAH, mientras que el fabricante extranjero deberá identificar una entidad local para cumplir con este requisito de MAH.
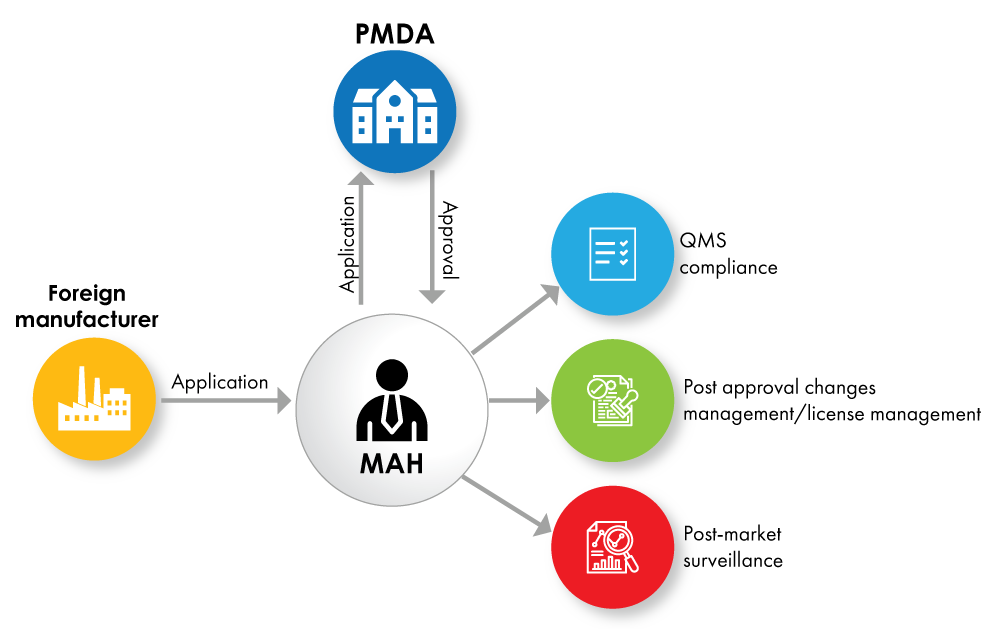
Fig. n.º 1: Diagrama de flujo de registro de Dispositivos Médicos con MAH como Titular de Licencia
Si los fabricantes extranjeros no desean ceder la propiedad total del producto al MAH, pueden designar a un Titular de Autorización de Comercialización Designado (DMAH). El DMAH presenta la solicitud en nombre del fabricante extranjero, y la aprobación se concede al fabricante extranjero para el dispositivo.
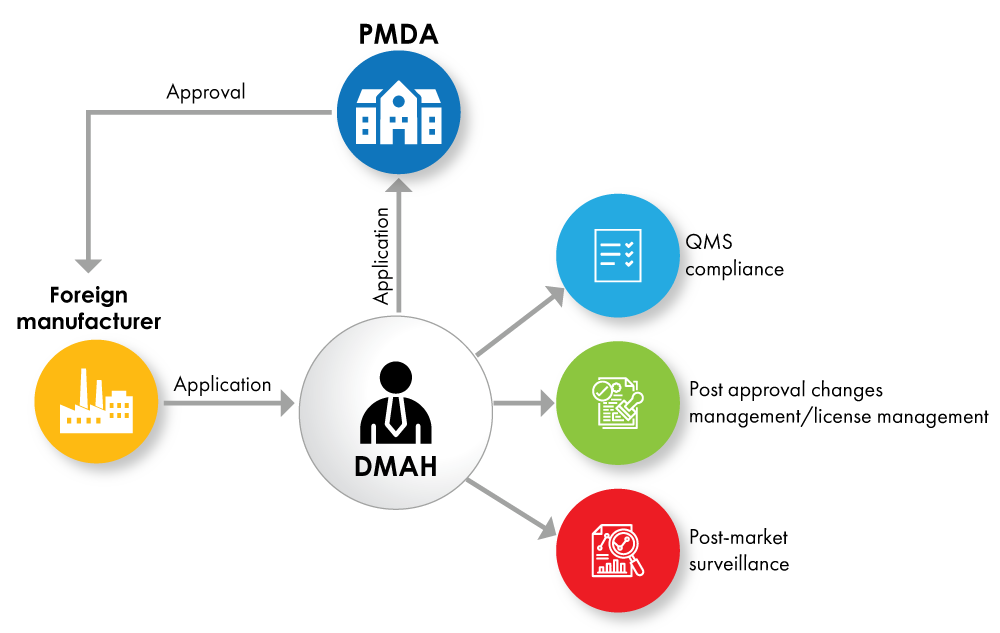
Fig. n.º 2: Diagrama de flujo de registro de dispositivos con DMAH como titular de la licencia
Existen tres (03) opciones posibles mediante las cuales el fabricante extranjero puede cumplir con el requisito de MAH de la PMDA. Los fabricantes extranjeros deben evaluar a fondo las tres (03) posibilidades. Estas incluyen:
Establecer una filial en Japón
Los fabricantes extranjeros pueden establecer una oficina local en Japón y actuar como MAH para lanzar sus productos en Japón. Esto permite al fabricante extranjero tener la propiedad total y una visibilidad completa de su(s) producto(s) en Japón. Esta podría no ser una opción preferida para fabricantes pequeños, ya que el costo asociado con el establecimiento de una filial en Japón y el mantenimiento de los requisitos de calidad del Ministerio de Salud, Trabajo y Bienestar (MHLW) es bastante elevado.
Distribuidor como MAH
Es una forma rentable para los fabricantes extranjeros que no tienen una oficina local en Japón. Los importadores o distribuidores pueden ser designados como MAH o DMAH. Considerando los ingresos generados por las ventas de dispositivos, los importadores y distribuidores generalmente no cobran tarifas adicionales por actuar como MAH o DMAH. Los fabricantes, sin embargo, enfrentan desafíos para lograr la penetración en el mercado, ya que el distribuidor que actúa como MAH podría no estar dispuesto a emitir un Certificado de No Objeción (NoC) a otros distribuidores. Los distribuidores, a veces, no cooperan con el fabricante extranjero en el cambio del MAH y la transferencia de la licencia del dispositivo al MAH/DMAH recién identificado.
Alianza con terceros
Los fabricantes extranjeros pueden designar a un proveedor de servicios externo independiente como su MAH/DMAH. La confidencialidad del dispositivo está bien protegida, y el fabricante extranjero controla la propiedad legal del producto. Los fabricantes pueden implementar y llevar a cabo sus planes de expansión de mercado.
Responsabilidades del Titular de la Autorización de Comercialización
Un MAH/DMAH actúa como representante en nombre del fabricante extranjero y asiste en la aprobación de dispositivos en Japón. Las principales responsabilidades de un MAH/DMAH incluyen:
- End-to-end aprobación de dispositivos
- Asegurar que dispositivos seguros y de calidad entren en el mercado japonés mediante la gestión adecuada de la fabricación y el control de calidad de los productos
- Ser responsable de la liberación del dispositivo a la parte que posee una licencia de venta/distribución de Dispositivos Médicos.
- Gestión de las actividades de Post-Market Surveillance (PMS)
Dado que el MAH/DMAH debe seguir todas las medidas de seguridad, del Sistema de Gestión de Calidad (QMS) y de Buenas Prácticas de Vigilancia (GVP) en nombre del fabricante extranjero, es extremadamente crítico elegir el MAH/DMAH adecuado. Por lo tanto, los fabricantes extranjeros deben evaluar a fondo todas las opciones antes de optar por el mejor modelo de MAH posible. Estas incluyen realizar un análisis de viabilidad, determinar el ROI, la relación con los importadores y distribuidores, el presupuesto disponible, el tamaño de la cartera, el beneficio por las ventas de dispositivos, los plazos para el lanzamiento del dispositivo, etc. Los fabricantes deben elegir meticulosamente si otorgan la propiedad del dispositivo al MAH o designan un DMAH y retienen la propiedad.
Para saber más sobre los requisitos de MAH/DMAH en Japón, contacte con un experto reglamentario en Freyr. Manténgase informado. Cumpla con la normativa.









