
Los Dispositivos Médicos se someten a una evaluación de conformidad antes de ser incluidos en la lista ARTG para asegurar que los dispositivos cumplan con los principios esenciales exigidos por la Therapeutic Goods Administration (TGA) de Australia. Los principios esenciales describen básicamente las características de seguridad y rendimiento que cualquier dispositivo debe cumplir para poder venderse en Australia. De forma similar al proceso en la UE, la evaluación de conformidad en Australia se basa en la clase de riesgo del dispositivo. Por lo tanto, la vía de evaluación de conformidad que debe seguir cualquier dispositivo depende de su clasificación.
Existen diversas normas reglamentarias que se aplican a varios tipos de dispositivos. El cumplimiento de una o más de estas normas es un requisito esencial. La identificación de las normas pertinentes aplicables al dispositivo y las pruebas posteriores del dispositivo para demostrar su cumplimiento con la norma se convierten en un requisito previo.
La evaluación de conformidad implica un examen sistemático de los documentos técnicos relacionados con el dispositivo. La gestión de riesgos, la evaluación clínica, el proceso de fabricación involucrado y las actividades de vigilancia gestionadas por el fabricante son las áreas críticas para la evaluación. Los dispositivos que requieren un certificado de evaluación de conformidad de la TGA se enumeran en el Reglamento 4.1 de las Reglamentaciones de Productos Terapéuticos (Dispositivos Médicos) de 2002. Si bien un certificado de evaluación de conformidad emitido por la TGA es un requisito previo para la comercialización de la mayoría de los Dispositivos Médicos en Australia, la TGA también acepta certificados de evaluación de conformidad emitidos por los Organismos Notificados en Europa. Además, la TGA también acepta la evaluación de conformidad de países que forman parte del MDSAP (Programa de Auditoría Única de Dispositivos Médicos).
Los requisitos de evaluación de la conformidad varían según la categoría de riesgo del dispositivo. La Tabla n.º 1 detalla el proceso de evaluación de la conformidad basado en la clasificación en Australia.
Proceso de Evaluación de la Conformidad - Australia
Clase | Procedimiento de Evaluación de la Conformidad. | Responsabilidades del fabricante |
| Yo | Parte 6 (Declaración de Conformidad, que no requiere evaluación por parte del Secretario) | Documentación para demostrar la conformidad con los Principios Esenciales |
| I (de medición) y IIa (no estéril) | Parte 6 (Declaración de Conformidad, que no requiere evaluación por parte del Secretario) Parte 5 (Sistema de gestión de calidad del producto) | Documentación para demostrar la conformidad con los Principios Esenciales. Implementar un sistema de gestión de calidad del producto para la inspección y pruebas finales para auditorías. Nota: No se requiere la presentación de la Declaración de Conformidad para la Clase I (no medidores y no estériles), pero debe estar disponible si la TGA lo solicita. |
| I (estéril) y IIa (estéril) | Parte 6 (Declaración de Conformidad, que no requiere evaluación por parte del Secretario) Parte 4 (Garantía de Calidad de la Producción) | Documentación para demostrar la conformidad con los Principios Esenciales. Implementar un sistema de gestión de calidad que excluye el elemento de diseño, basado en ISO 13485. |
| IIb | Parte 1 (Garantía de Calidad Total) excluyendo la Cláusula 1.6 (Examen del diseño) | Implementar un sistema de gestión de calidad completo que incluya diseño, producción, etiquetado, envasado e inspección final basado en ISO 13485. Excluye el expediente de diseño. |
| III & AIMD | Parte 1 (Garantía de Calidad Total) incluyendo la Cláusula 1.6 (Examen del diseño) | Implementar un sistema de gestión de calidad completo que incluya diseño, producción, etiquetado, envasado e inspección final basado en ISO 13485. Expediente de diseño de conformidad con los Principios Esenciales. |
| Sistemas o Kits de Procedimiento Parte 7 | (Procedimientos para Dispositivos Médicos utilizados con un fin especial) | Principios esenciales. Procedimiento de evaluación de la conformidad. Evidencia clínica para componentes individuales en un sistema o paquete. |
Tabla n.º 1. Requisitos de evaluación de la conformidad de los dispositivos
El proceso de aprobación habitual de Dispositivos Médicos por parte de la TGA es el siguiente:
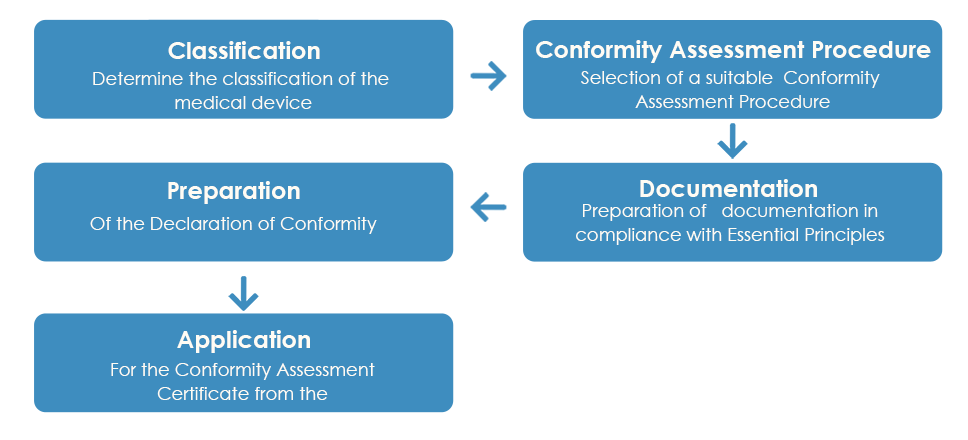
Como se detalla anteriormente, una vez que se recibe el Certificado de Evaluación de Conformidad de la TGA, el fabricante debe preparar una Declaración de Conformidad (DoC) que declare que el Dispositivo Médico cumple con los principios esenciales aplicables, las reglas de clasificación y la ruta de evaluación de conformidad. Sin embargo, a diferencia del Certificado de Evaluación de Conformidad, la TGA no acepta una DoC europea.
El mercado australiano ofrece un panorama prometedor para los fabricantes de Dispositivos Médicos, si se cumplen los requisitos reglamentarios de la Administración de Productos Terapéuticos (TGA). Los requisitos de conformidad y el proceso de evaluación varían según la clase de riesgo del dispositivo y del IVD. Aunque las reglamentaciones de Dispositivos Médicos están bien definidas y son transparentes, navegar por ellas es complejo y los fabricantes pueden buscar apoyo de los socios reglamentarios para el registro exitoso del dispositivo.
Para obtener información completa sobre los requisitos de evaluación de la conformidad, el Patrocinador Australiano y la inclusión en el ARTG en Australia, contacte a un experto reglamentario probado. Manténgase informado. Manténgase conforme.









