Ninsho (certificación de Dispositivos Médicos) es un sistema de certificación de terceros en Japón en el que un Organismo de Certificación Registrado (RCB), acreditado por el Ministro de Salud, Trabajo y Bienestar (MHLW), certifica Dispositivos Médicos designados de alta complejidad. Es aplicable a dispositivos de Clase II y a un número limitado de dispositivos de Clase III que tienen una Norma Industrial Japonesa (JIS) asociada. Algunos Dispositivos Médicos de Clase II sin criterios de certificación establecidos requieren aprobación bajo el programa Shonin.
¿Cuáles son las otras vías de registro de dispositivos en Japón?
En Japón, las vías Todokede y Shonin también se utilizan para las aprobaciones de Dispositivos Médicos, además de Ninsho. Dependiendo de la categoría de riesgo del dispositivo y de la disponibilidad de precedentes en Japón, el fabricante debe planificar cuidadosamente la presentación de su dispositivo.
¿Cuáles son los Requisitos previos para la Certificación Ninsho?
Los fabricantes que registran sus dispositivos a través de la vía Ninsho deben planificar meticulosamente las presentaciones en cuanto a lo siguiente:
- Selección de un RCB
- Presentación de datos generales del dispositivo, como la categoría del Dispositivo Médico, el uso previsto, los datos de análisis de riesgo de eficacia, los datos clínicos, etc.
- Proporcionar Resumen de la Documentación Técnica (STED).
- La provisión de documentos debe ser solo en idioma japonés.
- Los fabricantes extranjeros deben designar obligatoriamente un Titular de la Autorización de Comercialización (MAH) o un Titular de la Autorización de Comercialización Designado (DMAH)
- Los fabricantes extranjeros deben registrarse en el MHLW y obtener un certificado de Registro de Fabricantes Extranjeros (FMR) para sus establecimientos de fabricación.
¿Qué son los RCBs?
Los Organismos de Certificación Registrados (RCB) son organismos de certificación de terceros acreditados por el MHLW. Los RCB son responsables de revisar y certificar los Dispositivos Médicos elegibles y solicitados bajo la vía Ninsho. Los RCB también son responsables de llevar a cabo la auditoría de QMS de las instalaciones del fabricante.
¿Cuáles son los requisitos de QMS para el registro de dispositivos bajo la vía Ninsho?
Los fabricantes deben cumplir con todos los requisitos del Sistema de Gestión de Calidad (QMS) definidos en la Ordenanza 169. El MAH o DMAH debe presentar la solicitud a los RCB. Los RCB llevarán a cabo una inspección detallada del QMS en las instalaciones del fabricante y, tras la implementación satisfactoria del QMS, emitirán el certificado.
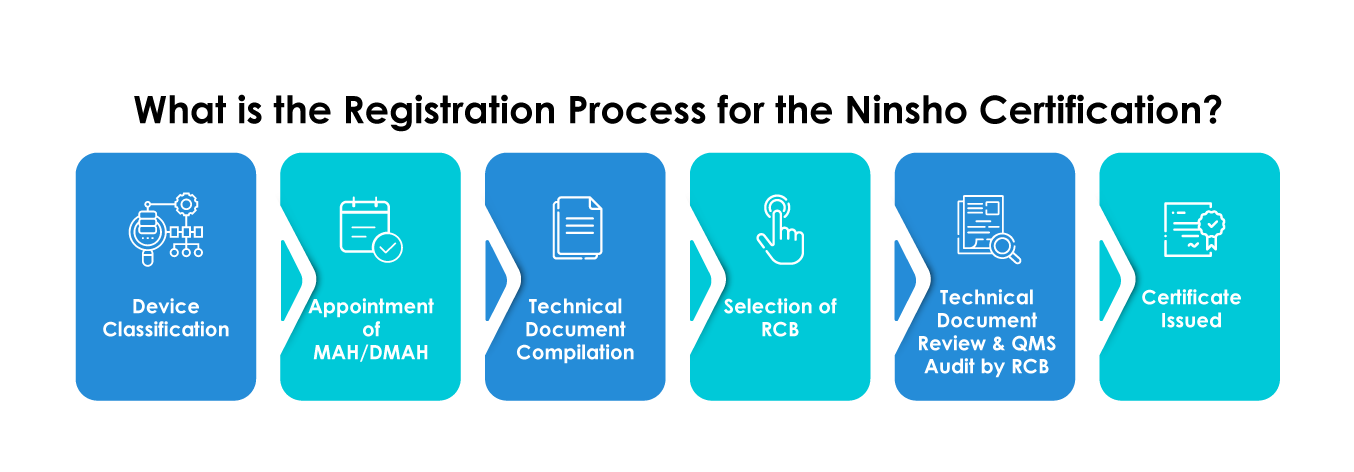
¿Cuál es el plazo promedio necesario para la certificación Ninsho?
El RCB normalmente requiere de tres (03) a cinco (05) meses para completar la evaluación técnica, ejecutar la auditoría del SGC y emitir el certificado Ninsho.
¿Existe algún plazo de caducidad para la Certificación Ninsho?
El registro de Dispositivos Médicos no caduca, pero el patrocinador debe renovar los certificados QMS cada cinco (05) años.
Japón, siendo el tercer mercado más grande para Dispositivos Médicos después de US y China, ofrece grandes oportunidades para los fabricantes de Dispositivos Médicos en todo el mundo. Los fabricantes que deseen comercializar sus dispositivos en Japón deben planificar cuidadosamente la certificación y aprobación de Dispositivos Médicos, ya que la PMDA tiene requisitos reglamentarios específicos. Los fabricantes pueden optar por un socio reglamentario fiable para un acceso sin complicaciones al mercado japonés.
Para saber más sobre la certificación de Dispositivos Médicos en Japón o cualquier otra regulación de la PMDA de Japón, Contacte a Freyr hoy mismo.
