Il Regolamento sui Dispositivi Medici dell'Unione Europea (EU MDR) 2017/745 definisce l'ambito dei dispositivi medici sterili come dispositivi che devono essere privi di microrganismi (batteri, virus, ecc.). I dispositivi di Classe I con funzione sterile possono anche ottenere un'autocertificazione, ma differisce in termini di requisiti rispetto ad altre sottocategorie di dispositivi di Classe I.
I requisiti per i dispositivi di Classe I variano notevolmente dalla produzione all'immissione del dispositivo sul mercato. Lo stesso vale per i dispositivi medici di Classe I con condizioni sterili. Ad esempio, se si tratta di un dispositivo di Classe I con funzione sterile, i requisiti per la produzione e l'istituzione di un Sistema di Gestione della Qualità (QMS) differirebbero notevolmente rispetto ai dispositivi di Classe I con funzioni di misurazione.
Questo articolo mira a fornire una breve checklist da considerare quando si immette un dispositivo di Classe I con condizioni sterili nell'Unione Europea. La checklist supporterà i produttori nel prendere decisioni informate riguardo a diversi aspetti.
Cosa fare!
Conoscere l'ambito prima della produzione
Secondo l'EU MDR, i dispositivi medici con funzioni sterili devono essere sviluppati e fabbricati con procedure appropriate per garantirne la sterilità fino alla loro immissione sul mercato. I dispositivi possono essere riutilizzati solo dopo appropriate procedure di pulizia, disinfezione e sterilizzazione.
La scelta delle pratiche di sterilizzazione appropriate
Ci sono diversi metodi di sterilizzazione che un produttore può scegliere per sterilizzare il dispositivo. Il metodo dell'ossido di etilene (EtO) è ampiamente utilizzato per sterilizzare i dispositivi medici. La scelta della sterilizzazione deve essere adeguatamente giustificata. Alcuni standard che i produttori possono seguire per stabilire, garantire e mantenere la sterilizzazione sono EN ISO 14937, ISO TS 21387, ISO TS 13004, ISO 11137 e altri.
Inoltre, si noti che la documentazione del metodo di sterilizzazione dettagliato, del metodo in-process e della convalida dei dati deve essere eseguita con precisione. Le informazioni sulla sterilizzazione, come la temperatura di riscaldamento, le condizioni ambientali, le convalide del processo, ecc., devono essere fornite in conformità ai requisiti dell'EU MDR.
Conoscere i requisiti e le linee guida da seguire
Uno dei passaggi fondamentali è documentare i requisiti tecnici e conoscere gli standard accettati nell'ambito del EU MDR. Ad esempio, la EN 556 è lo standard europeo per i dispositivi sterilizzati. La EN 556 descrive in dettaglio i requisiti per designare un dispositivo medico come sterile. Inoltre, la ISO TS 19930 specifica le strategie per garantire la sterilità dei dispositivi. Tuttavia, non è ancora stata adottata come standard UE.
Conoscere il proprio percorso
Per ottenere la marcatura CE, è importante essere informati sul coinvolgimento degli Organismi Notificati e sul percorso di valutazione della conformità da intraprendere. Inoltre, i dispositivi medici in condizioni sterili devono seguire gli Allegati IX e XI.
Il coinvolgimento di un Organismo Notificato è richiesto ma limitato. Nel caso di dispositivi sterili, il coinvolgimento degli Organismi Notificati riguarderà il mantenimento e la garanzia delle condizioni di sterilità. Ad esempio, le valutazioni di conformità includeranno valutazioni microbiologiche, metodi asettici, ecc.
Cosa non fare!
Non trascurare i requisiti di imballaggio ed etichettatura

Esistono requisiti aggiuntivi per la conformità dell'imballaggio e dell'etichettatura nei dispositivi sterili. Pur rispettando i requisiti di imballaggio ed etichettatura, non si devono dimenticare le informazioni che devono essere apposte. Il primo e più importante passo è apporre un simbolo di sterilità (menzionato di seguito) sull'etichettatura del dispositivo.
Devono essere incluse informazioni quali la dichiarazione di sterilità, il metodo di sterilizzazione, le istruzioni in caso di danneggiamento o apertura involontaria dell'imballaggio sterile, ecc. Inoltre, devono essere inclusi la durata di conservazione del prodotto sterile e il processo di risterilizzazione (se applicabile). Il numero di identificazione di un Organismo Notificato deve essere apposto anche sul dispositivo.
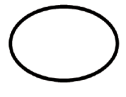
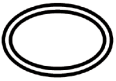
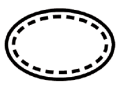
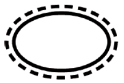
Alcuni dei simboli che devono essere aggiunti (a seconda dell'applicabilità) nell'etichettatura dei dispositivi medici sterili sono:
Simbolo | Indicazione |
| Dispositivi medici sterili con metodo di sterilizzazione utilizzato come tecnica asettica |
| Dispositivi medici sterili con metodo di sterilizzazione utilizzato come ossido di etilene |
| Dispositivi medici sterili con metodo di sterilizzazione utilizzato come calore secco o vapore |
| Dispositivi medici sterili con sterilizzazione a perossido di idrogeno vaporizzato |
| Dispositivi medici sterili con metodo di sterilizzazione utilizzato come radiazione |
| Il dispositivo non può essere sterilizzato di nuovo |
| Il dispositivo non è sterilizzato |
| Non utilizzatelo se la confezione è danneggiata |
| Sistema a barriera sterile singolo |
| Sistema a doppia barriera sterile |
| Sistema a barriera sterile singolo con imballaggio protettivo interno |
| Sistema a barriera sterile singolo con imballaggio protettivo esterno |
Non dimenticare i requisiti per l'immissione post-commercializzazione
I dispositivi sterili sono tenuti a mantenere un registro degli eventi avversi in caso di qualsiasi occorrenza. In questo caso, gli incidenti registrati, come i documenti, devono essere prodotti dalle autorità competenti su richiesta.
L'EU MDR ha requisiti specifici per quanto riguarda l'autocertificazione. È una procedura complessa, il fattore principale sono le diverse classi all'interno del dispositivo di Classe I e i loro diversi aspetti dei requisiti per ottenere la marcatura CE. I produttori con dispositivi di Classe I in condizioni sterili dovrebbero essere consapevoli della definizione dell'ambito e dei requisiti specifici.
Desideri comprendere in dettaglio i vari aspetti dei dispositivi sterili di classe I? Ti piacerebbe discuterne con un esperto comprovato? Contattaci.