
Nell'odierno panorama farmaceutico altamente regolamentato, garantire la conformità alle buone pratiche (GxP) non è solo un obbligo di legge, ma anche un impegno a favore della sicurezza dei pazienti e della qualità dei prodotti. Poiché le autorità di regolamentazione di tutto il mondo, tra cui la FDA EMA, prestano sempre maggiore attenzione ai controlli di produzione e all'uniformità dei prodotti, la verifica continua dei processi (CPV) si è affermata come una metodologia rivoluzionaria per garantire GxP in ogni fase del ciclo di vita del prodotto.
Comprendere la verifica continua dei processi
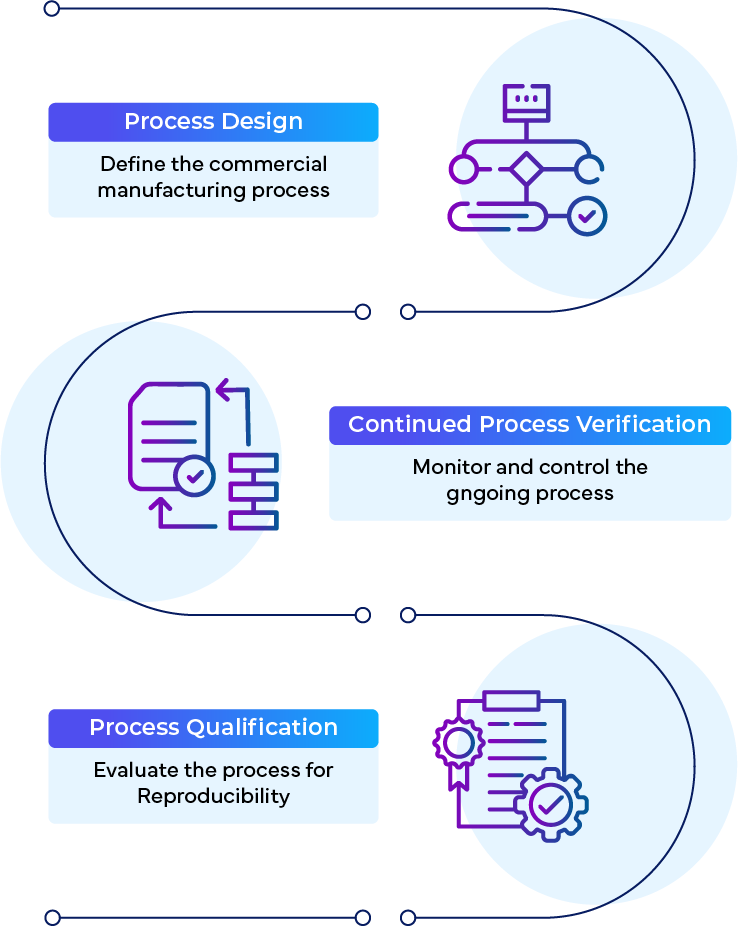
Il CPV è una (1) delle tre (3) fasi previste dalla linea guida FDAsulla convalida dei processi:
- Progettazione dei processi
- Qualificazione dei processi
- Verifica continua del processo
A differenza degli approcci di convalida tradizionali, che spesso si basano in larga misura sui dati limitati provenienti dai lotti pre-commercializzazione, la CPV pone l'accento sulla raccolta di dati in tempo reale e sull'analisi delle tendenze durante la produzione di routine. Questo passaggio da una gestione della qualità reattiva a una proattiva consente produttori individuare le deviazioni di processo, mitigare i rischi in fase precoce e mantenere uno stato di convalida per tutta la durata di vita commerciale del prodotto.
Perché il CPV rappresenta una svolta epocale
- Controllo qualità in tempo reale
Grazie alla raccolta e all'analisi dei dati durante ogni ciclo produttivo, CPV consente di individuare immediatamente eventuali anomalie. Queste informazioni in tempo reale permettono di prendere decisioni più rapide, riducendo il rischio di immettere sul mercato prodotti non conformi e prevenendo costosi richiami. - Migliorata Conformità normativa
Le autorità di regolamentazione si aspettano sempre più che le aziende farmaceutiche adottino approcci basati sul ciclo di vita per la convalida. CPV soddisfa questa aspettativa dimostrando uno stato di controllo continuo, allineandosi alle linee guida ICH , Q9 e Q10 e garantendo la conformità ai requisiti globali. - Ottimizzazione dei costi
Sebbene l'implementazione del CPV richieda un investimento iniziale in tecnologie analitiche e formazione, essa consente in definitiva di ridurre i costi a lungo termine. Riduce al minimo la necessità di frequenti rivalidazioni, diminuisce i rifiuti di lotti e migliora l'efficienza produttiva. - Processo decisionale basato sui dati
CPV si avvale di strumenti statistici avanzati e dell'automazione per elaborare grandi quantità di dati. Questo approccio strutturato alla gestione dei dati favorisce la pianificazione strategica, il miglioramento continuo e una gestione informata dei rischi: elementi fondamentali dei moderni sistemi di qualità.
Migliori pratiche di implementazione
1. Definizione dei parametri critici di processo (CPP)
Iniziare identificando e stabilendo i CPP e gli attributi critici di qualità (CQA) sulla base dei dati storici e sperimentali. Questi parametri costituiscono la base per il monitoraggio in tempo reale.
2. Sfruttare gli strumenti digitali e l'automazione
Integrare il software CPV con i sistemi di esecuzione della produzione (MES) e i sistemi di gestione delle informazioni di laboratorio (LIMS). L'automazione migliora l'accuratezza dei dati, la frequenza delle letture e la visualizzazione delle tendenze.
3. Collaborazione interfunzionale
Per garantire il successo dell'implementazione del CPV è necessario il coordinamento tra i team di controllo qualità, produzione e IT. La definizione di una strategia CPV unificata assicura coerenza e responsabilità condivisa.
4. Sviluppare modelli affidabili di analisi dei dati
Utilizzare il controllo statistico di processo (SPC), l'analisi multivariata e gli algoritmi di apprendimento automatico per analizzare le tendenze, prevedere gli scostamenti e favorire il miglioramento continuo.
5. Allineamento normativo
Documentate ogni aspetto del vostro processo CPV e assicuratevi che il vostro sistema sia pronto per gli audit. Allineate la vostra documentazione e le vostre procedure alle aspettative normative globali.
Il CPV in pratica: un caso esemplificativo
Si prenda ad esempio un'azienda farmaceutica che produce medicinali iniettabili sterili. Prima dell'implementazione del CPV, le attività di convalida si concentravano principalmente su tre (3) lotti pre-commercializzazione. Le variazioni post-commercializzazione spesso passavano inosservate fino a quando non venivano segnalati reclami sul prodotto.
Passando al CPV, l'azienda ha installato sensori di temperatura e pressione in tempo reale lungo tutta la linea di produzione. I dati sono stati analizzati costantemente tramite grafici SPC. Di conseguenza, è stato possibile individuare una variazione minima ma ricorrente nel volume di riempimento, con sufficiente anticipo da poter adottare misure correttive prima che la deviazione compromettesse la qualità del prodotto. Questo cambiamento non solo ha garantito GxP , ma ha anche ridotto in modo significativo i tempi di fermo e le rilavorazioni dei prodotti.
Conclusione
La verifica continua dei processi va ben oltre il semplice adempimento degli obblighi normativi. Si tratta di un approccio strategico volto a garantire una qualità costante dei prodotti, l'efficienza operativa e la conformità agli GxP in continua evoluzione. Con gli strumenti adeguati, la mentalità giusta e la guida di esperti, le aziende farmaceutiche possono trasformare i propri programmi di convalida e garantire una conformità duratura.
Lascia che Freyr ti guidi nel tuo percorso con il CPV
Noi di Freyr siamo specializzati in servizi end-to-end e conformità per l'industria farmaceutica. Che stiate appena iniziando a implementare il CPV o che vogliate migliorare il vostro sistema attuale, i nostri esperti possono aiutarvi a progettare, implementare e convalidare solidi sistemi CPV su misura per le vostre esigenze.
Sei pronto a migliorare GxP tua GxP ? Contatta Freyr oggi stesso per scoprire come possiamo aiutarti a rendere le tue operazioni farmaceutiche a prova di futuro.










