
I dispositivi medici sono sottoposti a valutazione della conformità prima di essere inclusi nell'elenco ARTG per garantire che i dispositivi siano conformi ai principi essenziali richiesti dalla Therapeutic Goods Administration (TGA), Australia. I principi essenziali delineano fondamentalmente le caratteristiche di sicurezza e prestazione che qualsiasi dispositivo dovrebbe soddisfare, in modo che possa essere venduto in Australia. Similmente al processo nell'UE, la valutazione della conformità in Australia si basa sulla classe di rischio del dispositivo. Pertanto, il percorso di valutazione della conformità da seguire per qualsiasi dispositivo dipende dalla sua classificazione.
Esistono vari standard normativi che si applicano a diversi tipi di dispositivi. La conformità a uno o più standard è un requisito essenziale. L'identificazione degli standard pertinenti applicabili al dispositivo e il successivo collaudo del dispositivo per dimostrarne la conformità allo standard diventano un prerequisito.
La valutazione di conformità implica un esame sistematico dei documenti tecnici relativi al dispositivo. La gestione del rischio, la valutazione clinica, il processo di fabbricazione coinvolto e le attività di vigilanza gestite dal fabbricante sono le aree critiche per la valutazione. I dispositivi per i quali è richiesto un certificato di valutazione di conformità TGA sono elencati nel Regolamento 4.1 del Therapeutic Goods (Medical Devices) Regulations 2002. Sebbene un certificato di valutazione di conformità rilasciato dalla TGA sia un prerequisito per la commercializzazione della maggior parte dei dispositivi medici in Australia, la TGA accetta anche certificati di valutazione di conformità rilasciati dagli Organismi Notificati in Europa. Inoltre, la TGA accetta anche valutazioni di conformità da paesi che fanno parte del MDSAP (Medical Device Single Audit Program).
I requisiti di valutazione della conformità variano in base alla categoria di rischio del dispositivo. La Tabella n. 1 illustra in dettaglio il processo di valutazione della conformità basato sulla classificazione in Australia.
Processo di valutazione della conformità - Australia
Classe | Procedura di valutazione della conformità | Responsabilità del produttore |
| I | Parte 6 (Dichiarazione di conformità, che non richiede la valutazione da parte del Segretario) | Documentazione per dimostrare la conformità ai Principi Essenziali |
| I (con funzione di misurazione) e IIa (non sterile) | Parte 6 (Dichiarazione di conformità, che non richiede la valutazione da parte del Segretario) Parte 5 (Sistema di gestione della qualità del prodotto) | Documentazione per dimostrare la conformità ai Principi Essenziali. Implementare un sistema di gestione della qualità del prodotto per l'ispezione finale e i test per gli audit. Nota: la presentazione della Dichiarazione di Conformità non è richiesta per la Classe I (non di misurazione e non sterile), ma dovrebbe essere disponibile su richiesta della TGA. |
| I (sterile) e IIa (sterile) | Parte 6 (Dichiarazione di conformità, che non richiede la valutazione da parte del Segretario) Parte 4 (Garanzia di qualità della produzione) | Documentazione per dimostrare la conformità ai Principi Essenziali. Implementare un sistema di gestione della qualità che esclude l'elemento di progettazione, basato sulla ISO 13485. |
| IIb | Parte 1 (Garanzia di qualità completa) esclusa la Clausola 1.6 (Esame della progettazione) | Implementare un sistema di gestione della qualità completo inclusi progettazione, produzione, etichettatura, confezionamento e ispezione finale basato sulla ISO 13485. Esclude il fascicolo di progettazione. |
| III & AIMD | Parte 1 (Garanzia di qualità completa) inclusa la Clausola 1.6 (Esame della progettazione) | Implementare un sistema di gestione della qualità completo che includa progettazione, produzione, etichettatura, imballaggio e ispezione finale, basato sulla ISO 13485. Fascicolo di progettazione in conformità ai Principi Essenziali. |
| Sistemi o kit procedurali Parte 7 | (Procedure per Dispositivi Medici Usati per uno Scopo Speciale) | Principi essenziali. Procedura di valutazione della conformità. Evidenza clinica per il singolo componente nel sistema o nella confezione. |
Tabella N.1. Requisiti di Valutazione della Conformità dei Dispositivi
Il consueto processo di approvazione dei dispositivi medici da parte della TGA è il seguente:
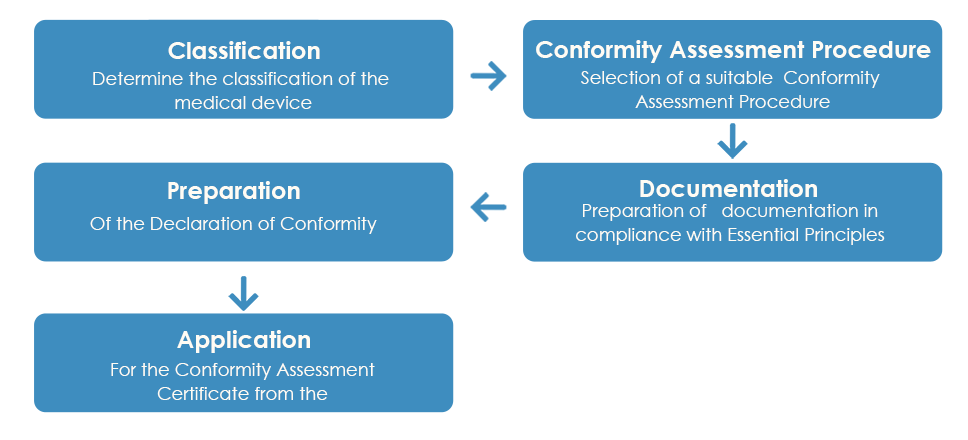
Come dettagliato sopra, una volta ricevuto il Certificato di Valutazione della Conformità dalla TGA, il fabbricante deve preparare una Dichiarazione di Conformità (DoC) dichiarando che il dispositivo medico è conforme ai principi essenziali applicabili, alle regole di classificazione e al percorso di valutazione della conformità. Tuttavia, a differenza del Certificato di Valutazione della Conformità, una DoC europea non è accettata dalla TGA.
Il mercato australiano offre uno scenario promettente per i produttori di dispositivi medici, a condizione che siano soddisfatti i requisiti normativi della Therapeutic Goods Administration (TGA). I requisiti di conformità e il processo di valutazione variano in base alla classe di rischio del dispositivo e dell'IVD. Sebbene le normative sui dispositivi medici siano ben definite e trasparenti, orientarsi tra esse è complesso e i produttori possono cercare supporto dai partner normativi per la registrazione di successo del dispositivo.
Per ottenere approfondimenti completi sui requisiti di valutazione della conformità, sullo Sponsor australiano e sull'inserimento nell'ARTG in Australia, contattate un esperto normativo comprovato. Rimanete informati. Rimanete conformi.









