
El software para Dispositivos Médicos en Corea del Sur se utiliza para diagnosticar, tratar y monitorizar a los pacientes en el sistema de atención médica moderno. Comprende tanto software integrado en Dispositivos Médicos como software independiente que puede utilizarse en PC, dispositivos móviles y servicios basados en la web. El Ministerio de Seguridad Alimentaria y Farmacéutica (MFDS) de Corea del Sur es responsable de regular el software para Dispositivos Médicos y garantizar su seguridad y eficacia. El 5 de julio de 2023, el MFDS estableció criterios para la aprobación e inspección del software para Dispositivos Médicos; estas regulaciones proporcionan una estructura que los solicitantes pueden seguir al presentar software para su aprobación o revisión.
Las regulaciones abordan una variedad de temas, incluyendo el alcance de la aplicación, los requisitos de documentación técnica y los informes de verificación de cumplimiento. Existen estándares y directrices internacionales que se aplican al software de Dispositivos Médicos, además de las directrices de la MFDS, como el estándar IEC (International Electrotechnical Commission) 62304 para los procesos del ciclo de vida del software y la guía de la Administración de Alimentos y Medicamentos de los Estados Unidos (US FDA) sobre aplicaciones médicas móviles.
Plan de desarrollo de software y análisis de requisitos
- El plan de desarrollo de software describe el enfoque general para el desarrollo de software, incluyendo especificaciones, métodos y herramientas de desarrollo. También cubre la verificación, la gestión de riesgos de Dispositivos Médicos, la gestión de configuración y la documentación.
- Análisis de Requisitos establece los requisitos de software para Dispositivos Médicos, incluyendo medidas de control de riesgos y métodos de verificación. Al planificar y analizar cuidadosamente el proceso de desarrollo de software, los desarrolladores pueden garantizar que el software resultante cumpla con los estándares necesarios de seguridad y eficacia.
- El informe de verificación de conformidad del software incluye un esquema del plan de desarrollo de software, el número de control de documentos del fabricante y una visión general del análisis de requisitos. Al adherirse a estas directrices, el software de Dispositivos Médicos puede desarrollarse con confianza, sabiendo que ha sido sometido a pruebas rigurosas y que cumple con los estándares necesarios de seguridad y eficacia.
Verificación y Validación del Software para Dispositivos Médicos
- Verificación de software de Dispositivos Médicos asegura que el software cumple con los requisitos especificados.
- Validación de software de Dispositivos Médicos asegura que el software satisface las necesidades del usuario y el(los) uso(s) previsto(s).
- Informe de verificación y validación de software de Dispositivos Médicos describe el proceso de verificación y validación, incluyendo el nombre del producto, la revisión y los nombres de las personas que examinaron y aprobaron el informe. El informe puede variar, dependiendo de las características del software, pero debe incluir una descripción del software, los métodos de verificación y validación utilizados, y los resultados de las pruebas.
Entorno operativo y software de origen desconocido (SOUP)
- Si el software depende de hardware específico, como el software integrado, el documento técnico debe describir las especificaciones del hardware.
- Sin embargo, si el software es independiente y está desarrollado para funcionar en hardware de propósito general, el entorno operativo debe describirse en el material de origen. Esto incluye las especificaciones mínimas recomendadas, como Microsoft Windows 10 o superior.
- Además, si el software de Dispositivos Médicos incluye Software Comercial de Origen Desconocido (SOUP), se debe crear un entorno operativo para garantizar un funcionamiento adecuado. Al describir cuidadosamente el entorno operativo y abordar cualquier SOUP, los desarrolladores pueden asegurar que su software de Dispositivos Médicos sea seguro y eficaz para su uso previsto.
Gestión de Riesgos y Requisitos de Documentación de Dispositivos Médicos
- El proceso de gestión de riesgos del software como dispositivo médico incluye identificar situaciones peligrosas, establecer medidas de control de riesgos, verificar esas medidas y gestionar los cambios del software.
- El documento MFDS-RM de gestión de riesgos de software proporciona información sobre la gestión de riesgos de software.
- Además, los requisitos de documentación son esenciales para garantizar que el software cumpla con los estándares necesarios de seguridad y eficacia.
- El plan de desarrollo de software, el análisis de requisitos de software para dispositivos médicos y los informes de verificación y validación de software deben incluirse en la documentación.
- El Informe de Verificación de Conformidad del Software describe los requisitos de documentación; también incluye un resumen de los documentos aplicables y el número de control de documentos del fabricante.
Figura 1: Proceso de gestión de riesgos de Dispositivos Médicos
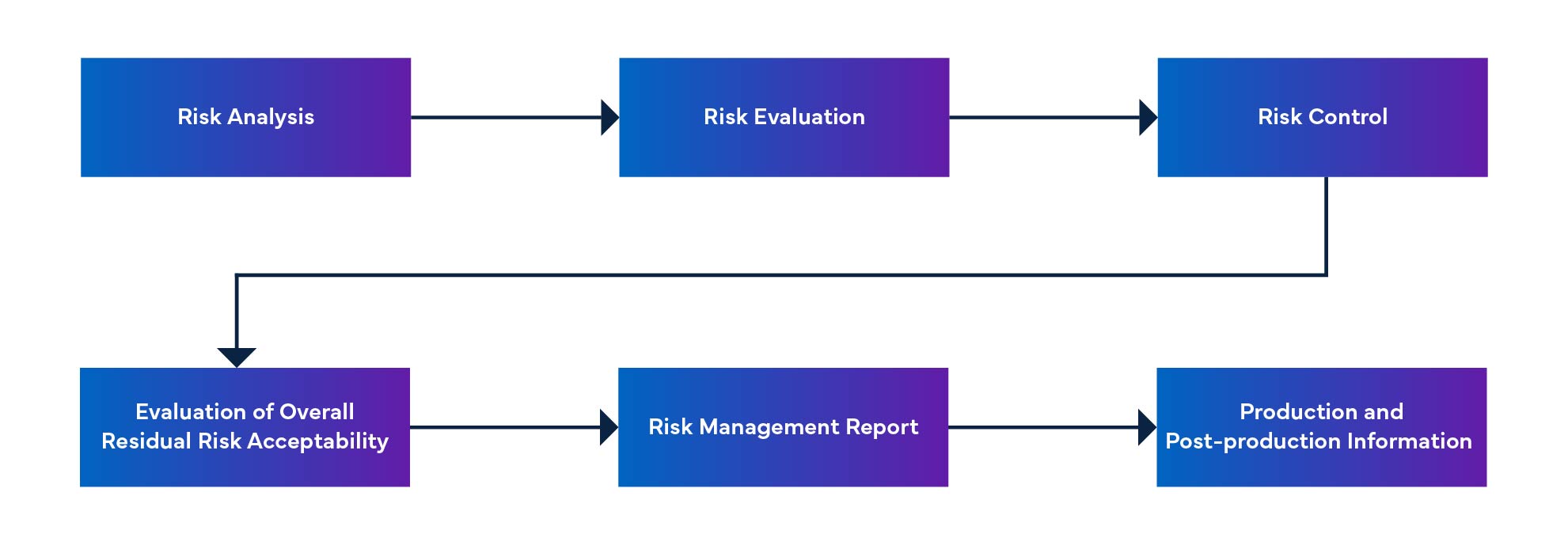
Anomalías no resueltas y acciones correctivas para el software SaMD
- El documento MFDS-PR (Resolución de Problemas de Software) describe el proceso de resolución de problemas de software, que incluye la notificación, el análisis, la implementación y la verificación de problemas.
- El documento también incluye una lista de problemas no resueltos, errores, defectos y anomalías, así como una evaluación de riesgos residuales para el sistema de software.
- Las acciones correctivas tomadas para abordar estos problemas deben documentarse en el plan de mantenimiento del software, el cual se establece de acuerdo con el proceso de mantenimiento del software.
- El documento de mantenimiento del MFDS proporciona información sobre el mantenimiento y la resolución de problemas del software SaMD.
Revisión de documentos técnicos y requisitos de presentación para software SaMD
Los principales documentos de revisión durante el proceso de revisión son los datos de rendimiento, el informe de confirmación de conformidad y los datos de verificación y validación del software de Dispositivos Médicos, la Especificación de Diseño de Software (SDS), la Declaración de Requisitos de Software (SRS) de Dispositivos Médicos y los informes de verificación y validación. El Informe de Confirmación de Conformidad y el Informe de Verificación y Validación del Software de Dispositivos Médicos deben presentarse.
Gestión de Riesgos del Software para Dispositivos Médicos
- Identificar los peligros potenciales asociados con el software y su uso.
- Evaluación de la gravedad de los riesgos asociados a estos peligros.
- Implementar medidas de control de riesgos para minimizar la probabilidad de daño.
- Supervisión y revisión de la eficacia de estas medidas de control de riesgos.
- Documentación de todas las actividades y decisiones de gestión de riesgos de Dispositivos Médicos.
En un sistema de software, los elementos de software se dividen en partes más pequeñas, incluyendo elementos de software detallados. Cuando un elemento no se puede dividir más, se denomina unidad. El sistema permite la división hasta el nivel de unidad, lo que ayuda a determinar el nivel de seguridad para cada elemento de software. Al unir estos elementos de software, podemos determinar el nivel de seguridad para todo el sistema de software.
Figura 2: Desmontaje e integración de software de Dispositivos Médicos
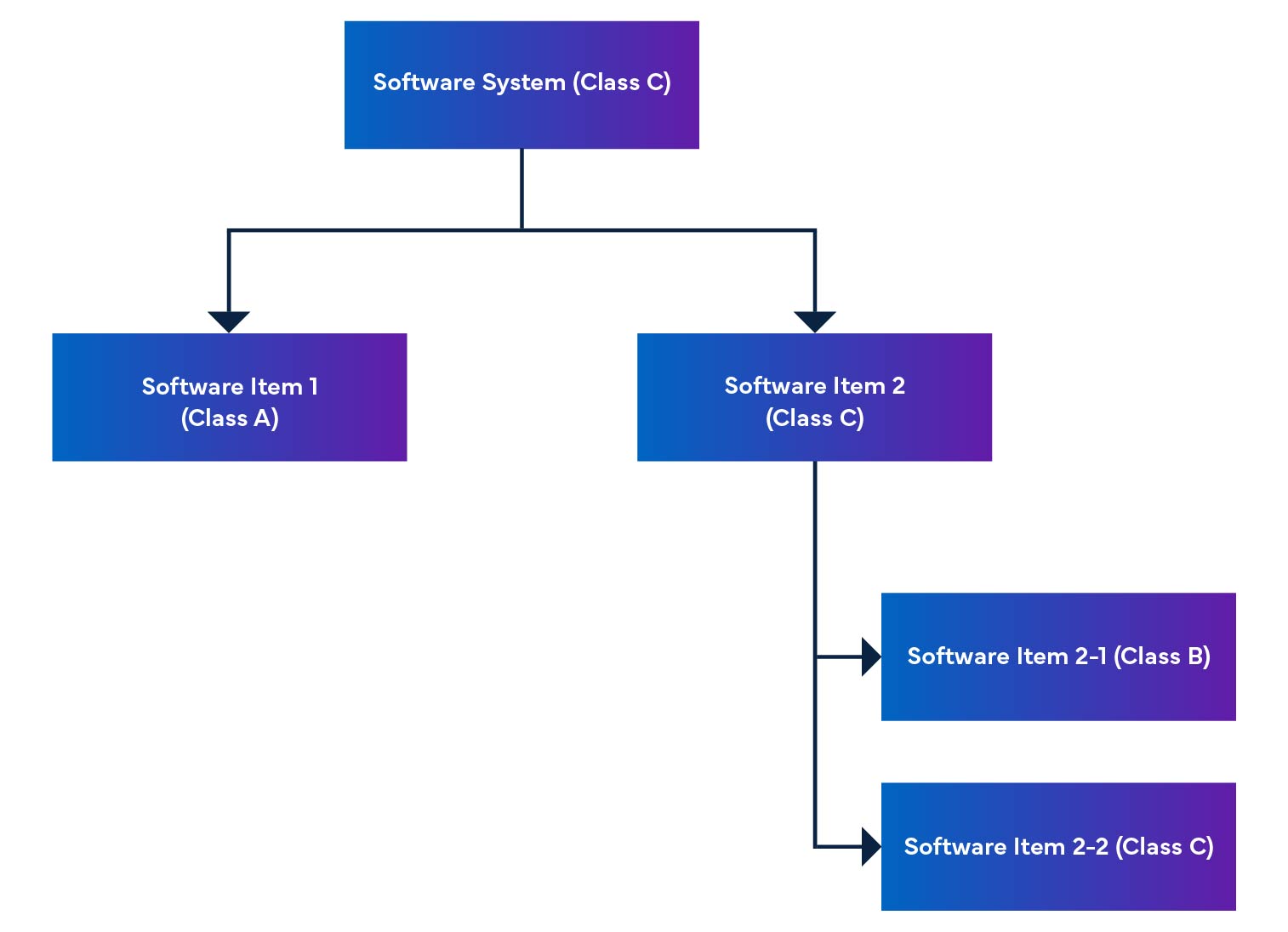
La normativa también menciona la clasificación de seguridad del software, que es una clasificación para identificar los riesgos del software SaMD (véase la Tabla 1).
Tabla 1: Definición de la clasificación de seguridad
| Calificación | Definición de Clase de Seguridad del Software para Dispositivos Médicos |
| Clase A | Sin posibilidad de lesiones o daños corporales. |
| Clase B | Es probable que ocurran lesiones menos graves (lesiones leves). |
| Clase C | Posibilidad de lesiones graves o la muerte. |
Gestión de la configuración del software
- Mantener documentación precisa y actualizada para todas las versiones, cambios y actualizaciones de software.
- Garantizar que toda la documentación sea debidamente revisada y aprobada.
- Implementar procedimientos para gestionar los cambios en la configuración del software.
- Documentación de todas las actividades y decisiones de gestión de la configuración del software.
Mantenimiento de software
- Probar y monitorear el software regularmente para asegurar que siga siendo seguro y efectivo para su uso previsto.
- Implementar procedimientos para abordar cualquier problema que pueda surgir, incluyendo correcciones de errores y actualizaciones de software.
- Documentación de todas las actividades y decisiones de mantenimiento del software.
Resolución de problemas
- Identificar la causa raíz del problema.
- Implementar acciones correctivas para abordar el problema.
- Documentación de todo el proceso de resolución de problemas para futuras referencias.
Al seguir las directrices anteriores, los desarrolladores pueden asegurarse de que cualquier problema con el software de sus Dispositivos Médicos se aborde y documente adecuadamente, y de que el software cumpla los requisitos necesarios para su aprobación o examen.
Si es un fabricante de dispositivos médicos que busca cumplir con los estándares de software para dispositivos médicos de Corea del Sur, los expertos reglamentarios de Freyr pueden guiarle a través del intrincado panorama reglamentario del país. Nos aseguraremos de que sus dispositivos se ajusten a las últimas regulaciones de dispositivos médicos de Corea del Sur para un cumplimiento sin problemas. ¡Contáctenos para saber más!










